Struktura Tripolifosforan Sodu (Na5P3O10), właściwości, zastosowania, uderzenie
- 3012
- 360
- Maksymilian Kępa
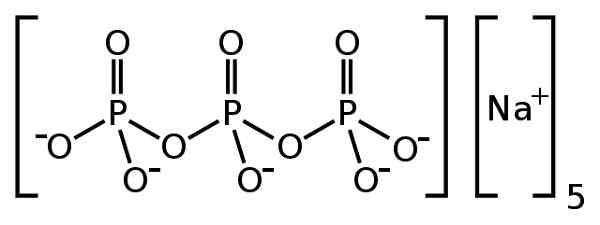
On Tripolifosforan sodu Jest to związek nieorganiczny utworzony przez pięć jonów sodu na+ oraz jon Prolifosforan P3ALBO105-. Jego formuła chemiczna to Na5P3ALBO10. Jon tripolifosforanowy zawiera trzy jednostki fosforanowe powiązane ze sobą i jest tak zwane skondensowany fosforan.
Anion trypolifosforanowy p3ALBO105- Ma zdolność do łapania jonów takich jak wapń CA2+ I Magnesio Mg2+, Dlatego Trypolif sodu.
 Tripolifosforan sodu5P3ALBO10. Benrr101 [domena publiczna]. Źródło: Wikimedia Commons.
Tripolifosforan sodu5P3ALBO10. Benrr101 [domena publiczna]. Źródło: Wikimedia Commons. Trypolifosforan sodu jest również stosowany jako źródło fosforu w karmieniu wypasanych zwierząt i w leczeniu niektórych dolegliwości innych rodzajów zwierząt. Służy również do zagęszczania i nadawania tekstury niektórym przetworzonym produktom, takim jak kremy, pudies i sery.
W przemyśle rolnym jest stosowany w nawozach w granulkach, aby zapobiec ich przyklejeniu się i może pozostać luźne.
Chociaż przeprowadzono dyskusje na temat wpływu na środowisko trupiolifosforanu sodu, który jest dodawany do detergentów, obecnie szacuje się, że nie przyczynia się to znacząco do uszkodzenia środowiska, przynajmniej przez detergenty.
[TOC]
Struktura chemiczna
Trypolifosforan sodu jest częścią skoczanych fosforanów skondensowanych, ponieważ są to kilka jednostek fosforanowych wraz ze sobą. W tym przypadku jon tripolifosforanowy jest liniowym fosforanem kondensatu, ponieważ ma liniową strukturę łańcucha, z wiązaniami fosforu-toksygen-fosfor (P-O-P) (P-O-P).
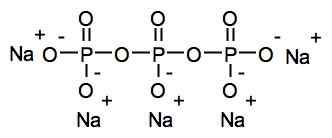 Struktura chemiczna tulolifosforanu sodu. Roland.Chem [gfdl (http: // www.gnu antylopa.Org/copyleft/fdl.html)]. Źródło: Wikimedia Commons.
Struktura chemiczna tulolifosforanu sodu. Roland.Chem [gfdl (http: // www.gnu antylopa.Org/copyleft/fdl.html)]. Źródło: Wikimedia Commons. Nomenklatura
- Tripolifosforan sodu
- Triphosforan sodu
- Triffosforan Pentasodio
- STPP (angielski akronim Tripolifan sodu)
Nieruchomości
Stan fizyczny
Krystaliczna biała stała.
Waga molekularna
367,86 g/mol.
Temperatura topnienia
622 ° C.
Gęstość
2,52 g/cm3
Rozpuszczalność
Rozpuszczalna w wodzie: 20 g/100 ml w 25 ° C i 86,5 g/100 ml w 100 ° C.
Może ci służyć: jakie są nieorganiczne funkcje chemiczne?Ph
1% roztwór trypolifosforanu sodu ma pH 9,7-9,8.
Właściwości chemiczne
Jest to agent porwania jonów, to znaczy może łapać jony i pozostać z nimi razem. Złożona forma z wieloma metali.
Jeśli roztwór trypolifosforanu sodu jest ogrzewany przez długi czas3PO4.
Inne właściwości
Jest lekko higroskopowy. Kształtować stabilne hydraty, to znaczy związki, które mają cząsteczki wody (bez reakcji z tym) wzoru na5P3ALBO10.NH2Lub gdzie n może być warte od 1 do 6.
Według niektórych źródeł ilość 20 mg tuszolifosforanu sodu w litrach wody nie wpływa na zapach, smak lub pH wspomnianej wody.
Uzyskanie
Trypolifosforan sodu jest wytwarzany przez odwodnienie ortofosforanów (takich jak monosodyczny fosforan NaH2PO4 I dis -fosfat na2HPO4) w bardzo wysokich temperaturach (300-1200 ° C):
Nie2PO4 + 2 na2HPO4 → na5P3ALBO10 + 2 godz2ALBO
Można go również uzyskać przez kontrolowane kalcynację (oznacza bardzo wysoką temperaturę ogrzewania) ortofosforanu sodu na3PO4 Z węglanem sodu na2WSPÓŁ3 i kwas fosforowy H3PO4.
Aplikacje
W detergentach
Trypolifosforan sodu ma właściwość tworzenia związków z niektórymi jonami, zachowując je. Ma również dyspergujące właściwości brudnych cząstek i utrzymuje je w zawieszeniu.
Z tego powodu jest szeroko stosowany w preparatach detergentu do łapania i unieruchomienia jonów wapnia Ca2+ i Magnesio Mg2+ wody (z twardych wód SO) i utrzymanie brudnego w wodzie zawieszonej.
Wspomniane jony zakłócają działanie czyszczące. Łapiąc je, Trypolifosforan zapobiega wytrącaniu się takich jonów wraz z środkiem czyszczącym lub przyklejającym się z brudnego tkaniny, uniemożliwiającym wystartowanie z tego plamy.
Mówi się w tym przypadku, że „trypolifosforan sodu„ zmiękcza ”wodę. Dlatego jest stosowany w detergentach do odzieży i automatycznych detergentów do zmywarki.
Może ci służyć: strzykawka PascalPonieważ tworzy stabilne hydracje, detergenty, które posiadają go w preparacie, można natychmiast wysuszyć przez spray (bardzo drobne rosa) tworzące suche proszki.
 Pył detergentowy, który może zawierać trypolifosforan sodu. Autor: Frank Habel. Źródło: Pixabay.
Pył detergentowy, który może zawierać trypolifosforan sodu. Autor: Frank Habel. Źródło: Pixabay. Do użytku weterynaryjnego
Trypolifosforan sodu jest stosowany jako suplement w roztworach płynnych jako źródło fosforu dla bydła.
 Pasze podciśnieniowe można uzupełnić truolifosforanem sodu jako źródło fosforu. Autor: Herney Gómez. Źródło: Pixabay.
Pasze podciśnieniowe można uzupełnić truolifosforanem sodu jako źródło fosforu. Autor: Herney Gómez. Źródło: Pixabay. Służy również do zapobiegania obliczeniom nerek u kotów, dla których zwierzęta te są dostarczane doustnie. Jednak należy zwrócić uwagę w dawce, ponieważ może to powodować biegunkę.
 Trypolifosforan sodu w bardzo niskich dawkach może zapobiegać nerkom u kotów. Autor: Scott Payne. Źródło: Pixabay.
Trypolifosforan sodu w bardzo niskich dawkach może zapobiegać nerkom u kotów. Autor: Scott Payne. Źródło: Pixabay. W medycynie
Trypolifosforan sodu został zastosowany w przygotowaniu nanocząstek do odpowiedniego transportu i uwalniania leków chemioterapii raka. Został również stosowany w nanocząstkach do leczenia infekcji grzybów w płucach.
 Tripolifosforan jest testowany w przygotowaniu nanofarmakali do leczenia infekcji grzybiczych w płucach. Autor: OpencLipart-Vectors. Źródło: Pixabay.
Tripolifosforan jest testowany w przygotowaniu nanofarmakali do leczenia infekcji grzybiczych w płucach. Autor: OpencLipart-Vectors. Źródło: Pixabay. W branży spożywczej
Jest stosowany w produktach mlecznych, takich jak podesy, bita śmietana, kwaśna śmietana i ser.
 Kwaśny Crector może zawierać tripolifing sodu, aby poprawić jego teksturę. Autor: Welikodub. Źródło: Pixabay.
Kwaśny Crector może zawierać tripolifing sodu, aby poprawić jego teksturę. Autor: Welikodub. Źródło: Pixabay. W innych pokarmach jest używany jako porywacz jonów, aby nadać teksturę, jako zagęszczacz i konserwant.
Inne zastosowania
- Jako stabilizator nadtlenków
- W płynach wiertniczych olejowych działa jako emulgator i dyspergator, aby kontrolować lepkość błota.
Może ci służyć: metale żelazne- W rolnictwie jest ono stosowane jako środek przeciwdziałający niektórym nawozom lub produktom rolnym, oznacza to, że zapobiega ich przyleganiu do siebie, a nawóz można łatwo rozpowszechniać. Jest również stosowany w formułach pestycydowych stosowanych do uprawy upraw.
 Fabryka nawozów. Czasami Trypolif sodu sodu. Van Twin [CC BY-SA 3.0 (https: // creativeCommons.Org/licencje/by-sa/3.0)]. Źródło: Wikimedia Commons.
Fabryka nawozów. Czasami Trypolif sodu sodu. Van Twin [CC BY-SA 3.0 (https: // creativeCommons.Org/licencje/by-sa/3.0)]. Źródło: Wikimedia Commons. Wpływ środowiska
Zastosowanie produktów z fosforanami zostało zidentyfikowane jako jeden z uczestników eutrofizacji wód na planecie.
Eutrofizacja jest przesadnym i przyspieszonym wzrostem glonów i gatunków roślin wodnych, które prowadzą do silnego spadku tlenu dostępnego w wodzie, co prowadzi do zniszczenia do dotkniętego ekosystemu (śmierć większości gatunków zwierząt w nim).
 Eutrofication to przesadny wzrost glonów w jeziorze, rzece lub morzu. F. Lamiot (własna praca) [CC BY-SA 2.5 (https: // creativeCommons.ORG/Licencje/BY-SA/2.5)]. Źródło: Wikimedia Commons.
Eutrofication to przesadny wzrost glonów w jeziorze, rzece lub morzu. F. Lamiot (własna praca) [CC BY-SA 2.5 (https: // creativeCommons.ORG/Licencje/BY-SA/2.5)]. Źródło: Wikimedia Commons. W latach 80. XX wieku pojawiły się kontrowersje, że zastosowanie trypolifosforanu sodu w detergentach przyczyniło się do eutrofizacji.
W dzisiejszych czasach wiadomo, że ograniczenie stosowania detergentów z Trypolifem sodu.
W rzeczywistości istnieją kraje, które uważają za trupiefosforan sodu za przyjazny dla środowiska element detergentów i promują ich użycie.
Ryzyko
Trypolifosforan sodu to drażniący skóra i oczy. Kontakt wzrokowy może powodować uszkodzenie tego. Przedłużony kontakt skóry może wytwarzać zapalenie skóry.
Jeśli zostanie spożywany w dużych ilościach, może to powodować nudności, wymioty i biegunkę, generując również poważne zmniejszenie jonu wapnia we krwi. U zwierząt spowodowało spadek wapnia w kościach.
Jest uważany za bezpieczny związek, ilekroć standardy produkcyjne produktu, w którym jest stosowany.
Bibliografia
- Liu i. I Chen, J. (2014). Cykl fosforu. Moduł referencyjny w systemach ziemskich i nauk o środowisku. Encyklopedia ekologii (wydanie drugie). Tom. 4, 2014, pp.181-191. Odzyskane z naukowym.com
- LUB.S. National Library of Medicine. (2019). Tripolifan sodu. National Center for Biotechnology Information. Odzyskane z Pubchem.NCBI.NLM.Nih.Gov.
- Mukherjee, ur. i in. (2017). Podawanie płuc biodegradowalnych nanonośników leków w celu bardziej efektywnego leczenia zakażeń grzybiczych w płucach: spostrzeżenia oparte na najnowszych ustaleniach. W systemach wielofunkcyjnych do łącznego dostarczania, bioczujania i diagnostyki. Odzyskane z naukowym.com.
- Kirk-Othmer. (1991). Encyklopedia technologii chemicznej. 4th Nowy Jork, John Wiley i synowie.
- Burckett st. Laurent, J. i in. (2007). Czyszczenie prania tekstyliów. W Podręczniku do czyszczenia/odkażania powierzchni. Odzyskane z naukowym.com.
- Budavari, s. (Redaktor). (1996). Indeks Merck. NJ: Merck and Co., Inc.
- Salahuddin, n. i Galal, aby. (2017). Poprawa dostarczania leków chemioterapii przez narzędzia nanoprecyzyjne. W nanrukturach do terapii przeciwnowotworowej. Odzyskane z naukowym.com.
- « Struktura szczawianu sodu (Na2C2O4), właściwości, zastosowania, ryzyko
- Właściwości cyjanku potasu (KCN), zastosowania, struktury, ryzyko, »

