Azotan magnezu (Mg (NO3) 2) Struktura, właściwości, wykorzystuje

- 1192
- 143
- Eugenia Czapla
On Azotan magnezu Jest to nieorganiczna substancja stała, której wzór chemiczny wynosi mg (nie3)2. Jest to związek jonowy utworzony przez połączenie kationu magnezu Mag2+ i dwa aniony azotanowe3-.
MG (nie3)2 Jest to krystaliczna biała stała. Jest bardzo higroskopijny, to znaczy łatwo pochłania wodę z środowiska. Pozostając w kontakcie z powietrzem środowiska, ma tendencję do tworzenia sześciokadru MG (nie3)2 •6h2ALBO.
 Azotan magnezu Mg (nie3)2 Sproszkowany. Ondřej Mang [domena publiczna]. Źródło: Wikimedia Commons.
Azotan magnezu Mg (nie3)2 Sproszkowany. Ondřej Mang [domena publiczna]. Źródło: Wikimedia Commons. Azotan magazynowy (nie3)2 •6h2O ma w strukturze krystalicznej 6 cząsteczek wody h2Lub dla każdej cząsteczki Mg (nie3)2. Azotan magnezu występuje w jaskini i kopalniach w postaci minerału nitromagnesytu.
MG (nie3)2 Uzyskuje się go w handlu przez reakcję metalu MG z kwasem azotowym HNO3.
Ma bardzo zróżnicowane zastosowania, takie jak rolnictwo, jak nawóz, ponieważ zapewnia pożywne elementy dla roślin takich jak azot (N) i magnez (MG).
Jest stosowany w branży fajerwerków lub pirotechniki, a także do uzyskania skoncentrowanego kwasu azotowego. Jest stosowany w analizie chemicznej, w eksperymentach fizycznych oraz w badaniach medycznych i naukowych.
[TOC]
Struktura
Azhydro azotan magnezu powstaje w wyniku kationu magnezio mg2+ i dwa aniony azotanowe3-.
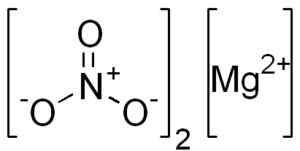 Struktura MG (nie3)2. Edgar181 [domena publiczna]. Źródło: Wikimedia Commons.
Struktura MG (nie3)2. Edgar181 [domena publiczna]. Źródło: Wikimedia Commons. Jon Magnesio mg2+ Ma konfigurację elektroniczną: 1s2, 2s2 2 p6, 3s0, Cóż, dały dwa elektrony zewnętrznej warstwy (3s). Ta konformacja jest bardzo stabilna.
Jon nr3- Ma płaską i symetryczną strukturę.
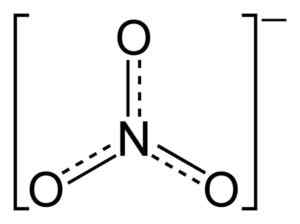 Struktura jonów płaskich azotanów nr3-. Kropkowane linie wskazują sprawiedliwy rozkład elektronów między trzema wiązaniami N-O. Benjah-BMM27 [domena publiczna]. Źródło: Wikimedia Commons.
Struktura jonów płaskich azotanów nr3-. Kropkowane linie wskazują sprawiedliwy rozkład elektronów między trzema wiązaniami N-O. Benjah-BMM27 [domena publiczna]. Źródło: Wikimedia Commons. W strukturze NO3- Obciążenie ujemne jest stale rozmieszczone między trzema atomami tlenu.
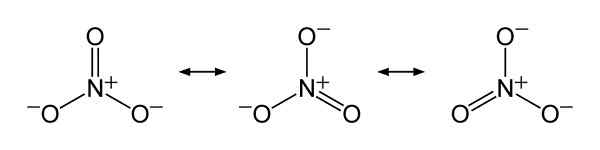 Struktury rezonansu jonów azotanowych3-, Wyjaśnić sprawiedliwy rozkład obciążenia ujemnego między trzema atomami tlenu. Benjah-BMM27 [domena publiczna]. Źródło: Wikimedia Commons.
Struktury rezonansu jonów azotanowych3-, Wyjaśnić sprawiedliwy rozkład obciążenia ujemnego między trzema atomami tlenu. Benjah-BMM27 [domena publiczna]. Źródło: Wikimedia Commons. Nomenklatura
-Azotan anhydro magnezu: mg (no3)2
Może ci służyć: woda destylowana-Dihydrated Magnesium Aztran: Mg (NO3)2 •2h2ALBO
-Azotan magnezu heksahydrata: MG (nie3)2 •6h2ALBO
-Dinitate magnezu
Nieruchomości
Stan fizyczny
-Mg (nie3)2 Bezhodny: białe stałe, sześcienne kryształy.
-Mg (nie3)2 Dihydrado: krystaliczne białe ciało stałe.
-Mg (nie3)2 Heksahided: bezbarwne solidne, monokliniczne kryształy
Waga molekularna
-Mg (nie3)2 Bezwodny: 148,31 g/mol
-Mg (nie3)2 Heksahydrat: 256,41 g/mol
Temperatura topnienia
-Mg (nie3)2 Heksahydrat: 88,9 ºC
Punkt wrzenia
-Mg (nie3)2 Heksahydrat: Nie gotuj, rozkładaj w 330 ° C
Gęstość
-Mg (nie3)2 Bezwodne: 2,32 g/cm3
-Mg (nie3)2 Dihydrain: 1456 g/cm3
-Mg (nie3)2 Heksahydrat: 1464 g/cm3
Rozpuszczalność
Azhydro azotan magnezu jest bardzo rozpuszczalny w wodzie: 62,1 g/100 ml w 0 ° C; 69,5 g/100 ml w 20 ° C. Jest to również bardzo higroskopijne, kontakt z powietrzem szybko tworzy heksahydrat.
MG (nie3)2 Dihydrado jest również bardzo rozpuszczalny w wodzie i etanolu. Jest higroskopowy.
MG (nie3)2 Heksahydrat jest również bardzo rozpuszczalny w wodzie. Jest umiarkowanie rozpuszczalny w etanolu. Jest to najbardziej stabilny z trzech kontaktów z powietrzem, to znaczy z trzech.
Efekt ogrzewania
Przesyłając wodny roztwór MG (nie3)2 Aby odparować wodę, sól, która krystalizuje się, to sześciokadrat: mg (nie3)2 •6h2ALBO. Heksahydrat oznacza, że w stałej każdej cząsteczki Mg (nie3)2 Jest powiązany z 6 cząsteczkami wody.
Istnieje również mg dihydrat (nie3)2 •2h2Lub, w którym MG (nie3)2 Stolizna jest przymocowana do 2 cząsteczek wody.
Ogrzewanie mg heksahydrat (nie3)2 •6h2Lub sól anhydra nie jest uzyskiwana, ponieważ azotan magnezu ma wysokie powinowactwo do wody.
Z tego powodu, ogrzewając go powyżej temperatury topnienia, mieszaną sól azotanu i wodorotlenku magnezu MG (nie3)2 •4mg (OH)2.
Ta mieszana sól, gdy osiągnie 400 °.
Może ci służyć: podchloryn wapnia (CA (CLO) 2)Uzyskanie
Można go przygotować przez reakcję węglanu magnezu MGCO3 Z kwasem azotowym HNO3, Rezygnowanie z dwutlenku węgla Co2:
MGCO3 + 2 HNO3 → Mg (nie3)2 + WSPÓŁ2↑ + H2ALBO
Można go również uzyskać za pomocą wodorotlenku magnezu Mg (OH)2 i kwas azotowy:
Mg (OH)2 + 2 HNO3 → Mg (nie3)2 + 2 godz2ALBO
Uzyskane na rynku na kilka sposobów:
1- Reagowanie magnesio mg z kwasem azotowym HNO3.
2- Według reakcji tlenku magnezu MGO z kwasem azotowym HNO3.
3- Dołączanie do Mg (OH) wodorotlenek magnezu2 i azotan amonu NH4NIE3, tworzenie azotanu magnezu z odłączeniem amoniaku NH3.
Lokalizacja w naturze
MG (nie3)2 Heksahydrat znajduje się naturalnie w kopalniach i jaskiniach lub jaskini w postaci minerału nitromagnesytu.
Ten minerał jest obecny, gdy Guano kontaktuje się z bogatymi skałami na magnezie. Guano jest materiałem wynikającym z wydalania ptaków morskich i fok w bardzo suchych środowiskach.
Aplikacje
MG (nie3)2 Heksahydrat jest stosowany w przemyśle ceramicznym, chemii i rolnictwa.
Związek ten jest nawozem, ponieważ zapewnia azot (N), który jest jednym z trzech podstawowych elementów wymaganych przez rośliny, i magnezu (mg), który jest również elementem wtórnym również dla nich ważnym dla tych.
W ten sposób jest stosowany z innymi składnikami w szklarniach i hydroponicznej hodowli. To ostatnie ma uprawiać rośliny w wodnym roztworze z solami nawozowymi zamiast gleby.
 Hydroponiczna kultura. Możesz zobaczyć kanały, przez które roztwór wodny z solami nawozowymi, takimi jak mg azotan magnezu3)2. Autor: Marsraw. Źródło: Pixabay.
Hydroponiczna kultura. Możesz zobaczyć kanały, przez które roztwór wodny z solami nawozowymi, takimi jak mg azotan magnezu3)2. Autor: Marsraw. Źródło: Pixabay. Jest również stosowany jako katalizator w uzyskiwaniu związków petrochemicznych. Pozwala dostosować lepkość w niektórych procesach. Azotan anhydro magnezu jest stosowany w pirotechnikach, to znaczy do produkcji fajerwerków.
 Fajerwerki zawierają azotan magnezu (nie3)2. Autor: Free-Goos. Źródło: Pixabay.
Fajerwerki zawierają azotan magnezu (nie3)2. Autor: Free-Goos. Źródło: Pixabay. Azhydro azotan magnezu jest środkiem odwodnionym. Jest używany na przykład do uzyskania skoncentrowanego kwasu azotowego, ponieważ eliminuje wodę i koncentruje opary kwasowe do 90-95% HNO3.
Może ci służyć: reguła przekątna Stężony kwas azotowy. Oryginalny przesyłanie był fabularny we włoskiej Wikipedii. [Gfdl (http: // www.gnu antylopa.Org/copyleft/fdl.html)]. Źródło: Wikimedia Commons.
Stężony kwas azotowy. Oryginalny przesyłanie był fabularny we włoskiej Wikipedii. [Gfdl (http: // www.gnu antylopa.Org/copyleft/fdl.html)]. Źródło: Wikimedia Commons. Służy również do pokrycia azotanu amonu i umożliwienia tworzenia perłów takiego sprężonego materiału.
Ma narzędzia w preparatach ITK, toner (czarny proszek używany w systemach fotokopowych) i produkty do kolorowania. Służy jako standard magnezu w chemii analitycznej.
Sól azotanowa magnezu i cerio mg (nie3)2 •Zmarszczyć brwi3)3 Interesuje to eksperymenty fizyki w niskich temperaturach, ponieważ jest stosowane jako czynnik chłodniczy w eksperymentach sumagnetyzacji adiabatycznej (bez przeniesienia ciepła).
Ta sól magnezu i cerio została zastosowana do ustalenia bardzo niskich poziomów temperatur skali Kelvina (blisko bezwzględnego zera).
W ostatnich badaniach
Kilku badaczy użyło MG (nie3)2 W kompozycjach z syntetycznymi i naturalnymi polimerami w celu zwiększenia przewodności w akumulatorach magnesio.
Został również zbadany w budowie superkaugadów w celu magazynowania energii o dużej mocy.
W badaniach chorób
Azotan magnezu podano szczurom laboratoryjnym z nadciśnieniem tętniczym (wysokie ciśnienie) i stwierdzono, że ciśnienie krwi skutecznie zmniejsza i osłabia lub zmiękcza skutki powikłań tej choroby.
Wykazał również działanie ochronne przed zaburzeniami neurologicznymi (zaburzeniem neuronów) i na śmierć u szczurów podczas procesów kaktonowania tętnicy szyjnej.
Bibliografia
- Qian, m. i in. (2018). Ekstrainarne porowate węglowodory o wysokiej pojemności z Pechini spalania żelu azotanowego magnezu. ACS Appl Mater Interfaces 2018, 10 (1): 381-388. NCBI odzyskało.NLM.Nih.Gov.
- Manjuladevi, r. i in. (2018). Badanie na temat elektrolitu polimerowego mieszania opartego na poli. Ionics (2018) 24: 3493. Link odzyskał.Skoczek.com.
- Kiruthika, s. i in. (2019). Ekologiczny elektrolit biopolimerowy, pektyna z azotanem magnezu, do zastosowania w urządzeniach elektochemicznych. J Solid State Electochem (2019) 23: 2181. Link odzyskał.Skoczek.com.
- Vilskerts r. i in. (2014). Azotan magnezu osłabia wzrost ciśnienia krwi u szczurów SHR. Magnes Res 2014, 27 (1): 16-24. NCBI odzyskało.NLM.Nih.Gov.
- Kuzenkov v.S. i Krushinskii a.L. (2014). Ochronne działanie azotanu magnezu na zaburzenia neurologiczne wywołane przez niedokrwienie mózgu u szczurów. Bull Exp Biol Med 2014, 157 (6): 721-3. NCBI odzyskało.NLM.Nih.Gov.
- Ropp, r.C. (2013). Grupa 15 (N, P, AS, SB i BI) Związki Ziemi alkalicznej. Azotan magnezu. W encyklopedii alkalicznych związków Ziemi. Odzyskane z naukowym.com.
- Kirk-Othmer (1994). Encyklopedia technologii chemicznej. Tom 1. Czwarta edycja. John Wiley & Sons.
- LUB.S. National Library of Medicine. (2019). Azotan magnezu. Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov.
- « Koncepcja i cechy systemu technicznego, elementy, przykłady
- Numer masowy, z czego składa się i jak go zdobyć (z przykładami) »

