Boyle Law
- 2622
- 221
- Maksymilian Kępa
Jakie jest prawo Boyle'a?
prawo Prawo Boyle lub Boyle-Maleotte Jest to taki, który wyraża związek między ciśnieniem wywieranym przez gaz lub na gaz, a objętością, którą to zajmuje; Ciągle zachowując zarówno temperaturę gazu, jak i jego ilość (liczba moli).
To prawo, wraz z prawem Charlesa, Gay-Lussaca, Charlesa i Avogadro, opisuje zachowanie idealnego gazu; w szczególności w zamkniętym pojemniku podlegającym zmianom objętości wywieranym przez siłę mechaniczną.
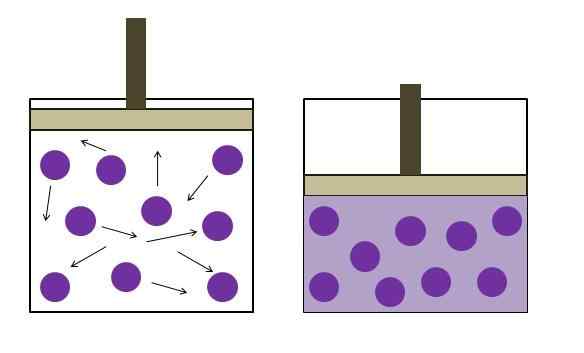
 Zwiększone ciśnienie redukcji ciśnienia. Źródło: Gabriel Bolívar
Zwiększone ciśnienie redukcji ciśnienia. Źródło: Gabriel Bolívar Górny obraz krótko podsumowuje prawo Boyle'a. Purple punkty reprezentują cząsteczki lub atomy gazowe, które zderzają się z wewnętrznymi ścianami pojemnika (po lewej). Zmniejszając dostępną przestrzeń lub objętość pojemnika zajmowanego przez ten gaz, kolizje są zwiększone, co przekłada się na wzrost ciśnienia (po prawej).
To pokazuje, że ciśnienie p i objętości V gazu jest odwrotnie proporcjonalne, jeśli pojemnik jest szczelnie zamknięty; W przeciwnym razie większe ciśnienie byłoby równe większemu rozszerzeniu pojemnika.
Jeśli wykres V przeciw P, z danymi V i P na osiach i i X, zostanie zaobserwowany, zaobserwowanoby krzywą asymptotyczną. Im niższy V, tym większy wzrost P; To znaczy krzywa rozciąga się na wysokie wartości p na osi x.
Oczywiście temperatura pozostaje stała; Ale gdyby ten sam eksperyment został przeprowadzony w różnych temperaturach, względne pozycje tych krzywych V vs P zmieniłyby się na osi kartezja. Zmiana byłaby jeszcze bardziej widoczna, gdyby były wykresy na osi trzywymiarowej, ze stałą t na osi Z.
Historia prawa Boyle
Tło
Ponieważ naukowiec Galileo Galilei wyraził swoją wiarę w istnienie pustki (1638), naukowcy zaczęli badać właściwości luk powietrznych i częściowych.
Chemik angloawolowy, Robert Boyle, rozpoczął studia nad nieruchomościami powietrznymi w 1638 r. Po dowiedzeniu się, że Otto von Gulericke, niemiecki inżynier i inżynier fizyczny, zbudował bombę powietrzną.
Może ci służyć: brom: historia, struktura, konfiguracja elektroniczna, właściwości, użyciaEksperyment rtęci
Aby przeprowadzić badania nad ciśnieniem powietrza, Boyle użył rurki „J”, której konstrukcję przypisano Robertowi Hookeowi, asystentowi Boyle. Krótkie koniec ramienia zostało zapieczętowane, a długi koniec rurki był otwarty, aby umieścić rtęć.
Od samego początku Boyle chciał zbadać elastyczność powietrza, jakościowo i ilościowo. Kiedy rtęć przelała się przez otwarty koniec rurki w postaci „J”, Boyle wydedukował, że powietrze w krótkim ramieniu rurki zostało zakontraktowane pod ciśnieniem rtęci.
Wyniki
Im większa ilość rtęci dodana do rurki, tym większe ciśnienie wywierane na powietrze i tym niższa jego objętość. Boyle uzyskał ujemną wykładniczą tabelę objętości powietrza w zależności od ciśnienia.
Tymczasem, jeśli wykreślono objętość powietrza w stosunku do odwrotnego ciśnienia, istnieje prosta linia dodatnich nachyleń.
W 1662 r. Boyle opublikował pierwsze prawo fizyczne, które zostało podane w postaci równania, które wskazywało na funkcjonalną zależność dwóch zmiennych. W tym przypadku ciśnienie i objętość.
Boyle powiedział, że istniała odwrotna zależność między ciśnieniem wywieranym na gaz a objętością zajmującą ten gaz, ten stosunkowo prawdziwy związek dla prawdziwych gazów. Większość gazów zachowuje się jak gazy idealne do umiarkowanych ciśnień i temperatur.
Kiedy występują wyższe ciśnienia i niższe temperatury, odchylenia od zachowania prawdziwych gazów ideałów stały się bardziej godne uwagi.
Edme Mariotte
Francuski fizyk Edme Mariotte (1620-1684) niezależnie odkrył to samo prawo w 1679 r. Ale miał zalety pokazania, że objętość zmienia się w zależności od temperatury. Dlatego nazywa się to prawem lub prawem Mariotte lub prawa Boyle i Mariotte.
Wzmocnienie prawa
Daniel Bernoulli (1737) wzmocnił prawo Boyle'a, wskazując, że ciśnienie gazu wytwarzane jest przez uderzenia cząstek gazu na ścianach zawierającego go pojemnika.
Może ci służyć: nukleofil: atak nukleofilowy, typy, przykłady, nukleofilnośćW 1845 r. John Waterston opublikował artykuł naukowy, który koncentruje się na głównych zasadach kinetycznej teorii gazów.
Następnie Rudolf Clausius, James Maxwell i Ludqwig Boltzmann umocnili kinetyczną teorię gazów, która wiąże ciśnienie wywierane przez gaz z prędkością cząstek gazu w ruchu w ruchu w ruchu ruchu w ruchu ruchu ruchu.
Im niższa objętość pojemnika zawierającego gaz, tym większa częstotliwość uderzeń cząstek, które tworzą go na ścianach pojemnika; A zatem im większe ciśnienie wywierane przez gaz.
Co to za prawo?
Eksperymenty przeprowadzone przez Boyle'a wskazują, że istnieje odwrotna zależność między objętością zajmowaną przez gaz a ciśnieniem wywieranym na niego. Jednak wspomniana relacja nie jest całkowicie liniowa, na co wskazuje wykres zmienności objętościowej zgodnie z ciśnieniem przypisanym Boyle.
Zgodnie z prawem Boyle wskazano, że objętość zajmowana przez gaz jest odwrotnie proporcjonalny do ciśnienia. Wskazuje się również, że iloczyn ciśnienia gazu według jego objętości jest stały.
Wyrażenie matematyczne
Aby dostać się do matematycznego wyrazu prawa Boyle'a, zaczyna się od:
V ∝ 1/p
Gdzie wskazuje, że objętość zajmowana przez gaz jest odwrotnie proporcjonalny do jego ciśnienia. Istnieje jednak stała, która decyduje o tym, jak odwrotnie proporcjonalny jest ten związek.
V = k/p
Gdzie k jest stałą proporcjonalności. Oczyszczanie k masz:
VP = k
Produkt ciśnienia gazu według jego objętości jest stały. Więc:
V1P1 = K i v2P2 = k
I można to wywnioskować, że:
V1P1 = V2P2
To ostatnie jest wyrażeniem lub ostatecznym równaniem prawa Boyle'a.
Po co to jest? Jakie problemy rozwiązuje prawo Boyle'a?
Silniki parowe
Prawo Boyle-Maleotte jest stosowane w działaniu maszyn parowych. Jest to zewnętrzny silnik spalania, który wykorzystuje transformację energii cieplnej ilości wody w energię mechaniczną.
Woda jest podgrzewana w szczelnie zamkniętym kotle, a wytwarzana przez parę ciśnienie zgodnie z prawem Boyle, które wytwarza rozszerzenie objętości cylindra, pchając tłok.
Może ci służyć: współczynnik rozcieńczeniaLiniowy ruch tłoka przekształca się w ruch obrotowy, stosując system korb i korby, który może napędzać koła lokomotywy lub wirnik generatora elektrycznego.
Popij napoje
Działanie aspirowania sody lub soku z butelki przez plastikową rurkę jest związane z prawem Boyle'a. Gdy sugerowane jest powietrze rurki za pomocą ust, następuje spadek ciśnienia wewnątrz rurki.
Ten spadek ciśnienia ułatwia rosnący ruch płynu w rurce, umożliwiając jego spożycie. Ta sama zasada działa w ekstrakcji krwi za pomocą strzykawki.
Układ oddechowy
Prawo Boyle'a jest ściśle związane z funkcjonowaniem układu oddechowego. Podczas fazy inspiracji występuje skurcz przepony i innych mięśni; Na przykład zewnętrzne interkostały, które wytwarzają rozszerzenie klatki piersiowej.
Powoduje to spadek ciśnienia wewnątrzprzewodnikowego, powodując rozszerzenie płucne, które powoduje wzrost objętości płuc. Dlatego ciśnienie wewnątrzustno -oddechowe zmniejsza się w zależności od tego, co jest podniesione w prawie Boyle.
Stając się subatose ciśnienie wewnątrzustonowe, powietrze atmosferyczne przepływa do płuc, co powoduje wzrost ciśnienia w płucach; Dopasowując w ten sposób presję do ciśnienia atmosferycznego i kończąc fazę inspiracji.
Następnie mięśnie wdechowe rozluźniają się, a mięśnie wydechowe kurczą się. Ponadto powstaje elastyczne wycofanie płuc, zjawisko, które powoduje spadek objętości płuc, z konsekwencją wzrostu ciśnienia wewnątrzustonowego, wyjaśniającego prawem Boyle'a przez Boyle'a.
Poprzez zwiększanie ciśnienia wewnątrzustonowego i stając się większym niż ciśnienie atmosferyczne, powietrze płynie wewnątrz płuc do atmosfery. Dzieje się tak do momentu równego ciśnienia, co kończy fazę ważności.
Bibliografia
- Prawo Boyle'a. Encyclopædia Britannica. Odzyskane z: Britannica.com
- Formuła prawa Boyle'a. Odzyskane z: Thoughtco.com

