Charakterystyka izomaltu, struktura, funkcje
- 4714
- 717
- Herbert Wróblewski
Izomaltoza (6-ALBO-α-D-glukopiranozylo-glukopiranozy) jest królewskim disacharydem maltozy (inny disaccharrid.
Jak sama nazwa wskazuje, jest to disacharyd. Etymologicznie, prefiks "ISO " Od słowa izomaltozowego odnosi się do „tego samego” do maltozy.
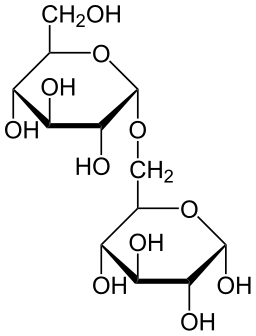
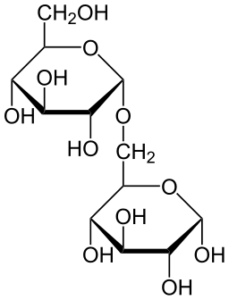 Reprezentacja Haworth dla izomaltozy (Źródło: Neurotoger [domena publiczna] za pośrednictwem Wikimedia Commons)
Reprezentacja Haworth dla izomaltozy (Źródło: Neurotoger [domena publiczna] za pośrednictwem Wikimedia Commons) Ten disacharyd został odkryty na początku 1960 roku, a jego synteza przemysłowa została po raz pierwszy osiągnięta w 1980 roku. Jednak nie został zatwierdzony dopiero w 1900 r. Do konsumpcji ludzi.
Znany również jako izogentobioous, izomaltoza jest disacharydem uważanym za niekynogeniczną zastępcę sacharozy u niektórych produktów sformułowanych u pacjentów z cukrzycą lub przedporodem.
Podczas trawienia skrobi izomalt i wiele oligosacharydów izomaltozowych są wytwarzane przez hydrolizę za pośrednictwem różnych rodzajów enzymów, zwłaszcza α-amylaz i α-glukozydazy.
Ten disacharyd jest głównym składnikiem oligosacharydów izomaltozy, znanych również jako IMO, które są naturalnie wytwarzane w sfermentowanych posiłkach, takich jak sos sojowy i sake.
[TOC]
Charakterystyka
Izomal jest disacharydem sklasyfikowanym w grupie redukujących disacharydów, w połączeniu z laktozą, celobious i maltozą. W przypadku hydrolizy podlega jej składowe monosacharydy dwie cząsteczki glukozy.
W komórkach pędzla jelita ssaków izomalt jest pre-Digerida lub hydrolizowany przez enzym disacaridazy związany z błoną plazmatyczną tego samego znanego jak izomaltaza cukru-izomaltaza.
Może ci służyć: Miller i Urey ExperimentTen disacharyd jest wytwarzany przemysłowo z sacharozy, poprzez katalityczne zmniejszenie obecności ogrzewania niklu lub glukozy (więc jest obecny w różnych typach syropów).
Izomaltoza i izomaltuloza
Istnieje inny disacharyd podobny do izomaltazy znanej jako izomaltuloza, ale różnica między nimi ma związek z disacharydem, z którego pochodzą, ponieważ izomer jest izomerem pochodzącym z maltozy i izomaltuli.
Izomaltuloza jest w rzeczywistości disacharydem glukozy i fruktozy, które są ze sobą powiązane przez glikozydowe wiązanie typu α-1,6 (ten sam typ łącza, który łączy odpady glukozy w izomalcie).
Ten disacharyd jest szeroko stosowany w przemyśle spożywczym i jest uzyskiwany sztucznie z sacharozy i przez enzymatyczne działanie syntazy syntezalulozowej, która powoduje strukturalne zlewni między monosacharydami, które go tworzą.
Struktura
Jak już wspomniano, izomaltoza jest izomerem maltozowym, więc składa się z dwóch cząsteczek glukozy.
Jego składowe monosacharydy są ze sobą zjednoczone poprzez glukozydyczne powiązania typu α-1,6, które różnica od maltozy, której łącze wynosi typ α-1,4.
Ten rodzaj łącza znacznie zwiększa elastyczność cząsteczki i zapewnia większe możliwości konformacyjne niż inne.
Dzięki obecności łącza typu α-1,6 izomalt w roztworze nie jest krystalizowany tak łatwo, jak inne disacharydy, jego komercyjna prezentacja ma postać krystalicznego pyłu.
Jego ogólny wzór chemiczny to C12H22O11. Ma masę cząsteczkową 342.3 g/mol i jest również znany jako α-D-glukopiranozylo-glukopiraniczny. Jego temperatura topnienia wynosi od 98 do 160 ° C, jest rozpuszczalna w wodzie i należąc do grupy cukrów fermentacyjnych.
Może ci służyć: acetylocholinesteraza: struktura, funkcje i inhibitoryFunkcje
Chociaż nie jest to tak łatwo strawne, izomalt, jako produkt uboczny enzymatycznej degradacji skrobi, jest to niezbędny disacharyd dla odżywiania ssaków.
Jego hydroliza, za pośrednictwem enzymu obecnego w błonie krawędzi pędzla zwanego tkanką cukrową-izomaltazą, jest źródłem węgla i energii, ponieważ glukozę można łatwo przetransportować do cytosolu i skierować się na podstawowe trasy kataboliczne.
W formie Aspergillus nidulans, Izomaltoza jest jednym z najskuteczniejszych induktorów w indukcji syntezy enzymu amylausowego, która ma ważne implikacje w biologii tego mikroorganizmu.
Zastosowania przemysłowe
Główne źródło izomaltu nie jest naturalne, ponieważ jest to uzyskiwane przemysłowo z bogatych syropów w maltozie dzięki działaniu enzymu transglukozydazy.
Innym enzymem bakteryjnym stosowanym biotechnologicznie do produkcji izomaltazy jest izomeraza sacharozy.
W ten sposób wyprodukowany izomal jest włączony do wielu jadalnych preparatów jako słodzik wśród nich, wśród których są słodycze, czekoladki lub cukierki i niektóre pokarmy w puszkach. Ponadto jest stosowany jako konserwujący żywność, taki jak płatki zbożowe, ciasteczka i pieczywo.
Jest stosowany z substytutem sacharozy dla pacjentów z cukrzycą, ponieważ nie jest tak strawny jako powszechny cukier, a zatem nie zwiększa znacząco poziomu glukozy we krwi (zapewnia również niższą zawartość kalorii).
W przypadku swoich jadalnych zastosowań należy ogólnie mieszać z innymi cukrami, ponieważ nie ma takich samych właściwości, co wspólny cukier (nie karmelizuje się podczas ogrzewania i nie można go używać do pieczonych preparatów).
Ponieważ jego preparaty mają jaśniejszy i bardziej przezroczysty wygląd, izomalt jest powszechnie stosowany do dekoracyjnych celów gastronomicznych.
Może ci służyć: Bioelements: klasyfikacja (podstawowa i wtórna)Ma również zastosowania w branży farmaceutycznej i kosmetycznej. Ponadto jest ważny dla preparatów żywnościowych zaprojektowanych przez zwierzęta domowe lub hodowlane.
Powiązane choroby
Istnieje wrodzona choroba autosomalna u ludzi znana jako niedobór zamieszania wobec zamieszkania lub CSID (angielski Wrodzona niedobór Lindy-Isomaltaza), który jest związany z defektami w trawieniu oligosacharydów i osmotycznie aktywnych disacharydów.
Ustalono, że choroba ta ma związek z różnymi jednoczesnymi czynnikami, w tym mutacje genów enzymów zaangażowanych w proces, takie jak izomaltaza zamiennika.
Niedolą disacharydów, takich jak sacharoza i izomaltaza, wytwarza jej „nietolerancję”. Stan patologiczny charakteryzuje się rozwojem skurczów brzucha, biegunki, wymiotów, jajków, hipoglikemii, nadmiernej produkcji gazów itp.
Bibliografia
- Badui, s. (2006). Chemia gastronomiczna. (I. Quintanar, wyd.) (Czwarty ed.). Meksyk d.F.: Edukacja Pearsona.
- Finch, str. (1999). Węglowodany: struktury, synteza i dynamika. Londyn, Wielka Brytania: Springer-Science+Business Media, b.V.
- Kato, n., Murakoshi i., Kato, m., Kobayashi, t., & Tsukagoshi, n. (2002). Izomaltoza utworzona przez α-glukosidaes wyzwala indukcję amylazy w Aspergillus nidulans. Obecna genetyka, 42(1), 43-50.
- Pubchem. (2005). Pobrano 6 sierpnia 2019 r. Z WWW.Pubchem.NCBI.NLM.Nih.Gov
- Stick, r. (2001). Węglowodany. Słodkie cząsteczki życia. Academic Press.
- Stick, r., & Williams, s. (2009). Węglowodany: niezbędne cząsteczki życia (2 wyd.). Elsevier.
- TreM, w. (1995). Wrodzona niedobór Lindy-Isomaltaza. Journal of Pediatric Gastroenterology and Nutrition, dwadzieścia jeden, 1-14.
- « Normalne obliczenia i przykładowy wektor
- Poziome funkcje strzelania, formuły i równania, ćwiczenia »

