Niesamowici
- 2819
- 379
- Arkady Sawicki
Co jest niesamowite?
Niesamowici Są to hormony żołądkowo -jelitowe, które stymulują wydzielanie stężeń fizjologicznych insuliny. Termin ten jest obecnie używany w odniesieniu do dwóch różnych hormonów jelitowych, które mają różne nazwy techniczne: GIP lub „zależne od glukozy polipeptyd insulinotropowy” i GLP-1 lub „peptyd glukagonu typu 1”.
„Insilein” to słowo i koncepcja wymyślona w 1932 r. Przez fizjologa belgijskiego Jeana La Barre, który wprowadził je w celu zdefiniowania czynników hormonalnych jelitowych, które uzupełniają wpływ wydzielający wydzielanie endokrynologiczne.
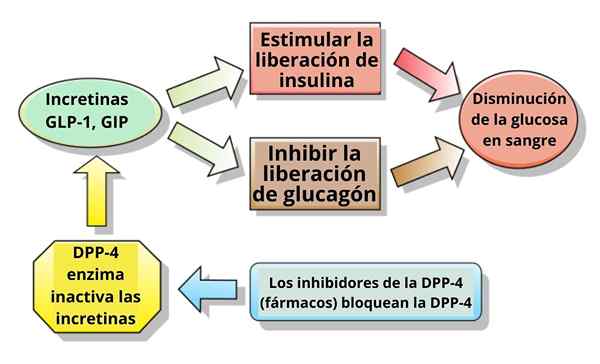
 Schemat mechanizmu działania niektórych inkretyn i ich inhibitorów (źródło: przypadki kliniczne, Ilmari Karonen [CC BY-SA (http: // CreativeCommons.Org/licencje/by-sa/3.0/)] przez Wikimedia Commons)
Schemat mechanizmu działania niektórych inkretyn i ich inhibitorów (źródło: przypadki kliniczne, Ilmari Karonen [CC BY-SA (http: // CreativeCommons.Org/licencje/by-sa/3.0/)] przez Wikimedia Commons) Innymi słowy, zamiatanie użył terminu IncredIn, aby oznaczyć każdy hormon jelitowy, który w warunkach fizjologicznych był w stanie stymulować lub przyczynić się do wydzielania hormonów trzustkowych, takich jak insulina, glukagon, polipeptyd trzustki (PP).
Jednak obecnie termin „niesamowity” jest używany tylko do oznaczania tych hormonów zdolnych do stymulowania syntezy zależnej od glukozy insuliny trzustkowej, szczególnie dwóch peptydów znanych jako GIP i LPG-1. Jednak nadejście nowych technologii i głębsze badania endokrynologiczne mogą ujawnić wiele innych peptydów o podobnych działaniach.
Rodzaje inkretyn i ich struktura
Tradycyjnie zdefiniowano tylko dwa niesamowite u ludzi: zależny od glukozy insulinotropowy polipeptyd (GIP) i peptyd typu 1 glukagonu (LPG-1); Dwa hormony funkcjonalnie działają po stymulacji wydzielania insuliny.
Pierwszym z nich, który został izolowany, był zależny od glukozy insulinotropowy polipeptyd (GIP, angielski Zależny od glukozy insulinotropowy polipeptyd). Jest to hormon peptydowy około 42 aminokwasów, który należy do rodziny peptydów glukagon-sekretyny.
 Struktura inkretyny GIP
Struktura inkretyny GIP Drugą nagą inkretyną była 1 peptyd glukagonowy (LPG-1, angielski Peptyd-1 podobny do glukagonu), który jest produktem ubocznym genu, który koduje hormon „proglucagon”; Część C-końcowego końca białka, bardziej dokładna.
Funkcje inkretyn
Początkowo inkretyny zdefiniowano jako czynniki pochodzące z przewodu jelitowego, które mają zdolność do obniżenia poziomu glukozy w osoczu poprzez stymulację wydzielania hormonów trzustki, takich jak insulina i glukagon.
Może Ci służyć: urządzenie lokomotoryczneTa koncepcja została utrzymana wraz z nadejściem Radioinensayos, gdzie potwierdzono stałą komunikację między jelitem a trzustką hormonalną.
Wykazano, że doustne podawanie glukozy wiąże się z istotnym wzrostem poziomu insuliny w osoczu, szczególnie w porównaniu z wynikami uzyskanymi z glukozą podawaną dożylnie.
Uważa się, że inkretyny są odpowiedzialne za wydzielanie prawie 70% insuliny w osoczu po doustnym podawaniu glukozy, ponieważ jest to tajne hormony w odpowiedzi na spożycie składników odżywczych, co zwiększa wydzielanie insuliny glukozy zależnej od insuliny glukozy.
Obecnie podejmuje się wiele wysiłków dotyczących doustnego lub dożylnego podawania niesamowitych pacjentom z chorobami, takimi jak cukrzyca typu 2 lub nietolerancja glukozy doustna. Wynika to z faktu, że badania wykazały, choć wstępne, że substancje te ułatwiają szybki spadek poziomów glikemii po spożyciu pokarmu.
Mechanizm akcji
GIP: insulinotropowy polipeptyd zależny od glukozy
Ta inkretyna jest wytwarzana przez K -Intestine Komórki K (w szczególności w dwunastnicy i jelita czczego) w odpowiedzi na spożycie tłuszczu lub glukozy i jest odpowiedzialna za zwiększenie wydzielania insuliny stymulowanej glukozy.
Ekspresja genu kodującego dla tego czynnika hormonalnego wykazano u ludzi i gryzoni zarówno w żołądku, jak i w jelicie. Badania z tym hormonem wskazują, że pochodzi on z „progipa” prekursora 153 aminokwasów, który ma dwa sygnały peptydów na jego końcówkach N i C-końcowych, które są podzielone w celu zapłaty aktywnego peptydu 42 odpadów.
Połowa życia GIP jest mniejsza niż 7 minut po zsyntetyzowaniu i przetworzeniu enzimatycznym. Peptyd ten jest rozpoznawany przez określony odbiornik, GIPR, który znajduje się w błonie plazmatycznej komórek trzustki, w żołądku, w jelicie cienkim, w tkance tłuszczowej, w krze nadnerczowej, w przysadki, w gruczołach przysadki, w gruczołach przysadki, w gruczołach przysadki, w gruczołach przysadki, w przysadki mózgowej, w przysadki mózgowej, w przysadki mózgowej. serce, w płucach i w innych ważnych narządach.
Może ci służyć: osmolarność w moczuKiedy GIP łączy receptory w komórkach beta trzustki, wyzwala wzrost produkcji AMPC, również hamowanie zależnych kanałów potasowych ATP, wzrost wapnia wewnątrzkomórkowego, a nareszcie egzocytozę granulowania insuliny.
Ponadto ten peptyd może stymulować transkrypcję genów i biosyntezę insuliny, a także inne składniki komórek beta trzustki w celu „cenzurowania” glukozy. Chociaż GIP działa głównie jako niesamowity hormon, wywiera także inne funkcje w innych tkankach, takich jak ośrodkowy układ nerwowy, kości,.
LPG-1: peptyd typu glukagonu
Ten peptyd jest wytwarzany z genu, który koduje „proglukagon”, więc jest to peptyd, który dzieli około 50% tożsamości z sekwencją glukagonu, a zatem nazywa się peptydem „typu glukagonu”.
LPG-1, posttranslacyjny produkt proteolityczny, jest specyficzną tkanką i jest wytwarzany przez komórki jelitowe L w odpowiedzi na spożycie pokarmu. Podobnie jak GIP, ta inkretyna ma zdolność zwiększania wydzielania insuliny stymulowanej przez glukozę.
Ekspresja genetyczna i przetwarzanie
Ten peptyd jest kodowany w jednym z eksonów genu proglukagonu, który jest wyrażany w komórkach alfa trzustki, w komórkach jelitowych L (w dystalnym jelicie) oraz w neuronach łodygi mózgu oraz podwzgórza i podwzgórza i podwzgórza.
W trzustce ekspresja wspomnianego genu jest stymulowana przez post i hipoglikemię (niskie stężenie glukozy we krwi) i jest hamowana przez insulinę. W komórkach jelitowych ekspresja genu dla proglukagonu jest aktywowana przez wzrost poziomu AMPC i spożycie pokarmu.
Produkt wynikający z ekspresji tego genu, peptydu typu glukagonu itp.
Może ci służyć: oś podwzgórza-hypofizy-owcyProdukcja i akcja
Spożycie pokarmu, zwłaszcza bogate w tłuszcz i węglowodany, stymuluje wydzielanie peptydu GLP-1 z komórek L jelita L (stymulacja nerwowa lub mediowana może również wystąpić przez wiele innych czynników).
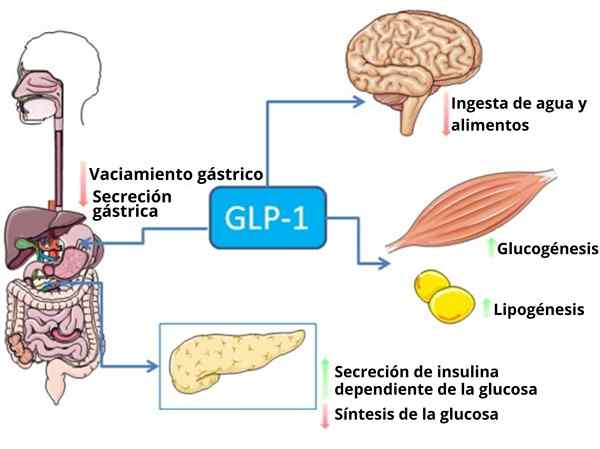 Niektóre funkcje peptydu LPG-1, oprócz jego działania jako niesamowitego hormonu (źródło: BQUB13-CBADIA [CC BY (https: // creativeCommons.Org/licencje/według/3.0)] przez Wikimedia Commons)
Niektóre funkcje peptydu LPG-1, oprócz jego działania jako niesamowitego hormonu (źródło: BQUB13-CBADIA [CC BY (https: // creativeCommons.Org/licencje/według/3.0)] przez Wikimedia Commons) U ludzi i gryzoni peptyd ten jest uwalniany w kierunku torrentu krążenia w dwóch fazach: po 10 lub 15 minutach spożycia, a następnie po 30 lub 60 minutach. Aktywne życie tego hormonu we krwi wynosi mniej niż 2 minuty, ponieważ jest on szybko inaktywowany proteolitycznie przez enzym dipeptydylowy peptydazy-4 (DPP-4).
LPG-1 łączy specyficzny receptor błony (LPG-1R) w różnych komórkach ciała, w tym w niektórych komórkach hormonalnych trzustki, gdzie stymuluje wydzielanie hensuliny insuliny zależne od glukozy zależne od glukozy.
Jak?
Związek JLP-1 do odbiornika w komórkach beta trzustki aktywuje produkcję AMPC za pośrednictwem cyklasy adenylanowej w tych komórkach. Istnieje bezpośrednie hamowanie zależnych kanałów potasowych ATP, które depolaryzują błonę komórkową.
Następnie wzrastają poziomy wewnątrzkomórkowe wapnia, co jest wynikiem wpływu pozakomórkowego wapnia zależnego od LPG-1 przez kanały wapnia zależne od napięcia, aktywację nieselektywnych kanałów kationowych i mobilizacji rezerw wapnia wewnątrzkomórkowych.
Zwiększa się również synteza mitochondrialna ATP, co sprzyja depolaryzacji. Później zależne od napięcia kanały potasu zamykają się, zapobiegając repolaryzacji komórek beta i, wreszcie, wystąpi egzocytoza granulek insuliny.
W układzie żołądkowo-jelitowym połączenie LPG-1 z jego receptorami ma hamujący wpływ na wydzielanie kwasów żołądka i opróżnianie żołądka, co osłabia wzrost poziomu glukozy we krwi związanej z przyjmowaniem pokarmu.

