Struktura hormonu wzrostu (somatotropina), funkcje
- 1671
- 461
- Eugenia Czapla
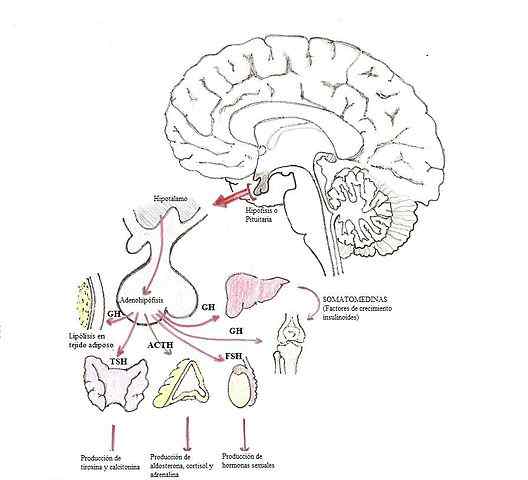
Somatotropina (STH) Hormon wzrostu U (GH) jest stosunkowo niewielkim białkiem wytwarzanym na poziomie adenohypofyzy i zaangażowanym w procesy rozwojowe, wzdłużne wzrost organizmu i kontrolę kilku procesów metabolicznych.
Jest to hormon nielkaro. Hormony gruczołowe z gromadzenia się przysadki mózgowej.
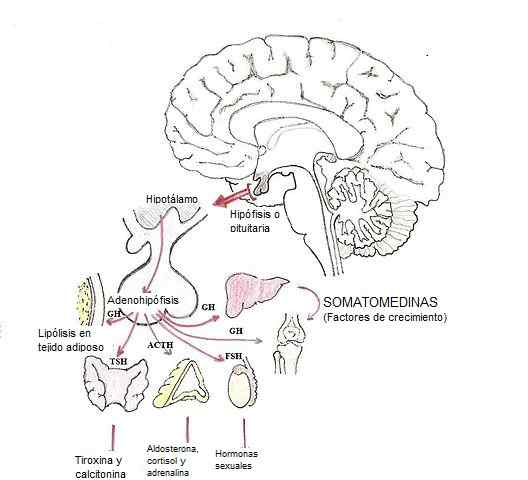 Modyfikacja hormonów w przysadce (źródło: Dubaele / Public Domena, Via Wikimedia Commons)
Modyfikacja hormonów w przysadce (źródło: Dubaele / Public Domena, Via Wikimedia Commons) Hormony Glandotropas to na przykład adrenokortypina (ACTH), gonadotropiny (FSH i LH) i hormon stymulujący tarczycę (TSH) (TSH).
Z drugiej strony hormony bez Glandropas, a wśród których uwzględniono prolaktynę i hormon wzrostu, działają bez rywalizacji o inną gruczoł hormonalny, ponieważ wywierają swoje działania bezpośrednio na białe komórki, których aktywność reguluje.
[TOC]
Struktura
Hormon wzrostu jest stosunkowo małym białkiem, które występuje w kilku izoformach. Główna izoforma składa się z około 191 aminokwasów, ma masę cząsteczkową 22 kDa i pochodzi z dłuższego peptydu prekursorowego (pre-GH) 28 kDa, który jest również wydzielany, ale brakuje to funkcji fizjologicznych.
W swojej strukturze somatotropina wydaje się być homologowana do prolaktyny i naczyniowej somatomamamototropiny (CS), wyprodukowana ta ostatnia w łożysku łożyska. Takie jest podobieństwo, które uważa się za, że cała trójka tworzy rodzinę hormonalną.
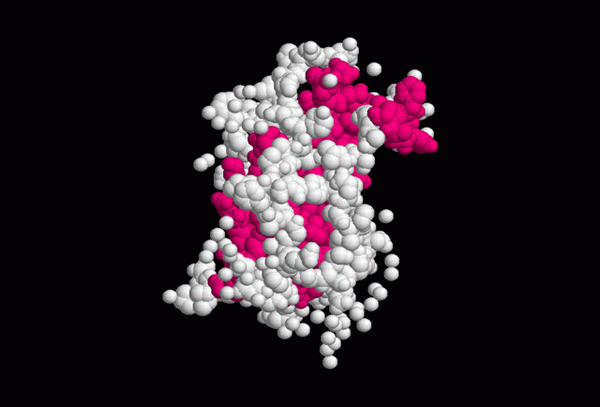 Przybliżona struktura hormonu wzrostu (źródło: роман бекер, przez Wikimedia Commons)
Przybliżona struktura hormonu wzrostu (źródło: роман бекер, przez Wikimedia Commons) Wtórna struktura somatotropiny pokazuje 4 śmigiery alfa stabilizowane dwoma mostami disiarczkowymi, których konfiguracja jest niezbędna do interakcji hormonu z jego odbiornikiem.
Fakt w odniesieniu do struktury i godny wyróżnienia, reprezentuje fakt, że pomimo faktu, że hormony wzrostu różnych gatunków mają niezwykłe podobieństwa z człowiekiem, tylko te ostatnie i naczelne, wywierają efekty znaczące u ludzi.
Funkcje
Funkcje somatotropiny są zwykle opisywane jako te związane z rozwojem i wzrostem organizmu. Również te związane z metabolizmem, które obejmują modyfikacje metabolizmu lipidów i glukozy promowanej przez hormon.
Funkcje wzrostu można jednak również uznać za metaboliczne, ponieważ sugerują one funkcje anaboliczne związane z syntezą białek, co nie wyklucza niektórych innych funkcji bez bezpośredniego związku z metabolizmem, takimi jak proliferacja komórek.
Niektóre funkcje lub działania rozmieszczone przez somatotropinę są wykonywane przez ten hormon bezpośrednio na jego białych tkankach, ale wiele z nich jest wykonywanych przez niektóre inne substancje, których synteza i uwalnianie są stymulowane przez hormon wzrostu.
Synteza IGF
Pierwsza linia działania somatotropiny jest dokładnie syntezą tych substancji, które są znane jako czynniki wzrostu podobne do insuliny (IGF), z czego typy 1 i 2 zostały zidentyfikowane. Są one oznaczone jako IGF1 (najważniejsze) i IGF2, zgodnie z akronimem w języku angielskim.
Czynniki te były początkowo znane i są nadal oznaczone jako mediatorzy somatotropiny lub somatomedin C (IGF1) i A (IGF2) lub również jako aktywność podobna do insuliny nieuprutowej (NSILA). Są one syntetyzowane przez wiele rodzajów komórek, ale występują głównie w wątrobie.
Działania STH i IGF1 są bardzo zróżnicowane. Niektóre ćwiczą każdą z tych substancji niezależnie, czasem w połączeniu i synergistycznie i innym razem działają antagonicznie.
Może ci służyć: elektroforez: podkład, technika, do czego jest przykładyIndukcja wzrostu
Jest to jedno z najważniejszych działań promowanych przez somatotropinę, ale wykonane w połączeniu z IGF1. Chociaż oba indukują wzrost wielu tkanek ciała, ich najbardziej widoczny wpływ wywiera na wzrost szkieletu.
Ten końcowy wynik jest wytwarzany przez kilka efektów indukowanych przez hormon i IGF1. Obejmują one wzrost złoża białka przez komórki chondrocytarne i osteogenne, najwyższą szybkość rozmnażania tych komórek i konwersję chondrocytów do komórek osteogennych; Wszystko to prowadzi do nowej depozytu kości.
Podczas wzrostu i rozwoju organizmu, a przed zamknięciem epifysów kostnych, nowa chrząstka jest osadzona w epifysach, a następnie jej konwersja w nową kość, która wydłuża moc, a epipsy są oddzielone.
Postępujące zużycie chrząstki nasadowej wyczerpuje ją, a kość nie może nadal rosnąć. Pod koniec okresu dojrzewania przepona i nasyfsy i wzrost długiej długości kości są spowolnione do każdego końca i wreszcie się zatrzymują.
Drugi mechanizm może wyjaśnić wzrost grubości kości. Osteoblasty periosteu osadzają nową kość na starym, a osteoklasty eliminują starą kość. Jeśli szybkość osadzania przekracza eliminację, grubość wzrasta.
Gdy hormon wzrostu ćwiczy intensywną stymulację osteoblastów, pod jego skutkiem grubość kości może nadal rosnąć, chociaż jego długość nie jest już modyfikowana z powodu zamknięcia nasadek.
Promowanie depozytów białkowych w tkankach
Efekt ten można osiągnąć poprzez różne mechanizmy: wzrost transportu aminokwasów przez błony komórkowe, wzrost translacji RNA na poziomie rybosomów, wzrost transkrypcji DNA do RNA w jądrze i zmniejszenie białka i aminokwasu Katabolizm.
Inne działania metaboliczne
W tkance tłuszczowej hormon wzrostu promuje lipolizę i uwalnianie kwasów tłuszczowych do torrentu krążenia, co zwiększa jego stężenie w płynach ustrojowych. Jednocześnie sprzyja we wszystkich tkankach konwersja kwasów tłuszczowych w koenzymie acetylu A i jego zastosowanie jako źródło energii.
Stymulacja stosowania tłuszczów, wraz z akumulacją białek ze względu na ich efekt anaboliczny, prowadzi do wzrostu chudej tkanki.
Wzrost mobilizacji tłuszczów może być tak wysoki, że wątroba wytwarza duże ilości kwasu acetooctowego, które prowadzą do ketozy i można wytworzyć stłuszczową wątrobę.
W odniesieniu do metabolizmu węglowodanów, działanie somatotropiny obejmuje spadek zbierania glukozy w tłuszczach i mięśni mięśniowej, zwiększonej produkcji wątroby glukozy i zwiększonej wydzielaniu insuliny.
Wszystkie te efekty są nazywane diabetogenami, a wydzielanie hormonu wysokiego wzrostu może odtwarzać zmiany metaboliczne, które towarzyszą cukrzycy zależnej od nieinsuliny.
Inne funkcje
Działania anaboliczne i mitogenne GH i IGF1 objawiają się również wzrostem i funkcją serca, wątroby, śledziony, tarczycy, grasicy i języka. Hormon może przyczynić się do pogrubienia skóry, stymulacji gruczołów potowych i wzrostu włosów.
W nerkach częstość filtracji kłębuszkowej i synteza kalcytriolu wzrasta, co sprzyja nie tylko wzrostowi, ale także mineralizacji kości. Promuje również erytropoezę i syntezę fibrynogenu i odpowiedź immunologiczną przez stymulację limfocytów T i makrofagów.
Może ci służyć: tkanka nabłonkowa: cechy, opis, funkcje, typyReceptory dla somatotropiny
Działania somatotropiny, w tym promocja syntezy czynników wzrostu podobnych do insuliny, pośredniczą w ich zjednoczeniu ze specyficznymi receptorami wyrażanymi w błonach białych krwinek.
Istnieją dwie formy tych receptorów, z których druga jest krótkim (skróconym) wariantem pierwszego; Skrócona postać, która hamuje funkcję długiego odbiornika i że po nadekspresji spowodowałaby niewrażliwość tkanki na hormon.
Długi odbiornik składa się z 638 aminokwasów i ma domenę zewnątrzkomórkową 250, domenę transmembraalną alfa wynoszącą około 38 i domenę wewnątrzkomórkową 350 aminokwasów. Każda cząsteczka somatotropiny kończy się łączeniem dwóch cząsteczek odbiornika i wytwarzania tak zwanej dimeryzacji receptora.
Ta dimeryzacja aktywuje białko kinazy JAK2 zlokalizowane na wewnątrzkomórkowych końcach każdego monomeru odbiornika, a te aktywne kinaza fosforylują inne substraty, takie jak STAT5 i sam receptor somatotropiny.
Fosforylowane cząsteczki STAT5 cierpią również na dimeryzację, która czyni je bardzo precyzyjnymi regulatorami ekspresji genów i syntezy białek.
Produkcja
Somatotropina jest syntetyzowana na poziomie komórek somatotropowych adenohypofyzy. Komórki te są intensywnie barwione substancjami kwaśnymi, więc są również nazywane kwasofilami. Są razem najliczniejszą grupą komórkową gruczołu, ponieważ reprezentują 50% z 5 różnych rodzajów.
Istnieje kompleks genetyczny 5 genów w długim ramieniu ludzkiego chromosomu 17, który koduje dla różnych izoform hormonu wzrostu i ludzkiego somatomamotropiny (HC) (HC).
Jednym z nich jest normalny HGH-N, który koduje najliczszą formę ludzkiego hormonu wzrostu, który jest wyżej wymienionych 22 kDa i stanowi 75% całkowitego krążącego hormonu wzrostu.
Jego posłańca RNA jest poddawany „Cut i splicing” Aby wytworzyć mniejszą postać hormonu, 20 kDa, w którym brakuje odpadów aminokwasowych od 32 do 46 i reprezentuje 10%.
Drugi gen (HGH-V) jest wyrażany głównie w łożysku i koduje wariant formy HGH, z której tylko znaczące ilości pojawiają się w krążeniu podczas ciąży. Pozostałe 3 geny kodują izoformy somatomamototropiny człowieka.
Uwolnienie
Zarówno synteza, jak i wydzielanie lub uwalnianie hormonu wzrostu są regulowane przez czynniki stymulujące i hamujące takie funkcje.
Stymulujące wpływy
Wśród głównych humorystycznych wpływów stymulujących syntezę i wydzielanie somatotropiny są peptydy GHRH (hormon wzrostu uwalniający hormon) i greliny.
Hormon wyzwalający hormon wzrostu (GHRH) jest peptydem podwzgórza, który istnieje w dwóch wariantach odpowiednio 40 i 44 aminokwasów. Przeprowadza w komórkach somatotropas do syntezy AMPC i do aktywacji specyficznego czynnika transkrypcyjnego PIT1 dla hormonu wzrostu.
Grelina jest endogenem hormonu wzrostu hormonu wzrostu. Jest to peptyd około 28 aminokwasów zsyntetyzowanych na podwzgórzu i poziomie żołądka. Działa synergalnie z GHRH, której uwalnianie promuje, hamując somatostatynę. Działa poprzez receptory, które aktywują fosfolipazę C.
Niektóre parametry metaboliczne, takie jak hipoglikemia, niski poziom wolnych kwasów tłuszczowych we krwi i wysokie stężenia aminokwasów, są ważnymi bodźcami wydzielania hormonu wzrostu.
Może ci służyć: 12 etapów rozwoju człowieka i jego cechyInnymi czynnikami stymulującymi, które liczą się ostre stres, przeciążenie ciała, ból, sterydy płciowe (dojrzewanie), dopamina, stymulacja receptorów α2, acetylocholina, galanina, serotonina i β-endorfina.
Wpływy hamujące
Wśród nich są somatostatyna lub inhibitor hormonu uwalniania hormonu wzrostu (GHRIH) i ujemne sprzężenie zwrotne.
Somatostatyna jest peptydem podwzgórza 14 aminokwasów, który hamuje wydzielanie, ale nie syntezę hormonu wzrostu. Długi wariant, 28 aminokwasów, jest syntetyzowany w przewodzie pokarmowym. Oba warianty wiążą się z tym samym odbiornikiem i hamują cykliczną syntezę AMP.
Jeśli chodzi o negatywną informację zwrotną, GH uwolniono poprzez działanie samoziarniste, hamuje własne dalsze uwalnianie. IGF1 hamuje podwzgórze hormonu wzrostu hormonu wzrostu i stymuluje somatostatynę, podczas gdy hamuje syntezę GH w przysadce mózgowej.
Niektóre parametry metaboliczne, takie jak hiperglikemia, wysokie poziomy wolnych kwasów tłuszczowych w osoczu i niskie poziomy aminokwasów, są inhibitorami wydzielania somatotropiny.
Inhibitory są również zimne, przewlekłe stres, otyłość, progesteron, hormony tarczycy, deficyty lub nadwyżek kortyzolu i stymulacja receptorów adrenergicznych β2 β2.
Dawka
Terapeutyczne zastosowanie biosyntezy hormonu wzrostu jest wskazane w leczeniu tych cierpień, w których ujawniono niedobór jego wydzielania, w krasnoluzmie przysadki i dzieci o niskiej wielkości według zespołu Turnera.
Podawanie jest dokonywane w postaci rozwiązania do wstrzykiwań odbudowanych z drogi zawierającej liofilizowaną z 40 u.Siema. hormonu biosyntetycznego i do którego dodaje się 2 ml towarzyszy 0,9 % roztworu chlorku sodu.
W niedoborze hormonu wzrostu u dzieci zaleca się od 0,07 do 0,1 u.Siema./kg masy ciała dziennie. W zespole Turnera 0,14 u.Siema./kg masy ciała dziennie. W przypadku niedoboru hormonu wzrostu u dorosłych: 0,018 do 0,036 u.Siema./kg masy ciała dziennie.
Efekty
Terapeutyczne podawanie hormonu wzrostu może towarzyszyć pewne niekorzystne efekty dodatkowe, takie jak manifestowanie nadwrażliwości poprzez uogólnioną pokrzywkę, hipoglikemia na czczo, zapalenie w miejscu wstrzyknięcia i bólu głowy pasażerskiego.
Opisano rozwój pewnego łagodnego nadciśnienia śródczaszkowego, częściej u dzieci i mniej u dorosłych.
Jeśli chodzi o metabolizm węglowodanów, rozwój cukrzycy odnotowano u pacjentów, którzy otrzymali leczenie hormonem wzrostu.
W odniesieniu do układu mięśni szkieletowych istnieją dowody zapalnego zapalenia mięśni z mięśniami i osłabieniem mięśni, wytwarzanych nie przez hormon, ale być może metakresol stosowany jako konserwatystka w formule.
Zgłoszono przypadki ginekomastii, niedokrwistości i ostrego zapalenia trzustki.
Bibliografia
- Ganong WF: Pukłowiec, wydanie 25. Nowy Jork, McGraw-Hill Education, 2016.
- Guyton AC, Hall JE: Hormony przysadki i ich kontrola według podwzgórza, w Podręcznik fizjologii medycznej, 13th Ed, AC Guyton, Je Hall (red.). Philadelphia, Elsevier Inc., 2016.
- Lang F, Verrey F: hormon, w Physiologie des Menschen roztoczy patofizjologa, 31 TH ED, RF Schmidt i in. (Eds). Heidelberg, Springer Medizin Verlag, 2010
- Voigt K: System Endokrines, w Physiologie, 6th Ed; R Klinke i in. (Eds). Stuttgart, Georg Thieme Verlag, 2010.
- Widmaier EP, Raph H i Strang KT: Układ hormonalny. Podwzgórze i przysadka mózgowa w ludzkiej fizjologii Vandera: mechanizmy funkcji ciała, wydanie 13; EP Windmaier i in. (Eds). Nowy Jork, McGraw-Hill, 2014.

