Wodorotlenek strontu (SR (OH) ₂)

- 1653
- 155
- Gabriela Łuczak
 Wodorotlenek strontu
Wodorotlenek strontu Co to jest wodorotlenek strontu?
On Wodorotlenek strontu (SR (OH) ₂) jest nieorganicznym związkiem chemicznym utworzonym przez jon strontu (SR) i dwa jony wodorotlenkowe (OH). Związek ten uzyskuje się przez połączenie soli zrębnej z silną zasadą, co powoduje związek o charakterze alkalicznym, którego wzór chemiczny to SR (OH)2.
Ogólnie rzecz biorąc, do przygotowania wodorotlenku strontu, wodorotlenku sodu (NaOH) lub wodorotlenku potasu (KOH) jest stosowany jako silna podstawa. Z drugiej strony sól strontowa (lub jon strontu), która reaguje z silną podstawą, to azotan strontu SR (nie3)2 A proces opisuje następującą reakcję chemiczną:
2KOH + SR (nie3)2 → 2KNO3 + SR (OH)2
W roztworze kation strontu (SR+) Skontaktuje się z anionem wodorotlenowym (och-) tworzenie podstawowej soli joonowej Strontium. Ponieważ stront jest metalem alkalicznym, wodorotlenek strontu jest uważany.
Uzyskanie wodorotlenku strontu
Oprócz wcześniej wyjaśnionego procesu można powiedzieć, że po przeprowadzeniu reakcji SR (OH)2 wytrąć w roztworze. Następnie jest to poddawane procesowi mycia i suszenia, w końcu uzyskując bardzo drobny biały proszek.
Alternatywną metodą uzyskiwania wodorotlenku strontu jest ogrzewanie węglanu strontu (SRCO3) lub siarczan strontu (srso4), z pary w temperaturze od 500 ° C do 600 ° C. Reakcja chemiczna występuje, jak pokazano poniżej:
SRCO3 + H2O → Sr (OH)2 + WSPÓŁ2
SRS + 2H2O → Sr (OH)2 + H2S
Może ci służyć: kwas siarkiStruktura chemiczna i właściwości fizykochemiczne
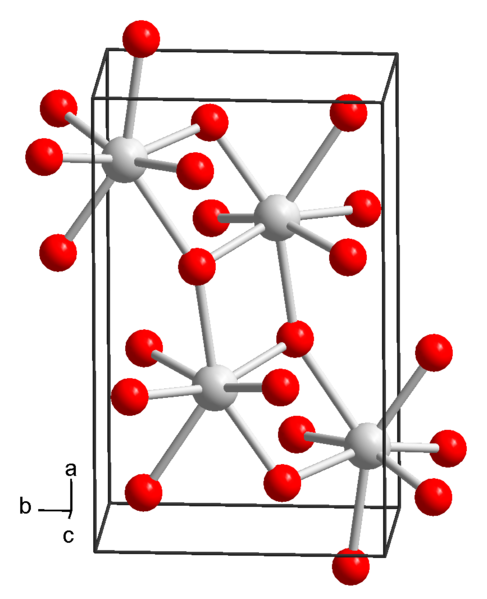 Struktura chemiczna wodorotlenku strontu. Źródło: Wikimedia Commons
Struktura chemiczna wodorotlenku strontu. Źródło: Wikimedia Commons Obecnie znane są 3 formy wodorotlenku strontu: oktahydrat, monohydrat i bezwodne.
Oktonowany wodorotlenek strontu
Od roztworów w normalnych warunkach temperatury i ciśnienia (25 ° C i 1 atm), wodorotlenek strontu wytrąca się w oktahydrat, którego wzór chemiczny to SR (OH)2∙ 8H2ALBO.
Związek ten ma masę molową 265,76 g/mol, gęstość 1,90 g/cm i wytrąca się jako kryształy tetragonalne (z grupą przestrzenną P4/NCC) czworokątnego wyglądu pryzmatycznego i bezbarwnego.
Podobnie, ośmiobrotowy wodorotlenek strontu ma zdolność wchłaniania wilgoci atmosferycznej, ponieważ jest to łatwo pyszny związek.
Wodorotlenek monohydowany
Zgodnie z badaniami mikroskopii optycznej (przeprowadzone za pomocą techniki dyfrakcji x -ray), poprzez podniesienie temperatury do około 210 ° C - stałe ciśnienie atmosferyczne - SR (OH)2∙ 8H2O jest odwodniony i przekształcany w monohydowany wodorotlenek strontu (SR (OH)2∙ h2ALBO).
Ta postać związku ma masę molową 139,65 g/mol, a jej temperatura topnienia wynosi -73,15 ° C (375K). Ze względu na konfigurację atomową przedstawia to mniej rozpuszczalności w wodzie niż opisana w postaci oktahydratu.
Bezwodny wodorotlenek strontu
Kontynuując wzrost temperatury systemu do około 480 ° C, odwodnienie jest przedłużane, aż bezwodny wodorotlenek rozciągający.
W przeciwieństwie do nawodnionych kształtów, ma masę molową 121,63 g/mol i gęstość 3625 g/cm3. Jego temperatura wrzenia jest osiągana w 710 ° C (1 310 ° F lub 983 K), podczas gdy temperatura topnienia wynosi 535 ° C (995 ° F lub 808 K).
Może ci służyć: Ididio 192Rozpuszczalność
Wodorotlenek oktahydratu strontu ma rozpuszczalność w wodzie 0,91 gramów na 100 mililitrów (mierzonych w 0 ° C), podczas gdy jego bezwodna postać w podobnych warunkach temperatury ma rozpuszczalność 0,41 gramów na 100 mililitrów.
Podobnie ta substancja jest uważana za nierozpuszczalną w acetonie i całkowicie rozpuszczalna w kwasach i chlorku amonu.
Reaktywność chemiczna
Wodorotlenek strontu nie jest łatwopalny, jego reaktywność chemiczna pozostaje stabilna przy umiarkowanych temperaturach i ciśnieniach i jest w stanie pochłonąć dwutlenek węgla z powietrza atmosferycznego, przekształcając go w węglan strontu strontu.
Ponadto jest to poważnie irytujący związek, jeśli skontaktujesz się ze skórą, drógami oddechowymi lub innymi błonami śluzowymi.
Zastosowanie wodorotlenku strontu
Ze względu na charakterystykę higroskopijną i podstawowe właściwości wodorotlenek strontu jest używany do różnych zastosowań w branży:
- Ekstrakcja moice i rafinacja cukru z buraków.
- Plastikowy stabilizator.
- Tłuszcze i smary.
Ekstrakcja moice i rafinacja cukru buraka
Na początku XXI wieku w Niemczech rozciągliwy wodorotlenek zaczął być wykorzystywany do rafinacji buraków z buraków, poprzez opatentowany proces Carla Scheiblera w 1882 roku.
Ta procedura polega na mieszaninie wodorotlenku strontu i słodkiej miazgi buraka, co powoduje nierozpuszczalny disacharyd. Rozwiązanie to jest oddzielone dekantacją, a po przeprowadzeniu procesu rafinacji cukru jest uzyskiwana jako produkt końcowy.
Chociaż ta procedura jest nadal stosowana, istnieją inne metody o znacznie większym zapotrzebowaniu na tańsze, które są stosowane w zdecydowanej większości światowych rafinerii cukrowych. Na przykład metoda barsil, która wykorzystuje krzemian baru lub metodę Steffen, przy użyciu wapna jako środka ekstraktora.
Może ci służyć: anomerowy węgiel: co to jest, charakterystyka, przykładyTłuszcze stronniane
Są to smarowanie tłuszczów zawierających wodorotlenek strontu. Są one w stanie silnie przestrzegać powierzchni o charakterystyce metalu, są wodoodporne i podtrzymują nagłe zmiany temperatury.
Ze względu na ich dobrą stabilność fizyczną i chemiczną tłuszcze te są stosowane jako smary przemysłowe.
Plastikowy stabilizator
Zdecydowana większość tworzyw sztucznych, narażona na czynniki klimatyczne, takie jak słońce, deszcz i tlen atmosferyczny, modyfikuje ich właściwości i degraduj.
Ze względu na jego znaczną wodoodporność wodorotlenek strontu jest dodawany do tych polimerów - podczas fazy fuzyjnej - działający jako stabilizator w produkcji produktów z tworzywa sztucznego w celu przedłużenia jego użytkowania.
Inne aplikacje
- W branży malarskiej jest stosowany jako niezbędny dodatek do przyspieszenia procesu suszenia w obrazach komercyjnych i przemysłowych.
- Z wodorotlenku strontu uzyskuje się sole lub jony strontu, które są wykorzystywane jako surowiec do produkcji artykułów pirotechniki.
Bibliografia
- Wikipedia (n.D.). Wodorotlenek strontu. Odzyskane z.Wikipedia.org
- Pubchem (s.F.). Wodorotlenek strontu. Uzyskane z Pubchem.NCBI.NLM.Nih.Gov
- Honeywell (s.F.). Octahydrat wodorotlenku stonżu. Pobrano z Honeywell.com

