Elektroforeza podkładowa, technika, do czego jest przykłady

- 4150
- 1313
- Prokul Woliński
Elektroforeza Jest to technika stosowana do oddzielenia cząsteczek w polu elektrycznym. Musi to zrobić konkretnie z migracją cząstek obciążonych pod wpływem prądu elektrycznego stosowanego między dwoma biegunami, jednym dodatnim i drugim ujemnym.
Elektroforeza jest obecnie jedną z najbardziej rutynowych procedur, które mają miejsce podczas opracowywania eksperymentu, szczególnie w dziedzinach związanych z chemią analityczną, biochemią oraz naukami biologicznymi i medycznymi w ogóle.
 Wiadro elektroforezy. Źródło: Melodygar/CC BY-SA (https: // creativeCommons.Org/licencje/nabrzeże/4.0)
Wiadro elektroforezy. Źródło: Melodygar/CC BY-SA (https: // creativeCommons.Org/licencje/nabrzeże/4.0) Służy do oddzielania białka, peptydów, DNA, RNA i innych w zależności od ich obciążenia, wielkości, gęstości i czystości.
Różne domy komercyjne zaprojektowały różne formaty, z różnymi aplikacjami i odpowiednimi zyskami do określonych celów, jednak wszystkie procedury wymagają tych samych podstawowych elementów:
- Źródło energii do generowania ładunku elektrycznego
- Medium wsparcia separacji
- Rozwiązanie buforowe (bufor) Aby utrzymać pH na stałym poziomie
[TOC]
Podstawa
Elektroforeza jest niczym więcej niż migracja (separacja) cząstek lub obciążonych cząsteczek (naturalnie lub sztucznie) w pożywce lub wsparciu pod wpływem pola elektrycznego.
Technika oparta jest na jednym z głównych fizycznych równań elektromagnetyzmu, zgodnie z którym siła jest równa ładunku elektrycznego pomnożonego przez pole elektryczne przyłożone w tym punkcie (F (siła) = Q (ładunek elektryczny) x E (pole elektryczne (pole elektryczne ).
Zgodnie z tym równaniem dwie cząstki o tej samej masie, ale o różnym obciążeniu, przejdą do różnych prędkości w tym samym polu elektrycznym. Ponadto prędkość ruchu tych cząstek będzie zależeć od związku między ich obciążeniem a masą.
Naukowcy skorzystali z tych właściwości i relacji ładunkowych/masy, aby oddzielić składniki od biomolekuł w swoich najmniejszych częściach, a także do oddzielenia różnych cząsteczek w mieszaninie, między innymi.
Ważne jest, aby pamiętać, że cząsteczki biologiczne, takie jak aminokwasy, peptydy, białka, niektóre węglowodany, nukleotydy i kwasy nukleinowe mają coś, co nazywamy „grupami jonizowanymi”, więc mogą istnieć jako gatunki pozytywne lub ujemnie naładowane w pewnych warunkach pH.
Technika
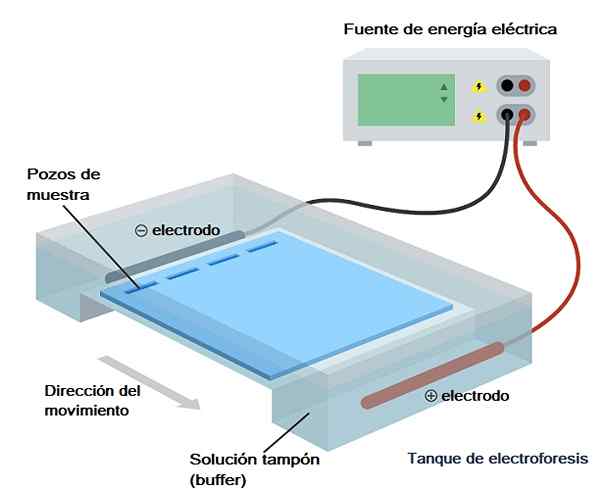
Chociaż istnieją różne rodzaje elektroforezy, elektroforeza żelowa jest najczęściej stosowana w analizie biochemicznej, biologii molekularnej i biotechnologii, więc będzie o tym krótko opowiedzieć w kategoriach technicznych.
Jak sama nazwa wskazuje, elektroforeza żelowa implikuje zastosowanie stałego podłoża wspornika w kształcie stałego, albo do analizy/oddzielenia mieszanin białka lub kwasów nukleinowych (DNA i/lub RNA) pod wpływem pola elektrycznego pola elektrycznego.
System lub aparat stosowany do wykonywania elektroforetycznego „biegu” może być pozioma (zwykle stosowana do kwasów nukleinowych) lub pionowo (zwykle stosowany do białka).
- Przykład techniki elektroforezy kwasu nukleinowego
Kwasy nukleinowe są zwykle oddzielone przy użyciu żeli agarozowych (polisacharyd galaktozy), który jest przygotowywany z odpowiedniego roztworu buforowego (Tris/Octan/EDTA lub TRIS/BORATO/EDTA) i którego stężenie określi „rozdzielczość” fragmentów różnych rozmiarów rozmiarów.
Może ci podać: Ziemia łańcuch pokarmowy: linki i przykładprzygotowanie próbki
Pierwszym krokiem przed wykonaniem elektroforetycznego przebiegu w żelu agarozowym jest uzyskanie próbki. Będzie to zależeć od końca eksperymentalnego, a próbki mogą być iloczynem trawienia enzymatycznego, od reakcji łańcuchowej polimerazy (PCR), oczyszczania kwasów nukleinowych itp.
 Mieszanka próbki z buflem obciążenia.Org/licencje/według/4.0) Via Wikimedia Commons)
Mieszanka próbki z buflem obciążenia.Org/licencje/według/4.0) Via Wikimedia Commons) Po uzyskaniu jest to mieszane z kolorowym rozwiązaniem (roztwór obciążenia), który umożliwia szybkie odkładanie próbki w studni, ponieważ ma glicerol i barwnik, który umożliwia uruchomienie wizualnie.
Przygotowanie żelu
Ten krok polega na zmieszaniu niezbędnej ilości podłoża żelującego (agarozy) z roztworem buforowym, topieniem go za pomocą ciepła i utrwalając go na podporę, która działa jako „pleśń”.
Podczas gelifikacji niektóre „grzebienia” są wprowadzane do żelu umieszczonego w „formie”, aby ograniczyć „studnie”, w których próbki zostaną wprowadzone przed przebiegiem.
Po ochłodzeniu i utrwalaniu żelu „Combs” zostaną usunięte i wprowadzane do pojemnika znanego jako „wiadro”, który jest pełen roztworu buforowego (Tris/Acetate/Edta lub Tris/Borato/Borato/Edta).
To wiadro jest z kolei uwzględnione w tak zwanej „komorze elektroforetycznej”, która jest niczym więcej niż pojemnikiem, przez który jest przekazywany pole elektryczne i ma przestrzeń, w której żel jest wprowadzany i dwie sekcje, które są wypełnione Rozwiązanie buforowe (bufor uruchomić).
Ten aparat ma dwie elektrody, jedną pozytywną i jedną ujemną, wśród których ruch jonowy jest wytwarzany po zastosowaniu pola elektrycznego (jest podłączony do źródła zasilania).
Ładowanie próbek
Po zmieszaniu próbek z odpowiednim roztworem obciążenia wprowadzane są one do „studni” wcześniej wykonanych do żelu.
Ponieważ kwasy nukleinowe mają ujemne obciążenie netto, migrują z bieguna ujemnego do dodatniego, więc należy to wziąć pod uwagę, gdy kamera jest podłączona do źródła zasilania, zapewniając, że biegun ujemny odpowiada większości miejsca obok miejsca w miejscu gdzie próbki zostały załadowane.
Czas koryta jest ustanowiony w ścisłej zależności od badacza odpowiedzialnego za eksperyment. Napięcie jest zazwyczaj obliczane w stosunku 5 woltów procentowym w żelu, który oddziela dwie elektrody.
Wyświetlacz
Kiedy żel działa (gdy próbki przemierzają żel z jednego końca do drugiego), jest on zanurzony w roztworze etydowego bromku (ETBR), barwnika przeplatanego między bazami azotu i tej „marki”, więc więc „marka”, więc Można je wizualizować w transilumenancie za pomocą światła ultrafioletowego.
Do czego służy elektroforeza?
Elektroforeza była historycznie używana z wieloma celami. Dziś jednak jego przydatność zależy w dużej mierze od „pytania”, o które badacz jest pytany w odniesieniu do zjawiska lub określonego systemu, a także od rodzaju elektroforezy, z której chce użyć.
Może ci służyć: topoizomeraza: co to jest, cechy, funkcje, typyMożemy jednak zaciągnąć niektóre z głównych funkcji, jakie ta technika ma, zaczynając od najbardziej „rzadkich” i kończących się najpopularniejszymi i przeważnie wykorzystywanymi w świecie nauk biologicznych. Elektroforeza jest przydatna:
- Do analizy ilościowej złożonych mieszanin makrocząsteczek i do obliczenia potencjalnej „zeta” (właściwość koloidalna cząstki w ciekłym pożywce pod wpływem statycznego pola elektrycznego).
- Do analizy surowic krwi do celów diagnostycznych.
- Do oddzielenia glukoprotein, lipoprotein i hemoglobiny krwi.
- Do analizy żywności, produktów farmaceutycznych i zanieczyszczeń środowiskowych.
Elektroforeza w żelach agarozowych
- Do oddzielenia fragmentów DNA po trawieniu enzymami ogranicznymi.
- Do oddzielenia cząsteczek kwasu nukleinowego przed przeniesieniem na błony do kolejnych analiz.
- Do analizy produktów PCR (reakcja łańcuchowa polimerazy) weryfikującą, czy wystąpiło, czy nie.
- Dla oszacowania wielkości cząsteczek w mieszaninie DNA lub RNA.
- Do oszacowania ilości i/lub jakości oczyszczonych kwasów nukleinowych.
Elektroforeza w żelach poliakryloamidowych w warunkach denaturalizujących lub natywnych
- Aby określić wielkość białka.
- Zidentyfikować białka.
- Aby określić czystość próbki po kilku etapach oczyszczania.
- W celu zidentyfikowania obecności wewnątrzcząsteczkowych połączeń disiarczkowych.
- Aby określić interakcję między białkami.
- Aby określić punkt izoelektryczny białka.
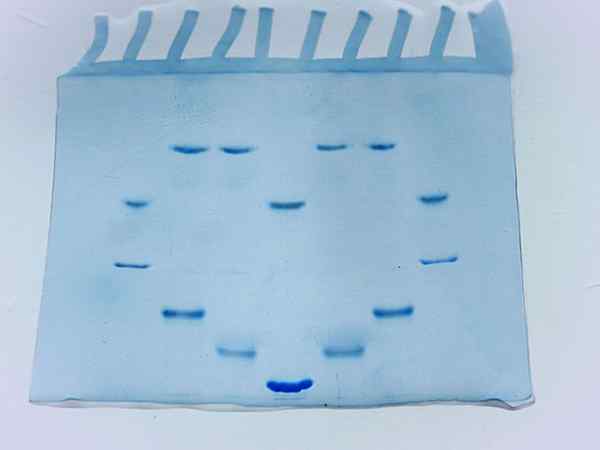 Fotografia żelu akryloamidowego po przebiegu kilku próbek białka (źródło: larionova.Marina/cc by-sa (https: // creativeCommons.Org/licencje/nabrzeże/4.0) Via Wikimedia Commons)
Fotografia żelu akryloamidowego po przebiegu kilku próbek białka (źródło: larionova.Marina/cc by-sa (https: // creativeCommons.Org/licencje/nabrzeże/4.0) Via Wikimedia Commons) Czynniki wpływające na elektroforeza
Migracja cząstki w polu elektrycznym zależy od różnych czynników, w tym:
- Twój ładunek elektryczny
- Jego wielkość molekularna
- Jego hydrofobowość i forma
- Wielkość zastosowanego pola elektrycznego
- Zastosowana temperatura systemu i siła jonowa roztworu buforowego
- Charakter środowiska, w którym się znajduje
W odniesieniu do próbki
Wśród parametrów związanych z cząstkami (próbką), które podlegają pola elektrycznego, główne czynniki wpływające na ten proces mają związek z ich obciążeniem, rozmiarem i kształtem.
Im większe obciążenie netto cząstki, tym większa jej szybkość migracji i ta wielkość będzie zależeć od pH. Jednak związek z wielkością jest odwrotnie proporcjonalny, co oznacza, że im bardziej „duża” cząsteczka, tym wolniej migruje.
Może ci służyć: Lia Agar (żelazna lizyna): co to jest, podkład, przygotowanie, użyciaW odniesieniu do pola elektrycznego
Do tej pory rozmawialiśmy o znaczeniu pola elektrycznego w celu osiągnięcia ruchu cząstki przez elektroforeza, ale nie zdefiniowaliśmy tego, co to jest: siła elektryczna na jednostkę obciążenia lub, w prostszym okresie, obszar przestrzeni, w którym istnieje siła elektryczna.
Parametry dotyczące pola elektrycznego, które mogą wpływać na migrację, to napięcie, prąd i opór.
Napięcie wpływa na „czas lotu” cząsteczek oddzielonych po zastosowaniu pola elektrycznego. Im wyższy jest, tym szybszy ruch.
Prąd (ciągłe i jednolite elektronach, które są „popychane” przez źródło napięcia) jest przeprowadzany między elektrodami układu elektroforetycznego dzięki jonom obecnym w roztworze buforowym. Jest bezpośrednio związany z napięciem.
W odniesieniu do roztworu buforowego
Skład, siła jonowa i pH roztworu bufora są głównymi parametrami, które wpływają na elektroforetyczne „bieg”, ponieważ bezpośrednio wpływają na niektóre właściwości próbek, zwłaszcza ładunek elektryczny.
Ponieważ? Roztwór bufora stabilizuje pH pożywki nośnej, w której występuje elektroforeza. Jego skład może wpływać na przesunięcie cząstek migrujących, a także stężenie jonowe, ponieważ jest on bezpośrednio związany z prądem.
W odniesieniu do medium wsparcia
Różne typy i formaty elektroforezy przedstawiają również różne media, na których występuje migracja i gdzie można ją następnie „zarejestrować”.
Szybkość migracji cząsteczek poddanych elektroforezie zależy od rodzaju pożywki nośnej, która zwykle powinna być obojętna.
Jego charakterystyka absorpcji, electroendo-osmoza jest ważna (pojemność ruchu cieczy przez membranę pod wpływem pola elektrycznego) i jego molekularne sito sitowe.
Przykłady zastosowania elektroforezy
Klasyczne przykłady technik elektroforetycznych stosowanych w biologii i biotechnologii obejmują:
- Elektroforeza w żelach agarozowych (angielski Żel elektroforezy)
- Elektroforeza w żelach akryloamidowych w denaturalizujących warunkach (SDS-PAGE, angielski Elektroforeza żelowa dodecylobrylowa sodowa)
- Elektroforeza w żelach akryloamidowych w warunkach rodzimych (BN-PAGE, angielski Blue Native Poliakryloamid Gel Electrroforeis)
- Elektroforeza w dwóch wymiarach (2D-strony, z angielskiego Dwuwymiarowa elektroforeza żelu poliakryloamidowego)
- Elektroforeza kapilarna (z angielskiego Kapilara elektroforezy)
- Isolectroenfoque (angielski Izolowanie)
- Pulsowana elektroforeza pola (angielski Pulsowane elektroforeza pola)
Bibliografia
- Beck, Kevin. (2020, 25 maja). Rodzaje elektroforezy. Naukowe.com. Pobrano z nauki.com
- Eseje, Wielka Brytania. (Listopad 2018). Rodzaje i zastosowania elektroforezy. Pobrano z Ukessays.com
- Nelson, zm. L., Lehninger, a. L., & Cox, m. M. (2008). Zasady biochemii lehninger. Macmillan.
- Parmar, s. 1. (Sierpień 2018). Elektroforeza: znaczenie, definicja i klasyfikacja (ze schematem). Technologia biologiczna. Pobrano z biotechnologii.com
- Perrett, zm. (2010). 200 lat elektroforezy. Chromatog. Dzisiaj 4-7.
- Righetti, s. 1. G. (2005). Elektroforeza: March of Pennies, March of Dimes. Journal of Chromatography A, 1079 (1-2), 24-40.
- Rilbe, h. (1995). Som Reminisciones of the History of Electrroforeis. Elektroforeza, 16 (1), 1354-1359.
- Vesterberg lub. (1993). Krótka historia metod elektroforetycznych. Elektroforeza, 14 (1), 1243-1249.
- Vinayagam, m. (Brak daty). Czynniki wpływające na elektroforeza. Akademia.Edu. Pobrano ze środowiska akademickiego.Edu
- « Wyjaśnienie równowagi chemicznej, czynniki, typy, przykłady
- Pochodzenie kultury Toltec, lokalizacja, cechy, organizacja »

