Struktura, właściwości, właściwości, właściwości, właściwości, właściwości
- 919
- 20
- Paweł Malinowski
On Siarczan sodu dodecyl (SDS), jest anionową, syntetyczną i amfifilową solą organiczną. Część apolarna i hydrofobowa odpowiada łańcuchowi węglowodorów; Podczas gdy część polarna i hydrofilowa jest spowodowana siarczanem, z obciążeniem ujemnym.
SDS jest środkiem powierzchniowo czynnym: jego cząsteczki są umieszczane na powierzchni roztworów wodnych, co powoduje spadek napięcia powierzchniowego. Ta funkcja pozwala na zastosowanie w szamponie, kremach dentystycznych, mydłach i innych artykułach dotyczących higieny osobistej i sprzątaniu domu.
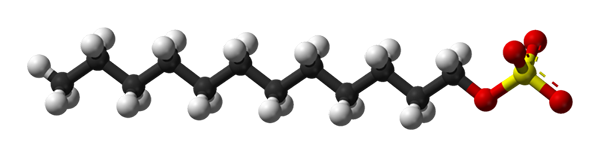
 Struktura dodania siarczanu sodu. Źródło: Benjah-BMM27 przez Wikipedia.
Struktura dodania siarczanu sodu. Źródło: Benjah-BMM27 przez Wikipedia. Siarczan sodu dodecyl wiąże się z białkiem i wytwarza jego rozwijanie, zdobywając wydłużony kształt. Grupy siarczanu są narażone na wodę, nabywając ujemne białka obciążenia, których liczba jest proporcjonalna do ich masy cząsteczkowej.
Z tego powodu SDS umożliwia określenie masowych masy białek przez elektroforeza w poliakryloamidu.
Chociaż podejrzewano możliwe działanie rakotwórcze SDS, nie zostało to jednoznacznie wykazane, że tak jest. SDS może wytwarzać, podobnie jak inne detergenty, podrażnienie skóry i oczu.
[TOC]
Struktura SDS
Na pierwszym obrazie pokazano cząsteczkę SDS za pomocą modelu sfery i słupków. Jak widać, ma hydrofobowy i apolowy ogon węglowy (czarno -białe kule); A jednocześnie głowa polarna, dzięki obecności grupy -4- (żółte i czerwone kulki).
Chociaż nie jest to pokazane, powinna istnieć fioletowa kula reprezentująca kation NA+, tuż obok grupy -4-, interakcja elektrostatycznie.
To powiedziawszy, jest to rozumiane gołym okiem, dlaczego ten związek jest amfiphylliczny; a także napięcie anionowe, ponieważ obciążenie SDS jest ujemne i może przyciągnąć inne kationy oprócz Na+.
Cząsteczka daje fałszywe wrażenie sztywności, nieruchomej struktury liniowej. Jednak jest to odwrotnie. SDS można porównać do „robaka”, którego ogon węglowy przedstawia wiele wibracji i obrotów jego prostych linków. To sprawia, że jest w stanie przyjmować różne konformacje lub fałdy na środku; Na przykład w wodzie.
Kryształy
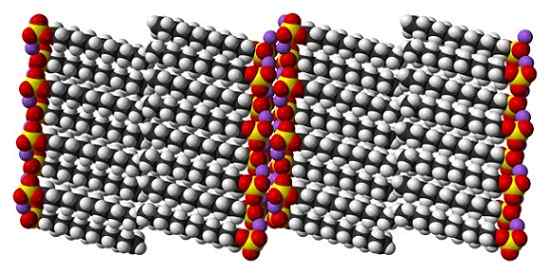 Struktura krystaliczna siarczanu dodecylu sodowego. Źródło: Benjah-BMM27 [domena publiczna]
Struktura krystaliczna siarczanu dodecylu sodowego. Źródło: Benjah-BMM27 [domena publiczna] Chociaż prawdą jest, że siarczan sodu dodecyl jest dynamiczną cząsteczką, w stanie stałym nie musi się poruszać, zachowując się jak „prosty” pasek. I tak, każda cząsteczka lub słupek są ustawione w taki sposób, że interakcje między kolejkami gazowanymi, a jednocześnie, wzrosną obciążenia ich obciążeń jonowych.
Może ci służyć: chloryn sodu (NaClo2): struktura, właściwości, zastosowania, ryzykoRezultatem jest powstawanie kryształu monoklinowego, w którym cząsteczki SDS są pakowane w kilka kolumn barowych (obraz górny). Siły międzycząsteczkowe, które je jednoczą, są takie, że kryształy te wymagają temperatury 206ºC w celu stopienia fazy ciekłej.
Micele
Poza komfortem swoich kryształów cząsteczka SDS nie może już pozostać w miejscu; Zacznij skręcać ogon, aby zwiększyć lub zmniejszyć interakcje ze środowiskiem zewnętrznym.
Jeśli to medium jest wodą, występuje zjawisko zwane tworzeniem miceelli: węgiel i hydrofobowe ogony wiążą się z otoczeniem, podczas gdy głowy polarne, grupy -4-, Pozostają na powierzchni oddziałując z cząsteczkami H2ALBO.
Następnie miceella nabywa oblate elipsoidowe morfologię (taką jak Ziemia, ale bardziej zmiażdżona). W krysztale są one jak bloki prętów, a w wodnej pożywce jak micele elipsoidowe. Co by było, gdyby medium było olejem? Myce zostanie zainwestowany: Polar Heads Tak4- Poszliby do jądra, podczas gdy ich gazowane ogony byłyby narażone na ropę.
Nieruchomości
Nazwy
- Dodeklosulfate sodu (SDS).
- Laurilsulfate sodu (SLS).
Formuła molekularna
C12H25ALBO4Sna.
Masa cząsteczkowa
288 378 g/mol.
Opis fizyczny
Kilka prezentacji: suchy kurz, ciekł lub wilgotny stał. Jego kryształy mają białe lub kremowe zabarwienie.
Zapach
Ojciec zapach substancji tłuszczowych, toalety.
Temperatura topnienia
206 ° C.
Rozpuszczalność wody
1 · 105 Mg/L. 1 g Rozpuszczony w 10 ml roztworu oparentowego.
Gęstość
1,01 g/cm3.
Stabilność
Jest stabilny w zalecanych warunkach przechowywania.
Rozkład
Po podgrzaniu do rozkładu emituje biały dym tlenku siarki i tlenku sodu.
Napięcie powierzchniowe
39,5 dynami/cm w 25 ° C.
Krytyczne stężenie molowe
Ma 8,2 mm w czystej wodzie w temperaturze 25 ° C.
Aplikacje
Habit i sprzątanie w domu
Siarczan dodecyl jest środkiem powierzchniowo czynnym stosowanym w wielu produktach, takich jak mydła toaletowe, kąpiele z pianki, kremy z brzytwy itp. Służy również do usuwania plam z trudności w usuwaniu, w czyszczeniu podłóg i łazienki, futrzane przedmioty kuchenne itp.
Może ci służyć: olej lub eter benzyny: formuła, struktura, zastosowaniaMedycyna weterynaryjna i ludzka
Jest używany jako środek odstraszający pchły i kleszcze, obecne u zwierząt. Jest również stosowany jako krem nawilżający w niektórych antybiotykach, do użytku doustnego lub miejscowego.
SDS jest drobnoustrojami przeciwko wirusom z owijaniem, takimi jak HIV, typy 1 i 2, oraz opryszczka prostego opryszczki (HSV-2). Działa również na wirusa bez owijania: brodawczaka, reowirusa, rotawirusa i polio. Jednak to użycie nie jest zatwierdzone.
Używanie SDS zostało zasugerowane jako prysznic pochwy, który zapewnia ochronę przed wirusem przenoszonym drogą płciową. Ponadto w przetwarzaniu mleka matki w celu wyeliminowania lub zmniejszenia możliwości przenoszenia HIV poprzez karmienie piersią.
Oprócz działania przeciwwirusowego SDS działa na bakterie patogenne i grzyby. SDS eliminuje oporność na leki i czynniki oporności seksualne z E. coli; i blokuje wzrost wielu dodatnich bakterii Gram.
W laboratorium
SDS wiąże się z białkami powodującymi ich denaturacja, zapewniając obciążenia ujemne i zmiana konformacyjna. Umożliwia to określenie jego masy cząsteczkowej poprzez elektroforeza w poliakryloamidu.
SDS jest również stosowany w przygotowaniu próbek tkanki mózgowej do zastosowania w mikroskopii optycznej. Jest również stosowany w przygotowaniu próbek krwi do liczby erytrocytów.
SDS stosuje się w oczyszczaniu kwasów nukleinowych, ze względu na ich zdolność do rozpuszczenia błon i ich hamujące działanie na aktywność enzymów Arnasa i DNAasa.
Ponadto SDS stosuje się w charakterystyce czwartorzędowych związków amonowych.
Dodatek do żywności
SDS jest używany jako emulgator i pogrubienie żywności. Poprawia stabilność i teksturę produktów upieczonych. Dodatkowo jest stosowany jako pomocniczy w suszonych produktach jajowych.
Może ci służyć: azotan cynku: struktura, właściwości, uzyskiwanie, użyciaPrzemysł
SDS jest stosowany w branży galwanoplastyki, szczególnie nikiel i cynku; jako emulgowanie i penetrującego lakieru i zmywacza malowania; w sformułowaniu materiałów wybuchowych ukształtowanych przez wtrysk; i w solidnych rakietach, takich jak pienowanie.
Ryzyko
SDS Stała ekspozycja może powodować rozrost skóry u świnek morskich. Królik i ludzie są mniej podatni na te obrażenia. Bezpośredni kontakt z SDS w stężeniu ≤ 20%, może powodować umiarkowane zapalenie i podrażnienie skóry.
Z drugiej strony przedłużająca się ekspozycja na SDS może wytwarzać zapalenie skóry, z oznakami zaczerwienienia, obrzęku i tworzenia się ampułki.
SDS może wytwarzać przez kontaktowe podrażnienie oka. Może być również bardzo reaktywny u niektórych osób i powodować podrażnienie inhalacji dróg oddechowych i niewydolności oddechowej.
Rzadko spożycie SDS może powodować zmiany żrące. Ale zgłoszono go u dzieci, które spożywały SDS, obfite wymioty szybkiego rozwoju, depresji OUN i niewydolności oddechowej.
Nie stwierdzono dowodów genotoksyczności lub działania teratogennego w SDS. U 242 pacjentów z wypryskanym zapaleniem skóry stwierdzono 6,4 % pacjentów z alergią, w których można zastosować stosowanie SDS.
Bibliografia
- Dane strukturalne z L. DO. Smith, r. B. Hammond, k. J. Roberts, zm. Machin, g. McLeod (2000). Określenie kryształowego strumienia bezwodnego dodecylulfanu sodu przy użyciu kombinacji dyfrakcji proszku proszku i modelowania mochrotronowego. Journal of Molecular Structure 554 (2-3): 173-182. Doi: 10.1016/s0022-2860 (00) 00666-9.
- Wikipedia. (2019). Siarczan dodecylu sodu. Źródło: w:.Wikipedia.org
- National Center for Biotechnology Information. (2019). Siarczan dodecylu sodu. Baza danych Pubchem. CID = 3423265. Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov
- Hammouda b. (2013). Wpływ temperatury na nanostrukturę miceli SDS w wodzie. Journal of Research of National Institute of Standards and Technology, 118, 151-167. Doi: 10.6028/JRES.118.008
- Elsevier. (2019). Siarczan dodecylu sodu. Nauka bezpośredni. Pobrano z: Scientedirect.com
- Kumar, s., TheJajeenuo, j. K. i Tsipila, t. (2014). Toksykologiczne działanie dodecylulfan sodu. Journal of Chemical and Pharmaceutical Research 6 (5): 1488 - 1492.
- Sieć danych toksykologii. (S.F.). Laurylosulfan sodu. Toxnet. Odzyskane z: toksnet.NLM.Nih.Gov
- « Struktura trzeciorzędowa głównych cech cech
- Struktura fosfatydilseryny, synteza, funkcje, lokalizacja »

