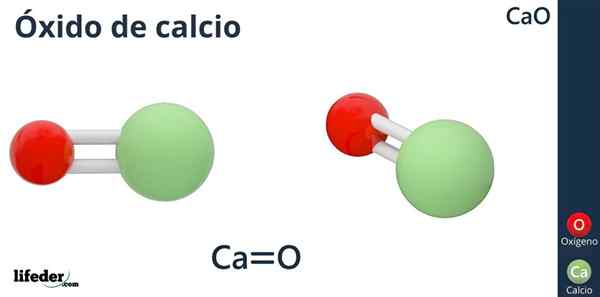
Tlenek wapnia (CAO)
- 5056
- 780
- Bertrand Zawadzki
Co to jest tlenek wapnia?
On tlenek wapnia (CaO) jest związek nieorganiczny, który zawiera wapń i tlen w postaciach jonowych (nie w celu pomylenia z nadtlenkiem wapnia, Cao2). Światowe znane jako wapno, słowo, które wyznacza każdy związek nieorganiczny, który zawiera węglany, tlenki i wodorotlenki wapnia, oprócz innych metali, takich jak krzemion, aluminium i żelazo.
Do tego tlenku (lub wapna) również powołuje się na życie lub wapno, w zależności od tego, czy jest on nawodniony. Żywe wapno to tlenek wapnia, a wapno jest jego wodorotlenkiem. Z kolei wapień (wapno lub hartowane wapno) jest w rzeczywistości skałą osadową złożoną głównie z węglanu wapnia (CACO3).
Jest to jedno z największych naturalnych źródeł wapnia i stanowi surowiec do produkcji tlenku wapnia. Jak powstaje ten tlenek? Węglany są podatne na rozkład termiczny; Podgrzewanie węglanów wapnia w temperaturach większych niż 825 ° C, prowadzi do tworzenia wapna i dwutlenku węgla.
Poprzednie stwierdzenie można opisać w następujący sposób: CACO3(s) → Cao (s) + co2(G). Ponieważ skorupa Ziemi jest bogata w wapień i kalcyt, aw oceanach i plażach skorupy morskie (surowce do produkcji tlenku wapnia) są obfite, a tlenek wapnia jest stosunkowo tani odczynnikiem.
Formuła
Chemiczna wzór tlenku wapnia to CaO, w którym wapń jest jak jon kwasowy (akceptor elektronów) CA2+, i tlen, taki jak podstawowy jon (dawca elektronów) lub2--.
Dlaczego wapń ma ładunek +2? Ponieważ wapń należy do grupy 2 tabeli okresowej (SR. Scholambara) i ma tylko dwa elektronach walencyjnych do tworzenia linków, co daje atom tlenu.
Może ci podać: tlenek potasu (K2O)Struktura tlenku wapnia
 Krystaliczna struktura tlenku wapnia
Krystaliczna struktura tlenku wapnia Struktura krystaliczna (typ soli klejnot) dla tlenku wapnia jest reprezentowana na górnym obrazie. Obszerne czerwone kule odpowiadają jonom CA2+ i białe kule do jonów lub2-.
W tym sześciennym układzie krystalicznym każde jon ca2+ jest otoczony sześcioma jonami lub2-, Ochodźcie w oktaedrycznych otworach pozostawionych wśród nich dużych jonów.
Struktura ta wyraża maksymalny charakter jonowy tego tlenku, chociaż niezwykła różnica w radiotelefonach (czerwona kula jest większa niż biała) daje słabszą energię krystaliczną siatkową, jeśli w porównaniu z MGO.
Właściwości tlenku wapnia
 Wygląd tlenku wapnia
Wygląd tlenku wapnia Fizycznie jest to krystaliczna biała stała, toaleta i silne interakcje elektrostatyczne, które są odpowiedzialne za ich wysokie punkty połączenia (2572 ° C) i gotowanie (2850 ° C). Ponadto ma masę cząsteczkową 55 958 g/mol i interesującą właściwość termoluminescencyjnego.
Oznacza to, że kawałek tlenku wapnia narażonego na płomień może świecić intensywnym białym światłem, znanym w języku angielskim z nazwą ŚWIATŁO WAPIENNE, lub po hiszpańsku światło wapnia. Jony ca2+, W kontakcie z ogniem pochodzą z czerwonawego płomienia, jak widać na następującym obrazie.
 Światło wapnia lub światło reflektorów
Światło wapnia lub światło reflektorów Rozpuszczalność
CAO to podstawowy tlenek, który ma silne powinowactwo do wody, w takim stopniu, który pochłania wilgoć (jest higroskopową substancją stałą), natychmiast reagując, aby uzyskać wyłączenie lub wodorotlenek wapnia:
Cao (y) + h2Lub (l) => ca (OH)2(S)
Ta reakcja jest egzotermiczna (porzuca ciepło) ze względu na tworzenie stałego z silniejszymi interakcjami i bardziej stabilną siecią krystaliczną. Jednak reakcja jest odwracalna, jeśli CA (OH) jest podgrzewany2, odwodnianie i oświetlenie wapna; Następnie wapno „odrodzone”.
Może ci służyć: safranina: charakterystyka, stosowanie, techniki, toksycznośćPowstały roztwór jest bardzo podstawowy, a jeśli jest nasycony tlenek wapnia, osiąga pH 12,8.
Podobnie jest rozpuszczalny w glicerolu oraz w kwasach i słodkich roztworach. Podobnie jak tlenek podstawowy, naturalnie ma skuteczne interakcje z tlenkami kwasu (SIO2, Do2ALBO3 i wiara2ALBO3, na przykład) bycie rozpuszczalnym w ich ciekłych fazach. Z drugiej strony jest nierozpuszczalny w organicznych alkohole i rozpuszczalnikach.
Używa/aplikacje
CAO ma ogromne niezliczone zastosowania przemysłowe, a także w syntezie acetylenu (CHrag), w ekstrakcji fosforanów ścieków oraz w reakcji z dwutlenkiem siarki napojów bezczelnych.
Inne zastosowania tlenku wapnia opisano poniżej:
Jako moździerz
Jeśli tlenek wapnia jest mieszany z piaskiem (SIO2) i woda, ciastka piaskiem i reaguje powoli z wodą, tworząc matowe wapno. Z kolei co2 Z powietrza rozpuszcza się w wodzie i reaguje z sól, tworząc węglan wapnia:
CA (OH)2(s) + co2(g) => caco3(s) + h2Lub (l)
Kako3 Jest to bardziej odporny i twardy związek niż CaO, powodujący stwardnienie zaprawy (poprzednia mieszanina) i naprawianie cegieł, bloków lub ceramiki między nimi lub na pożądaną powierzchnię.
W produkcji szkła
Podstawowym surowcem do produkcji szkła są tlenki krzemowe, które są mieszane z wapnem, węglanem sodu (na2WSPÓŁ3) i inne dodatki, a następnie poddane ociepleniu, co skutkuje szklistymi ciałami. Ta substancja stała jest następnie ogrzewana i wysadzona w dowolne figurki.
W górnictwie
Tępe wapno zajmuje większą objętość niż żywe wapno z powodu interakcji przez mosty wodorowe (O-H-O). Ta właściwość jest wykorzystywana do zerwania skał z jej uznania.
Może ci służyć: katalityczne uwodornienieOsiąga się to poprzez wypełnienie ich zwartą mieszanką wapna i wody, która jest uszczelniona w celu skupienia ciepła i ekspansywnej mocy w skale.
Jak krzemem agenta zmywacza
CAO łączy się z krzemianami, tworząc ciecz koalescyjną, która jest następnie wydobywana z surowca z określonego produktu.
Na przykład minerały żelaza są surowcem do produkcji metalicznego żelaza i stali. Te minerały zawierają krzemiany, które są niepożądanymi zanieczyszczeniami dla procesu i są eliminowane przez niedawno opisaną metodę.
Nanocząstki tlenku wapnia
Tlenek wapnia może być syntetyzowany jako nanocząstki, zmieniające stężenie azotanu wapnia (CA (NO (NO3)2) i wodorotlenek sodu (NaOH) w roztworze.
Cząstki te są sferyczne, podstawowe (a także skala stała do makro) i mają dużo powierzchni powierzchniowej. W konsekwencji te właściwości korzystają procesy katalityczne. Który? Dochodzenia obecnie odpowiadają na to pytanie.
Te nanocząstki zostały wykorzystane do syntezy podstawionych związków organicznych - wynikających z pirydyny - w preparacie nowych leków do przeprowadzania transformacji chemicznych, takich jak sztuczna fotosynteza, do oczyszczania wody z ciężkich i szkodliwych metali oraz jako środki fotokatalityczne.
Nanocząstki można zsyntetyzować na wsparcie biologiczne, takie jak liście papai i zielonej herbaty, aby wykorzystać je jako środek przeciwbakteryjny.
Bibliografia
- Scifun.org. (2018). Wapno: tlenek wapnia. Odzyskany z: Scifun.org.
- Wikipedia. (2018). Tlenek wapnia. Źródło: w:.Wikipedia.org
- Pubchem. (2018). Tlenek wapnia. Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov
- Shiver & Atkins. (2008). Chemia nieorganiczna. W Elementy grupy 2. (czwarta edycja., P. 280). MC Graw Hill.