TRIOROLENEK Arsenowy (AS2O3)
- 3824
- 76
- Filip Augustyn
On TRIOROKEK Arsenowy Jest to związek nieorganiczny, którego wzór chemiczny jest tak2ALBO3. Arsen w swoim stanie metalicznym jest szybko przekształcany w ten tlenek, który jest bardzo toksyczną trucizną, która może mieć ostre i przewlekłe objawy.
Będąc elementami arsenu i tlenu bloku P, o stosunkowo niskiej różnicy elektroonegatywności, ACE jest oczekiwane2ALBO3 składać się z kowalencyjnej natury; to znaczy, że wiązania As-O dominują w ich stałym, na elektrostatycznych interakcjach między jonami ACE3+ I2-.
Ostre zatrucie tritlekiem arsenu jest wytwarzane przez spożycie lub wdychanie, będąc najważniejszym objawami tego: silne zaburzenia przewodu pokarmowego, skurcze, zapadnięcie się krążenia i obrzęk płuc.
Jednak pomimo swojej toksyczności był używany przemysłowo; Na przykład w ochronie drewna, w opracowaniu pigmentów, półprzewodników itp. Podobnie był wcześniej stosowany w leczeniu licznych chorób.
TRIOTOLENEK ARSENIA JEST Związkiem Amfoterycznym, rozpuszczalnym w kwasach i rozcieńczonej alkalii, nierozpuszczalnym w rozpuszczalnikach organicznych i stosunkowo rozpuszczalny w wodzie. Jest przedstawiony jako stały (obraz górny), z dwiema krystalicznymi formami: sześcienne i monokliniczne.
Struktura trójtlenku arsenu
Claudetita
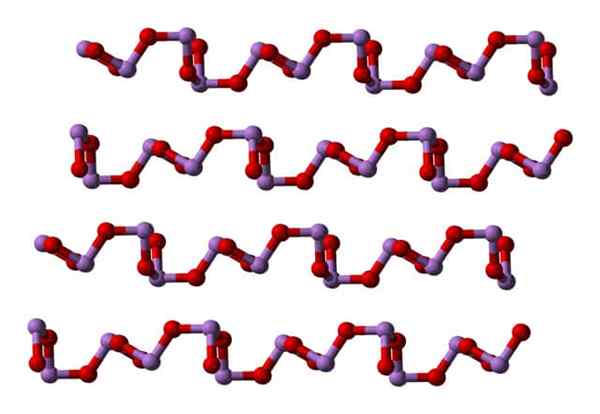
W temperaturze pokojowej as2ALBO3 Krystalizuje w dwóch monoklinicznych polimorfach, oba znalezione w minerałach Claudetita. W nich są trygonalne piramidy aso3, które wiążą się z ich atomami tlenu w celu zrekompensowania samego niedoboru elektronicznego urządzenia.
W polimorfie jednostki ASO3 Są one powiązane z wierszami (Claudetita I), a w drugim są one powiązane tak, jakby produkowali sieć (Claudetita II):
Może ci służyć: materiały aglomerantowe Claudetita Polymorfo Struktura I. Źródło: Ben Mills [domena publiczna].
Claudetita Polymorfo Struktura I. Źródło: Ben Mills [domena publiczna].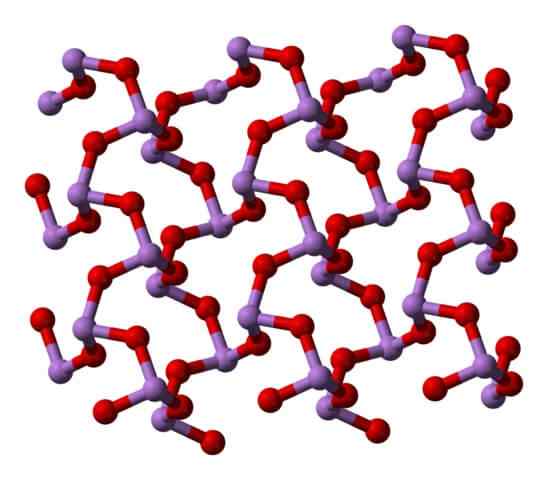 Claudetita Polymorfo Struktura II. Źródło: Ben Mills [domena publiczna].
Claudetita Polymorfo Struktura II. Źródło: Ben Mills [domena publiczna].
Ciekł i gazowy
Kiedy wszystkie te struktury definiujące kryształy monokliniczne są podgrzewane, wibracje są takie, że kilka linków AS-O jest zepsutych, a kończy się mniejszą cząsteczką:4ALBO6. Na dolnym obrazie pokazano jego strukturę.
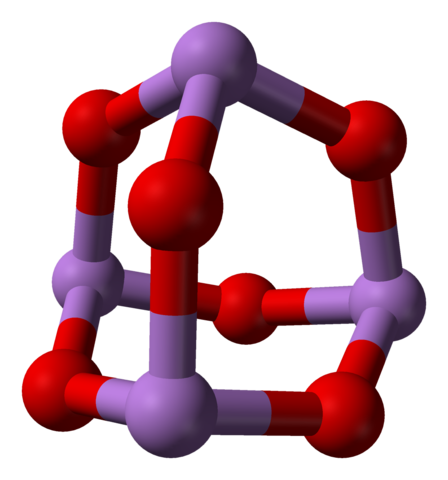 Cząsteczka AS4O6. Źródło: Ben Mills [domena publiczna]
Cząsteczka AS4O6. Źródło: Ben Mills [domena publiczna] Można powiedzieć, że składa się z dnia2ALBO3. Jego stabilność jest taka, że obsługuje 800 ° C w fazie gazowej; Ale powyżej tej temperatury jest fragmentaryczna jako cząsteczki2ALBO3.
Arsenolit
Taki sam jak4ALBO6 może wchodzić w interakcje ze sobą, aby krystalizować w sześciennym substancji stałej, której struktura znajduje się w minerałach arsenolitowych.
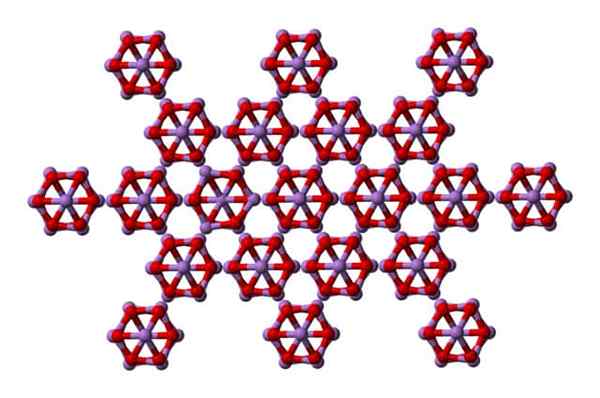 Cząsteczki AS4O6 w stałym arsenolicie. Źródło: Ben Mills [domena publiczna]
Cząsteczki AS4O6 w stałym arsenolicie. Źródło: Ben Mills [domena publiczna] Zauważ, że na obrazie struktura jest wyświetlana z wyższej płaszczyzny. W porównaniu do Claudetita widoczna jest jej różnica strukturalna w stosunku do arsenolitu. Tutaj są dyskretnymi cząsteczkami4ALBO6 że jednostki są utrzymywane przez siły van der Waalsa.
Nieruchomości
Tradenames
-Arsenolit
-Arsodent
-Trisenox
-Claudetita
Waga molekularna
197,84 g/mol.
Wygląd fizyczny
-Białe kryształy sześcienne (arsenolit).
-Monokliniczne bezbarwne kryształy (Claudetita).
-Białe lub przezroczyste stałe, szkliste, amorficzne grudki lub krystaliczny kurz.
Zapach
Toaleta.
Smak
Bez smaku.
Punkt wrzenia
460 ° C.
Temperatura topnienia
-313 ° C (Claudetita).
-274 ° C (arsenolit).
punkt zapłonu
485 ° C (Sublima).
Rozpuszczalność wody
17 g/l A 18 ° C (20 g/l A 25 ºC).
Rozpuszczalność
Kwas rozpuszczalny (szczególnie w kwasie solnym) i alkalii. Praktycznie nierozpuszczalne w chloroformu i eterze.
Może ci służyć: wirowanieGęstość
-3,85 g/cm3 (kryształy sześcienne);
-4,15 g/cm3 (kryształy rombowe).
Ciśnienie pary
2,47 · 10-4 MMHG w 25 ° C.
Rozkład
To nie jest paliwo, ale z powodu ocieplenia może powodować toksyczny dym, który może obejmować Arsinę.
Korozja
W obecności wilgoci może być żrący dla metali.
Ciepło parowe
77 kJ/mol.
Stała dysocjacji (KA)
1,1 · 10-4 w 25 ° C.
Współczynnik załamania światła
-1755 (arsenolit)
-1.92-2.01 (Claudetita).
Reaktywność
-TRIOTLENEKIE ARSENIKU jest związkiem amfoterycznym, ale działa najlepiej jako kwas.
-Może reagować z kwasem solnym lub kwasem fluorhorycznym, tworząc triflouride arsenowe lub triflouriur arsenowy.
-Reaguje również z silnymi utleniaczami, takimi jak kwas azotowy, powodując kwas arsenowy i podtlenek azotu.
-TRIOTLENEKID ARSENIKU może reagować z kwasem azotowym, wytwarzającym arsynę lub element arsenowy, w zależności od warunków reakcji.
As2ALBO3 + 6 Zn +12 HNO3 => 2 popiół3 + 6 Zn (nie3)2 + 3 godz2ALBO.
Ta reakcja służyła jako podstawa do stworzenia testu bagiennego, zastosowanego do wykrywania zatrucia arsenu.
Nomenklatura
Na 2ALBO3 Można go wyznaczyć zgodnie z następującymi nomenklatury, wiedząc, że arsen współpracuje z Walencją +3:
-Tlenek arsenioso (tradycyjna nomenklatura).
-Tlenek arsenu (iii) (nomenklatura zapasowa).
-TRIOTOLENEK DIARSENIKU (NOMENKLUARZA SYSTEMATYCZNA).
Aplikacje
Przemysłowcy
-Jest stosowany w produkcji szkła, szczególnie jako środek zanikający. Jest również stosowany w opracowaniu ceramiki, produktów elektronicznych i fajerwerków.
-Jest dodawany jako niewielki składnik stopów opartych na miedzi, aby zwiększyć odporność na korozję metali stopowych.
-As2ALBO3 Jest to materiał wyjściowy do przygotowania elementarnego arsenu, poprawy stawów elektrycznych i do opracowania półprzewodników Arsenuros
Może ci służyć: chemia nuklearna: historia, dziedzina studiów, obszary, zastosowania-As2ALBO3, Oprócz arseniko miedzi, są one używane jako drewniane konserwatywy. Zastosowano go w połączeniu z octanem miedzianym do opracowania zielonego pigmentu Paryża, stosowanego w opracowaniu obrazów i raticides.
Lekarze
-TRIOTLENEKIKA ARSENIA JEST ZNIKUSUJĄCEM UTYCZNYM STAWIENIE SIĘ SIĘ W LECZENIU LIKE. Zastosowano go jako tonik w leczeniu zaburzeń żywieniowych, neuralgii, reumatyzmu, zapalenia stawów, astmy, Korei, malarii, kiły i gruźlicy.
-Podobnie był stosowany w miejscowym leczeniu chorób skóry, stosowany do zniszczenia niektórych powierzchniowych nabłonków.
-Roztwór Fowlera zastosowano w leczeniu chorób skóry i białaczki. Zastosowanie tego leku jest przerwane.
-W latach siedemdziesiątych chiński badacz Zhang Tingdong opracował badanie na temat zastosowania trójtlenku arsenu w leczeniu ostrej białaczki promielocytowej (APL). Co doprowadziło do produkcji leku Trisenox, który został zatwierdzony przez FDA Stanów Zjednoczonych.
-Trisenox był stosowany u pacjentów z PLA, którzy nie reagują na leczenie „pierwszej linii”, składającej się z całego kwasu przez kwas kwasowy (ATTRA). Umawiano, że trójtlenek arsenu indukuje komórki rakowe cierpieć apoptozę.
-Trisenox jest stosowany jako cytostatyczny w leczeniu opornego podtypu promiselocytowego (M3) aplikacji.
Bibliografia
- TRIOROKEK Arsenowy. Sevier. Pobrano z: Scientedirect.com
- Tlenek arsenu (iii). Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov

