Skład roztworów krystalicznych, typy i przykłady
- 3500
- 1085
- Matylda Duda
Rozwiązania krystaloidalne Są to te utworzone przez rozpuszczanie elektrolitu i innych małych cząsteczek rozpuszczalnych w wodzie, stosowanych w rutynowych procedurach klinicznych, takich jak dostosowanie objętości płynu układu krążenia. W prostych terminach chemicznych: rozwiązania te są niczym więcej niż wodnymi i rozcieńczonymi roztworami wydobywczymi.
Roztwory krystaloidowe odgrywają ważną rolę w terapiach klinicznych, takich jak infuzje dożylne płyny w przypadku krwotoku, odwodnienia, hipowolemii i infekcji. Zwykle jego stężenie soli fizjologicznej jest izotoniczne, co oznacza, że liczba jego rozpuszczonych jonów jest porównywalna z stężeniem w osoczu krwi.
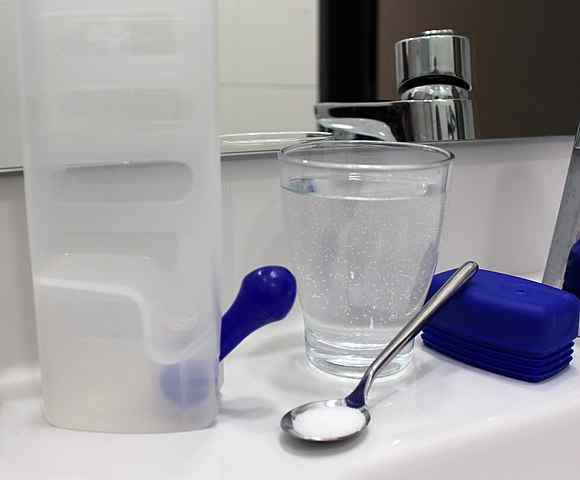
 Roztwór krystaliczny można przygotować po prostu przez rozpuszczenie soli i innych substancji rozpuszczonych w wodzie w umiarkowanym stężeniu. Źródło: Rillke/CC BY-SA (https: // creativeCommons.Org/licencje/by-sa/3.0)
Roztwór krystaliczny można przygotować po prostu przez rozpuszczenie soli i innych substancji rozpuszczonych w wodzie w umiarkowanym stężeniu. Źródło: Rillke/CC BY-SA (https: // creativeCommons.Org/licencje/by-sa/3.0) Roztwory krystaloidowe nie powodują zatem zmian osmotycznych, ale zapewniają odpowiednią objętość cieczy, aby krew nadal nawadniała przez układ krążenia. W ten sposób osiąga się, że serce pompuje rozcieńczoną krew i może dostarczać tlen do tkanek.
Przykładem roztworu krystaloidowego jest normalny roztwór soli fizjologicznej, który zawiera NaCl w stężeniu 0,9%. Jednak w zależności od przypadku klinicznego można wybrać inne roztwory, z różnymi składnikami, stężeniami i rodzajami toniczności.
[TOC]
Skład roztworów krystaloidowych
Wszystkie roztwory krystaloidowe oparte są na sterylizowanych lub bezpłatnych mikroorganizmach, więc jest to jego ulubiony rozpuszczalnik. W przeciwnym razie nie mogliby zintegrować zdrowia z naszym ciałem i spowodować jakąkolwiek niepożądaną reakcję. Jako rozwiązanie lub rozwiązanie, ma również substancje rozpuszczone, które w istocie są solami mineralnymi lub silnymi elektrolitami.
Sprzedaż może być kilka, o ile przyczyniają się do umiarkowanych koncentracji, jony NA+, AC2+, K+ i Cl-. Oprócz soli nieorganicznych, mogą one również mieć bardzo rozpuszczalne organiczne substancje rozpuszczone w wodzie, takie jak octany, glukoniany i mleczan. Ponadto niektóre z tych roztworów zawierają glukozę (dekstroza).
Może ci służyć: hydroksyapatytStężenia tych soli lub substancji rozpuszczonych są bardzo zróżnicowane i są wyrażane albo w wartościach procentowych, miligram przez decylitarów (mg/dl), molowości lub osmolarności. Wybór jednego lub drugiego będzie zależeć od kryteriów klinicznych.
Chłopaki
Na początku powiedziano, że roztwory krystaliczne są często stosowane w celu zapewnienia objętości cieczy dla układu krążenia. W tym procesie, w zależności od jego toniczności, w osoczu krwi cierpi lub niezmienne zmiany, które promują lub faworyzują niektóre pożądane stany u pacjenta.
Zatem jedyną rzeczą, która odróżnia roztwór krystaliczny od drugiego, nie jest chemiczny charakter jego substancji rozpuszczonej, ale jej toniczność; to znaczy, jeśli jest to roztwór hipertoniczny, izotoniczny lub hipotoniczny.
Hipertoniczny
Hipertoniczny roztwór krystaloidowy to ten, którego stężenie soli fizjologicznej jest lepsze niż w osoczu krwawym. Dlatego woda migruje z wnętrza komórek do osocza, która zwiększyła jej toniczność z powodu obecności hipertonicznego roztworu krystaloidowego. Przykładem tego typu roztworu jest 3% NaCl, w szczególności bardziej skoncentrowane niż 0,9% normalny roztwór soli fizjologicznej.
Rozwiązania te są przeciwwskazane w większości przypadków klinicznych, z wyjątkiem tych, którzy przedstawiają następujące następstwa neurologiczne.
Izotoniczny
Izotoniczny roztwór krystaloidowy to ten, którego stężenie soli fizjologicznej jest porównywalne lub identyczne z stężeniem w osoczu krwi i stężenie wnętrza komórkowego. Dlatego nie ma wymiany wody między dwoma mediami. Przykładem tego typu rozwiązania jest 0,9%NaCl, już wspomniane powyżej.
Hipotoniczne
I wreszcie, hipotoniczny roztwór krystaloidowy to ten, którego stężenie soli fizjologicznej jest niższe niż w osoczu krwi i przedziału wewnątrzkomórkowego lub przestrzeni. Tym razem woda porusza się do wnętrza komórki, aż do osiągnięcia równowagi. Przykładem tego typu rozwiązania jest 0,45% NaCl.
Może ci służyć: metale alkalicznePodobnie jak w przypadku hipertonicznych roztworów krystaloidowych, hipotoniczne są przeciwwskazane w większości przypadków klinicznych, szczególnie w przypadku tych, w których istnieje ryzyko obrzęku mózgu.
Przykłady roztworów krystalicznych
Niektóre przykłady roztworów krystalicznych zostaną wymienione i opisane poniżej. Różnica między jednym a drugim będzie polegać na tożsamości jego elektrolitów lub rozpuszczonych soli.
Normalny roztwór soli fizjologicznej
Normalny roztwór soli fizjologicznej ma skład 0,9%NaCl, jest izotoniczny i jest również najbardziej nawracającym roztworem krystaloidowym, ponieważ służy do leczenia nieskończoności wspólnych przypadków odwodnienia; takie jak te spowodowane przez biegunkę, wstrząs, wymioty, krwawienie, między innymi. Unika się jednak u pacjentów z problemami z nerkami lub problemami sercowymi.
Roztwór mleczanowy
Znany również jako roztwór Ringer lub Hartmann (chociaż różnią się nieznacznie stężeniami jonowymi), jest to taka, która składa się z mieszaniny chlorku sodu, mleczanu sodu, chlorku wapnia i chlorku potasu.
Jego skład soli fizjologicznej jest tym, który przypomina skład w osoczu krwi, więc jest to typ izotoniczny. Jest stosowany jako płyn regulatorowy lub płyn do przypadków oparzeń, urazów, nierównowagi elektrolitycznej, kwasicy metabolicznej. Jest to jednak przeciwwskazane u pacjentów cierpiących na hiperkalcemiię.
Mleczan jest metabolizowany w naszym ciele i kończy się przekształceniem w wodorowęglan. Ten roztwór może również zawierać anion glukonianowy, a także pewne ilości magnezu, mg2+.
Roztwór glukozy
Znany również jako roztwór krystaloidowy dekstrozy, występuje w dwóch stężeniach: odpowiednio 5 i 10% (odpowiednio D5 lub D10). Jest to początkowo hipotoniczne, ale jest przekształcane w izotonikę po wchłanianiu glukozy, zapewniając wodę nerkom. Chociaż zapewnia znaczną ilość kalorii, jest przeciwwskazany u pacjentów cierpiących na hiperglikemię.
Może ci służyć: kwas elagiczny: struktura, właściwości, uzyskanie, lokalizacja, zastosowaniaW przeciwieństwie do innych roztworów krystalicznych, są one słodkie. Najsłodsze mają stężenia większe niż 10% (D20, D30, D50 itp.) I są przeznaczone dla pacjentów z obrzękiem płuc i mózgu. Z drugiej strony zmniejszają katabolizm białkowy, chronią wątrobę i pomagają w walce z upadkami krążenia.
Hipertoniczne i hipotoniczne roztwory soli fizjologicznej
Hipertoniczne roztwory soli fizjologicznej (3 i 5% NaCl) są wykorzystywane do dostarczania płynności pacjentom z płonącego, indukowania hiperosmolarności i złagodzenia bezdokładności nerek. Z drugiej strony, hipotoniczne roztwory soli fizjologicznej (0,45% NaCl lub niższe stężenie), kontrolują hipernatremiię i są przeciwwskazane u płonących pacjentów.
Dlatego jeden dostarcza skutki sprzeczne z drugim; Gdy roztwór hipertoniczny jest niezbędny, hipotonika jest odrzucana i odwrotnie.
Mechanizm wszystkich roztworów krystaloidowych opiera się na równowadze osmotycznej i wodnej między płynami wewnątrz i płynami zewnątrzkomórkowymi.
Bibliografia
- Lewis Sr i in. (3 sierpnia 2018 r.). Koloidy lub krystaloidy do wymiany płynów u krytycznie ludzi. Współpraca Cochrane. Odzyskane z: Cochrane.org
- Epstein em, Waseem m. (29 listopada 2019). Płyny krystaloidalne. W: StatPearls. Treasure Island (FL): StatPearls Publishing 2020 -. Odzyskane z: NCBI.NLM.Nih.Gov
- Wikipedia. (2020). Ekspander objętościowy. Źródło: w:.Wikipedia.org
- Elsevier b.V. (2020). Krystaloid. Scientedirect. Pobrano z: Scientedirect.com
- Sheila Bouie. (2020). Krystaloidy: definicja i przykład. Badanie. Odzyskane z: Study.com

