Obiecana (PM) struktura, właściwości, uzyskiwanie, zastosowania

- 3862
- 752
- Estera Wojtkowiak
On Obiecane Jest to element chemiczny, który należy do klasy Lantanids. Jest identyfikowany z symbolem PM, a jego liczba atomowa wynosi 61. Jest to radioaktywne metaliczne stałe i jest najbardziej niestabilnym elementem pierwszych 84 elementów stolika okresowego.
Ten element jest naturalnie występujący w bardzo niskich stężeniach (około 4 x 10-piętnaście gramy na kg) w rodzaju uraninitów, który jest minerałem uranu, w którym obiecane występują ze względu na spontaniczne rozszczepienie uranu-238.
 Symbol, liczba atomowa i masa atomowa obietnicy. Źródło: ME/CC BY-S (https: // creativeCommons.ORG/Licencje/BY-SA/2.5). Źródło: Wikimedia Commons.
Symbol, liczba atomowa i masa atomowa obietnicy. Źródło: ME/CC BY-S (https: // creativeCommons.ORG/Licencje/BY-SA/2.5). Źródło: Wikimedia Commons. Pomimo braku skorupy ziemskiej, został wykryty w spektrum gwiazdy HR465 konstelacji Andromeda, na której powierzchni szacuje się, że ostatnio tworzy się, ponieważ żaden izotop PM nie ma dłuższego półfinansowania 17, 7 lat.
Było to przydatne w obiektach, które świecą w ciemności, ale ze względu na ich radioaktywność, której zatrzymał się w nich. Służy do pomiaru grubości materiału i baterii energii jądrowej.
[TOC]
Odkrycie
Istnienie Prometio było podejrzewane w 1902 r. Przez chemika czeskiego bohuslava Braunera. Później, w 1914 r., Angielski fizyk Henry Moseley stwierdził w swoich badania.
Następnie, chociaż kilka grup badaczy (Włosi w 1924 r., Amerykanie w 1926 i 1938 r.) Ogłosło swoje odkrycie, trudność oddzielenia go od innych elementów i odtworzenia doświadczeń sprawiła.
 Jacob a. Marinsky. Domena ornl / pub. Źródło: Wikimedia Commons.
Jacob a. Marinsky. Domena ornl / pub. Źródło: Wikimedia Commons. Wreszcie w 1944 r. Naukowcy Marinsky J.DO., Glendenin L.I. i Coryell c.D. Testowali swoją obecność i wyizolowali ją z produktów rozszczepienia uranu w reaktorze jądrowym Clinton Laboratories w Oak Ridge w Tennessee w Stanach Zjednoczonych.
 Larry e. Glendenin. Domena ornl / pub. Źródło: Wikimedia Commons.
Larry e. Glendenin. Domena ornl / pub. Źródło: Wikimedia Commons. Jednak nie zgłosili priorytetu w odkryciu do 1946 r. Za to, że zostali w pełni poświęcone tajnym dochodzeniu związanym z działaniami obronnymi podczas II wojny światowej.
Przypisanie nazwy
Chociaż naukowcy zaproponowali go nazwanie go „Clintonem” na cześć laboratoriów, w których pracowali, żona Coryella przekonała ich, aby nazwali go „obiecaną” jako wspomnienie greckiego Tytana Prometeusza lub Prometeusza.
 Charles D. Coryell. Autor zdjęcia: Christian A. Coryell/gfdl (http: // www.gnu antylopa.Org/copyleft/fdl.html). Źródło: Wikimedia Commons.
Charles D. Coryell. Autor zdjęcia: Christian A. Coryell/gfdl (http: // www.gnu antylopa.Org/copyleft/fdl.html). Źródło: Wikimedia Commons. Według niektórych interpretacji mitologii greckiej Prometeusz ukradł ogień bogów, aby dać go ludzkości, więc został okrutnie ukarany za całą wieczność. Inne legendy mówią, że zapewniło ludziom matematykę, naukę, rolnictwo i medycynę, a nawet stworzył człowieka.
Może ci służyć: równanie Clausius-clapeyron: po co to jest przykłady, ćwiczenia Reprezentacja Prometeusza przez niemieckiego rzeźbiarza. © El Grafo / CC-BY-SA-4.Domena 0 / pub. Źródło: Wikimedia Commons.
Reprezentacja Prometeusza przez niemieckiego rzeźbiarza. © El Grafo / CC-BY-SA-4.Domena 0 / pub. Źródło: Wikimedia Commons. Te wątpliwości co do tego, jaki był wkład Prometeusza w ludzkość, przypomina niepewność co do tego, kto odkrył ten element. Z drugiej strony, według żony Coryella, nazwa była uzasadniona, ponieważ naukowcy „ukradli ogień bogów” podczas odkrywania go podczas programu tajnego bomb atomowego.
Struktura elektroniczna
Konfiguracja elektroniczna tego elementu to:
1S2; 2S2 2P6; 3S2 3P6 3D10; 4S2 4P6 4D10; 5S2 5P6; 4F5 6S2;
które można również wyrazić jako:
[Xe] 4F5 6S2.
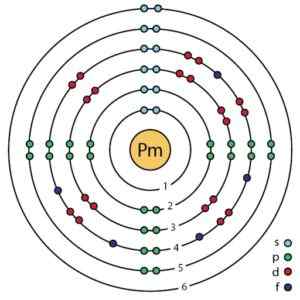 Struktura elektroniczna Prometio według ulepszonego modelu atomowego Bohra. Hazard.ScienceWriter/CC BY-SA (https: // creativeCommons.Org/licencje/nabrzeże/4.0). Źródło: Wikimedia Commons.
Struktura elektroniczna Prometio według ulepszonego modelu atomowego Bohra. Hazard.ScienceWriter/CC BY-SA (https: // creativeCommons.Org/licencje/nabrzeże/4.0). Źródło: Wikimedia Commons. Nomenklatura
- Obiecany, symbol PM.
- Prometio-147, PM-147 lub 147PM: Isotope del Prometio z masą atomową 147.
Właściwości Prometio
Stan fizyczny
Silone metaliczne stałe, sześciokątne kryształy.
Masa atomowa
144,91
Temperatura topnienia
1042 ºC
Punkt wrzenia
3000 ° C
Gęstość
7,26 g/cm3
Właściwości chemiczne
Należy do rodziny Lantanidów, Lantanoidów lub „Ziemi rzadkich”, zwanych tak, ponieważ w skorupie Ziemi zawsze są w postaci swoich tlenków. Są częścią 6 okresu okresowej tabeli elementów.
Według źródeł konsultowanych, PM, podobnie jak inne Lantanids, reaguje bezpośrednio z wodą, powoli zimno, szybko podczas podgrzewania, uwalniania wodoru (H2). Szybko przyciemnia w powietrzu i spala się łatwo wytwarzając tlenek.
Przygotowano ponad 30 związków Prometio, a większość z nich ma pewnego rodzaju zabarwienie. Jego stan utleniania w tych związkach wynosi +3. Nie tworzy tetravalentów.
Tworzenie niektórych związków
Rozpuszczenie go w kwasie solnym (HCl) Obiecane tworzy PMCL3 który jest żółty i rozpuszczalny w wodzie. W kwasie azotowym (HNO3) PM jest generowany (nie3)3 to jest różowe, a także rozpuszczalne w wodzie.
Jeśli rozwiązanie zawierające jony PM3+ jest alkalizowany z NH3, Oznacza to, że pH jest zwiększone, wytrąty wodorotlenkowe (PM (OH)3) jasnobrązowy.
Może ci służyć: link joniczny: Charakterystyka, sposób, w jaki jest tworzone i przykładySiarczan PM2(POŁUDNIOWY ZACHÓD4)3 Jest lekko rozpuszczalny w wodzie. Jeśli szczawian Prometio zostanie podgrzewany, staje się tlenek PM2ALBO3 biały lub lawenda.
Emisja radioaktywna
Emituje promieniowanie beta w postaci elektronów, które pozostawiają jądro ich atomów. Podczas wydawania go staje się elementem Samarium (SM). Z drugiej strony może stać się neodymem (ND), eliminując rdzeń pozytron i przechwytywanie elektronu w tym samym. PM nie emituje promieni gamma.
Izotopy
Do tej pory znanych jest 14 izotopów prometio, z masami atomowymi, które wynoszą od 134 do 155. Wszystkie są niestabilne (radioaktywne), co odróżnia go od innych Lantanides.
Prometio-147 jest tym, który ma największą użyteczność i ma okres półtrwania wynoszący 2,6 roku.
Izotop z większą półfinią
Najdłuższy izotop okresu półtrwania to Prometio-145 z 17,7 lat, który rozpada się przez schwytanie elektroniczne, które składa się z atomowego elektronu, jest łączone z protonem i tworzy neutron i neutrino.
Jest to jednak jedyny izotop PM, który może również cierpieć rozpad alfa (emisja 2 neutronów). Wynika to z faktu, że ma 84 neutrony, a wydanie 2 z nich sprawia, że jest to prometio-141 z 82 neutronami, co jest stabilną konfiguracją jądra. Ale jest to rodzaj rozpadu, który występuje bardzo niewiele.
Aktualne uzyskiwanie
W 1963 r. Przygotowano około 10 gramów Prometio przy użyciu metod chromatograficznych wymiany jonowej w odpadach paliwowych reaktora atomowego. Dziś wciąż wraca do zdrowia jako sole 147Po południu3+.
Według niektórych źródeł był on również przygotowywany w tych latach poprzez redukcję fluoru (PMF3) Z litową parą (Li). Jest również przygotowywany przez redukcję chlorków (PMCL3) Z wapniem (CA) w wysokich temperaturach.
Można go również uzyskać z neodymu-146. Izotop ten podlega bombardowaniu neutronami, aby każdy atom przechwytuje neutron i staje się neodymem-147. Ten ostatni trwa około 11 dni cierpiących na rozpad beta, przekształcając w ten sposób w Prometio-147.
Aplikacje
Izotop 147 (147PM) to ten, który był najbardziej używany, będąc jedynym, który można znaleźć komercyjnie. Nie emituje promieni gamma i jest dostarczany w postaci tlenku lub chlorków. Jednak ich transport i manipulacja wymagają ochrony przed promieniowaniem.
Może ci służyć: hydroliza: co to jest i przykłady reakcjiPosiadał niektóre zastosowania, których dziś nie ma, ponieważ jest obecnie używany w specjalnych aplikacjach.
W bateriach
Prometio-147 jest stosowany w długoterminowych akumulatorach atomowych. W tym przypadku małe kawałki PM są umieszczane w matrycy półprzewodnika w celu przekształcenia emisji beta w energię elektryczną.
Ten rodzaj akumulatorów energii jądrowej może zapewniać energię przez około 5 lat i były stosowane we wszystkich typach urządzeń, od pocisków po rozruszniki serca, które są urządzeniami umieszczonymi u pacjentów z problemami z sercem.
 Bugemakerzy mogą mieć długie baterie oparte na Prometio. Autor: 242799. Źródło: Pixabay.
Bugemakerzy mogą mieć długie baterie oparte na Prometio. Autor: 242799. Źródło: Pixabay. W zastosowaniach medycznych
Według niektórych źródeł tlenek Prometio jest stosowany w medycynie jako źródło promieniowania.
W przemyśle
Został użyty do pomiaru grubości niektórych materiałów, co odbywa się poprzez pomiar promieniowania beta, które przechodzi przez próbki.
Potencjalne aplikacje
Można go używać jako źródła do transportu x -sztabki, ale najwyraźniej ta aplikacja nie została jeszcze opracowana w handlu.
 Zdjęcie rentgenowskie uzyskane w 1963 r. Z małym urządzeniem (około 10 cm x 5 cm x 1 cm) zawierającego Prometio-147. Energia.Domena Gov / Pub. Źródło: Wikimedia Commons.
Zdjęcie rentgenowskie uzyskane w 1963 r. Z małym urządzeniem (około 10 cm x 5 cm x 1 cm) zawierającego Prometio-147. Energia.Domena Gov / Pub. Źródło: Wikimedia Commons. Służyłby również do zapewnienia energii do sond kosmicznych i satelitarnych lub tworzenie urządzeń, które umożliwiają komunikację z podwodnymi.
Przerwane zastosowanie w sygnałach lekkich
Początkowo Prometio-147 zastosowano do wymiany elementu radiowego w świetlistych tarczy, ponieważ dowiedział się, że radio było zbyt niebezpieczne. W tym celu PMCL była mieszana3 Z luminoforami, które świecą od zielonkawego żółtego do niebieskiego, gdy wpływa na nie promieniowanie obiecanych (cząsteczki beta).
 Kilka lat temu igły zegarków bransoletki można było zobaczyć w ciemności z powodu jasności spowodowanej radioaktywnością Prometio. Autor: Monakocannes. Źródło: Pixabay.
Kilka lat temu igły zegarków bransoletki można było zobaczyć w ciemności z powodu jasności spowodowanej radioaktywnością Prometio. Autor: Monakocannes. Źródło: Pixabay. Ta właściwość była używana w zegarkach lub tarczy bransoletki, aby zabłysnąć w ciemności. Również w guziku zapłonu niektórych lamp fluorescencyjnych. Ponadto nie uszkodziło luminoforów, jak ma to miejsce w przypadku innych źródeł promieniowania beta, przedłużając żywotność urządzeń.
Jednak kiedy odkryto, że obiecanie jest również niebezpieczne, jego użycie na rynku przedmiotów, które świecą w ciemności.
Ryzyko
PM jest elementem radioaktywnym, więc musi być manipulowany z ekstremalną ostrożnością i odpowiednią ochroną. Oprócz emitowanych cząstek beta, mogą one wpływać na elementy o głównej liczbie atomowej i generować x.
 Próbki Prometio muszą być transportowane w grubej osłonie ołowiu, aby uniknąć szkodliwych skutków promieniowania, które emitują. Energia.Domena Gov / Pub. Źródło: Wikimedia Commons.
Próbki Prometio muszą być transportowane w grubej osłonie ołowiu, aby uniknąć szkodliwych skutków promieniowania, które emitują. Energia.Domena Gov / Pub. Źródło: Wikimedia Commons. Bibliografia
- LUB.S. National Library of Medicine. (2019). Promethium - PM (element). Odzyskane z Pubchem.NCBI.NLM.Nih.Gov.
- Ganjali, m.R. i in. (2016). Wprowadzenie do serii lantanowców (od Lanthanum do Lotetium). Promethium. W określaniu szeregów lantanowców różnymi metodami analitycznymi. Odzyskane z naukowym.com.
- Choppin, g. i in. (2013). Pochodzenie wszechświata i nukleosyntezy. Powolne przechwytywanie neutronów. W radiochemii i chemii nuklearnej (wydanie czwarte). Odzyskane z naukowym.com.
- Ołów, d.R. (redaktor) (2003). Podręcznik chemii i fizyki CRC. 85th CRC Press.
- Bawełna, f. Albert i Wilkinson, Geoffrey. (1980). Zaawansowana chemia nieorganiczna. Czwarta edycja. John Wiley & Sons.
- Royal Society of Chemistry. (2020). Promethium. RSC odzyskał.org.

