Struktura azotanu sodu (nano3), właściwości, zastosowania, ryzyko

- 696
- 43
- Pani Waleria Marek
On Azotan sodu Jest to krystaliczna nieorganiczna substancja stała utworzona przez jon sodu+ i jon azotanowy3-. Jego formuła chemiczna to nano3. W naturze znajduje się go jako minerał nitatyny lub nitratytu, który jest obfity na pustyni Atacama w Chile, więc ten minerał nazywany jest również Salitre de Chile lub Kaliche.
Azotan sodu jest niezakładającą substancją stałą, ale może przyspieszyć utlenianie lub spalanie łatwopalnych materiałów. Z tego powodu ma szerokie zastosowanie w fajerwerkach, w materiałach wybuchowych, w meczach, w cegłach węglowych i niektórych rodzajach pestycydów, w celu wyeliminowania gryzoni i innych małych ssaków.
 Nitratyna lub nitratita, nano azotanowy minerał3. John Sobolewski (JSS) [CC przez 3.0 (https: // creativeCommons.Org/licencje/według/3.0)]. Źródło: Wikimedia Commons.
Nitratyna lub nitratita, nano azotanowy minerał3. John Sobolewski (JSS) [CC przez 3.0 (https: // creativeCommons.Org/licencje/według/3.0)]. Źródło: Wikimedia Commons. Zdolność do spalania lub zapłonu innych materiałów oznacza, że należy go z wielką ostrożnością manipulować. Jeśli jest narażony na płomienie lub pożary, może to wykorzystać. Mimo to nano3 Jest stosowany w przemyśle spożywczym, ponieważ ma właściwości konserwujące, zwłaszcza mięso i niektóre rodzaje serów.
Jednak ich nadmierne spożycie może powodować problemy zdrowotne, szczególnie u kobiet w ciąży, dzieci i dzieci. Podczas transformacji w azotyny w układzie trawiennym może powodować pewne choroby.
[TOC]
Struktura chemiczna
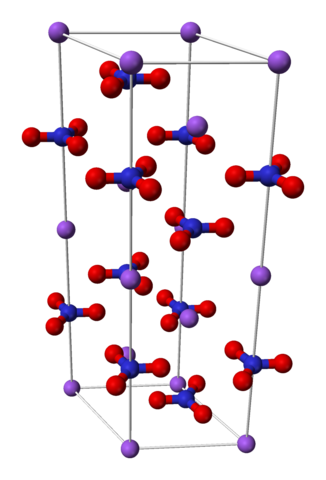 Nano3 Romboédrica Unitary Cell. Źródło: Benjah-BMM27 [domena publiczna]
Nano3 Romboédrica Unitary Cell. Źródło: Benjah-BMM27 [domena publiczna] Azotan sodu składa się z kationu sodu+ i anion azotanowy3-.
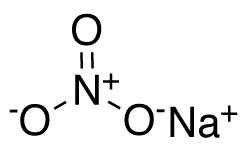 Azotan sodu nano3. Ccroberts [domena publiczna]. Źródło: Wikimedia Commons.
Azotan sodu nano3. Ccroberts [domena publiczna]. Źródło: Wikimedia Commons. W anionie azotanu nr3- Azot n ma wartościowość +5, a tlen wartościowość -2. Z tego powodu anion azotanowy ma obciążenie ujemne.
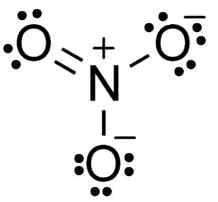 Struktura jonów azotanowych Lewis. TEM5PSU [CC BY-SA 3.0 (https: // creativeCommons.Org/licencje/by-sa/3.0)]. Źródło: Wikimedia Commons.
Struktura jonów azotanowych Lewis. TEM5PSU [CC BY-SA 3.0 (https: // creativeCommons.Org/licencje/by-sa/3.0)]. Źródło: Wikimedia Commons. Anion nr3- Ma płaską i symetryczną strukturę, w której trzy tleny rozkładają sposób ujemny lub jednolity.
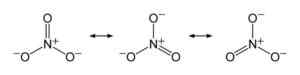 W jonie azotanu obciążenie ujemne jest równo rozmieszczone między trzema atomami tlenu. Benjah-BMM27 [domena publiczna]. Źródło: Wikimedia Commons.
W jonie azotanu obciążenie ujemne jest równo rozmieszczone między trzema atomami tlenu. Benjah-BMM27 [domena publiczna]. Źródło: Wikimedia Commons. Nomenklatura
-Azotan sodu
-Azotan sodu
-Salpeter sodu (angielski Salpeter sodu)
-Nitro Soda (angielski Soda nitre)
-Salitre de Chile
-Azotan chilijski
-Nitratyna
-Nitratita
-Caliche
Nieruchomości
 Romboédyczne kryształy azotanu sodu uzyskane z jego przesyconego roztworu. Źródło: Vadim Sedov [CC przez 4.0 (https: // creativeCommons.Org/licencje/według/4.0)]
Romboédyczne kryształy azotanu sodu uzyskane z jego przesyconego roztworu. Źródło: Vadim Sedov [CC przez 4.0 (https: // creativeCommons.Org/licencje/według/4.0)] Stan fizyczny
Kolor bez kolorów do białych, trygonalnych lub romboedicznych kryształów.
Waga molekularna
84 995 g/mol
Temperatura topnienia
308 ° C
Punkt wrzenia
380 ° C (rozkładają się).
Gęstość
2257 g/cm3 w 20 ° C.
Rozpuszczalność
Rozpuszczalna woda: 91,2 g/100 g wody w temperaturze 25 ° C lub 1 g w 1,1 ml wody. Lekko rozpuszczalne w etanolu i metanolu.
Ph
Roztwory azotanów sodu są neutralne, to znaczy ani kwas, ani podstawowy, dlatego jego pH wynosi 7.
Inne właściwości
Jest to higroskopijna substancja stała, to znaczy pochłania wodę ze środowiska.
 Azotan sodu nano3 solidny. Ondřej Mang [domena publiczna]. Źródło: Wikimedia Commons.
Azotan sodu nano3 solidny. Ondřej Mang [domena publiczna]. Źródło: Wikimedia Commons. Jego rozpuszczanie wody powoduje ochłodzenie roztworu, więc mówi się, że ten proces rozpuszczania jest endotermiczny, innymi słowy, podczas rozpuszczania się pochłania ciepło ze środowiska, a zatem roztwór chłodzi.
Może ci służyć: podstawowy węgiel: cechy, typy i przykładyW bardzo niskich temperaturach azotan sodu jest rozpuszczalny w ciekłym amoniaku NH3, tworzenie nano3· 4nh3 Poniżej -42 ºC.
Nano3 To nie jest paliwo, ale jego obecność przyspiesza spalanie materiałów lub związków. Dzieje się tak, ponieważ po ogrzewaniu, tlen lub2, między innymi gazami.
Uzyskanie
Uzyskuje się głównie przez ekstrakcję złóż mineralnych lub kopalni Salitre de Chile (Caliche lub Nitratita). W tym celu stosuje się solankę, a następnie krystalizacja i rekrystalizacja jest wykonywana w celu uzyskania nano kryształów3 Najczystszy.
Kopalnie te znajdują się głównie w Ameryce Południowej w północnym Chile na pustyni Atacama. Istnieje związany z azotanem potasu3 i do rozkładu materii organicznej.
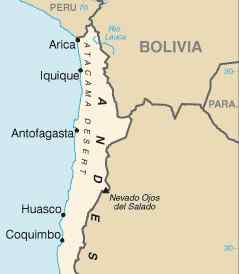 Położenie pustynne Atacama w północnym Chile, gdzie występują ważne złoża azotanu sodu. CIA [domena publiczna]. Źródło: Wikimedia Commons.
Położenie pustynne Atacama w północnym Chile, gdzie występują ważne złoża azotanu sodu. CIA [domena publiczna]. Źródło: Wikimedia Commons. Można go również uzyskać przez reakcję kwasu azotowego z węglanem sodu na2WSPÓŁ3 lub z wodorotlenkiem sodu NaOH:
2 HNO3 + Na2WSPÓŁ3 → 2 Nano3 + WSPÓŁ2↑ + H2ALBO
Obecność w organizmie ludzkim
Azotan sodu może wchodzić do ludzkiego organizmu przez żywność i picie wody, która go zawiera.
60-80% połkniętego azotanu pochodzi z owoców i warzyw. Drugie źródło to wyleczone mięso. Przemysł mięsny używa go, aby zapobiec rozwojowi drobnoustrojów i zachowania koloru.
Jednak wysoki odsetek azotanu obecnego w ludzkim ciele pochodzi z jego endogennej syntezy lub z powodu procesów w organizmie.
Aplikacje
W branży spożywczej
Jest stosowany jako konserwujący żywność, jako środek utwardzający dla marynowanych mięs i jako środek retencyjny dla mięs. Pokarmy, które mogą go zawierać, to boczek, kiełbaski, szynka i niektóre sery.
 Mięso utwardzone, które prawdopodobnie zawierają azotan sodu. Autor: Falco. Źródło: Pixabay.
Mięso utwardzone, które prawdopodobnie zawierają azotan sodu. Autor: Falco. Źródło: Pixabay. W nawozach
Azotan sodu jest stosowany w mieszaninach nawozowych, aby nawozić tytoń, bawełniane i warzywne uprawy.
 Traktor nawozu plantacji. Autor: Franck Barske. Źródło: Pixabay.
Traktor nawozu plantacji. Autor: Franck Barske. Źródło: Pixabay. Jako promotor lub pochlebstwo spalania lub eksplozji
Nano3 Jest stosowany jako utleniacz w wielu zastosowaniach. Jest to solidny bogaty w tlen, który ułatwia proces zapłonu poprzez produkcję lub2.
Obecność nano3 sprawia, że materiały nie wymagają tlenu ze źródeł zewnętrznych do zapłonu, ponieważ dostarcza to wystarczające lub2 Jeśli chodzi o samowystarczalne reakcje egzotermiczne (generatory ciepła), które występują podczas zapalenia lub wybuchu.
Był używany od dawna jako główny utleniacz w materiałach pirotechnicznych (fajerwerki), jako komponent utleniający w materiałach wybuchowych i detonacyjnych lub wybuchach oraz jako środek paliwa.
Może ci służyć: związek chemiczny Fajerwerki. W jego składzie znajduje się azotan nano sodu3. Autor: noszenie. Źródło: Pixabay.
Fajerwerki. W jego składzie znajduje się azotan nano sodu3. Autor: noszenie. Źródło: Pixabay. Służy również do poprawy spalania cegieł węglowych (briquetas), aby sprzyjać zapłonowi w dopasowaniach.
Aby wyeliminować gryzonie i inne ssaki
Jest używany do specjalnego rodzaju pestycydów. Kompozycje, które go zawierają, są pirotechnicznymi fumigantami, które są umieszczane i spalane w norach, uwalniając śmiertelne dawki toksycznych gazów.
Z tego powodu jest używany do kontroli kilku gryzoni, świnek, kojotów i skunksów, na otwartych polach, użytkach zielonych, obszarach niezwiązanych.
W przygotowaniu innych związków
Jest stosowany w produkcji kwasu azotowego HNO3, Azotyn nano sodu2, a także działa jako katalizator w przygotowaniu kwasu siarkowego H2południowy zachód4.
Jest stosowany w produkcji tlenku azotu n2O i jako środek utleniający w produkcji związków farmaceutycznych.
W ekstrakcji elektronicznych metali odpadowych
Niektórzy badacze odkryli, że nano3 Ułatwia niezakładającą ekstrakcję metali zawartych w urządzeniach elektronicznych (telefony komórkowe, tabletki, komputery itp.).
Przydatne metale, które można wyodrębnić z komponentów tych urządzeń elektronicznych, to nikiel Ni, Cobalt Co, Mangan MN, cynk Zn, Cief Cu i aluminium.
Ekstrakcja odbywa się za pomocą tylko jednego roztworu nano3 i polimer. I osiągana jest wydajność 60%.
W ten sposób odpady elektroniczne można poddać recyklingowi przyczyniając się do minimalizacji odpadów i stabilnego odzyskiwania zasobów.
W badaniach nad zdrowiem i ćwiczeniami
Według niektórych badań, spożycie nano suplementów3 lub żywność, która go zawiera, mają pozytywne skutki dla zdrowia. Niektóre pokarmy bogate w azotany to buraki, szpinak i rukola.
Wśród efektów jest poprawa układu sercowo -naczyniowego, zmniejszenie ciśnienia krwi, poprawa przepływu krwi i podniesienie ilości tlenu w tkankach, które są fizycznie wykonywane.
Wskazuje to, że można rozważyć użycie nano3 jako tani leki w zapobieganiu i leczeniu pacjentów z problemami ciśnienia krwi.
Ponadto może służyć jako skuteczna i naturalna pomoc w zwiększeniu siły mięśni u sportowców.
W kilku zastosowaniach
 Plakat reklamowy XX wieku, podżegający do zapłaty gruntu z azotanem Chile. David Perez [domena publiczna]. Źródło: Wikimedia Commons.
Plakat reklamowy XX wieku, podżegający do zapłaty gruntu z azotanem Chile. David Perez [domena publiczna]. Źródło: Wikimedia Commons. Jest stosowany jako utleniacz i środek założycielowy w produkcji szklanek i emaliów do ceramiki. Jest również używany w specjalnych cementach.
Służy jako środek chemiczny w odzyskiwaniu cyny z śmieci metalu, w lateksowej krzepnięciu, w przemyśle jądrowym i kontroli korozji w systemach wodnych.
Może ci służyć: dyspozycja: struktura, właściwości, uzyskiwanie, użyciaRyzyko
Niebezpieczeństwa związane z jego manipulacją
Ma własność przyspieszania spalania materiałów łatwopalnych. Jeśli jesteś zaangażowany w ogień, może wystąpić wybuch.
W przypadku eksploatacji na ciepło lub ogień można wykorzystywać, wytwarzając toksyczne tlenki azotu.
Problemy związane z spożyciem z żywnością lub wodą
Azotan po spożyciu może stać się azotynem zarówno w jamie ustnej, jak i żołądkowej i jelit.
Azotyn podczas reakcji z aminami obecnymi w niektórych pokarmach może stać się nitrozaminy w kwaśnej pożywce, jak w żołądku. Nitrozoamina jest rakotwórcza.
Jednak nie dzieje się tak, gdy owoce i warzywa zawierające azotany są ngawane naturalnie.
Według niektórych badań obecność wysokiego poziomu azotanów może wytwarzać zaburzenie krwi, które powoduje skuteczne uwalnianie tlenu w tkankach.
Może się to zdarzyć u dzieci, których wzór nabiału jest przygotowywany z wodą wodną zawierającą azotany.
Zaobserwowano również, że wysoki poziom azotanu może generować problemy w ciąży niemowląt, powodując spontaniczne aborcje, przedwczesne porody lub wady w rurce nerwowej płodów.
Ostatnio stwierdzono, że azotan sodu może oznaczać ryzyko rozwoju układu mięśniowo-szkieletowego, a u ludzi ma wpływ na komunikację-mięśniowo-multi-mięśnia.
Azotan sodu w żywności
 Azotan sodu występuje jako addytywne w boczku i innych produktach mięsnych. Źródło: Cookbookman17 przez flickr (https: // www.Flickr.com/zdjęcia/[e -mail chroni]/6175755733)
Azotan sodu występuje jako addytywne w boczku i innych produktach mięsnych. Źródło: Cookbookman17 przez flickr (https: // www.Flickr.com/zdjęcia/[e -mail chroni]/6175755733) Azotan sodu jest synonimem mięsa, ponieważ wraz z azotynem są do nich dodawane w celu zachowania ich i poprawy ich wyglądu i smaków. Ze względu na przyczynę nadmierne spożywanie mięsa (perrocalientes, boczek, szynki, wędzone ryby itp.) był zaangażowany w niepokojące połączenie nowotworów w całym układzie trawiennym.
Podczas gdy związek między mięsem leczonym solami azotanowymi i rakiem nie jest absolutna, zaleca się, aby złagodzić jego spożycie.
Z drugiej strony warzywa (marchew, buraki, rzodkiew, sałata, szpinak itp.) Są bogate w nano3 Ponieważ wchłonęli go z gleb uprawnych ze względu na ich działanie nawozu. Spożycie tych warzyw, w przeciwieństwie do produktów mięsnych, nie jest powiązane z cytowanymi chorobami.
Wynika to z dwóch powodów: różnicy w poziomach białka takich pokarmów i sposobu, w jaki gotują. Mięta.
Zawartość witaminy C, błonnika i polifenoli w warzywach zmniejsza tworzenie się tych nitrosoamin. Dlatego nano3 Sam nie stanowi zagrożenia dla jedzenia.
Bibliografia
- LUB.S. National Library of Medicine. (2019). Azotan sodu. Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov.
- Encyklopedia chemii przemysłowej Ullmanna. (1990). PIĄTA EDYCJA. VCH Verlagsgellschaft MBH.
- Pouretal, h.R. i Ravanbod, m. (2015). Badanie kinetyczne Mg/Nano3 Pyrotechniczny za pomocą techniki nie-ooseathermalnej TG/DSC. J Therm Anal Calim (2015) 119: 2281-2288. Link odzyskał.Skoczek.com.
- Jarosz, J. i in. (2016). Azotan sodu zmniejsza indukowany agryną receptor grupowania acetylocholiny. BMC Pharmacology and Toxicology (2016) 17:20. Pobrano z BMCPharmacoltoksicol.Biomedcentral.com.
- Bawełna, f. Albert i Wilkinson, Geoffrey. (1980). Zaawansowana chemia nieorganiczna. Czwarta edycja. John Wiley & Sons.
- Prival, m.J. (2003). Rak. Rakotwórcze w łańcuchu pokarmowym. W Encyclopedia of Food Sciences and Nutrition (wydanie drugie). Odzyskane z naukowym.com.
- Zakhodyaeva i.DO. i in. (2019). Złożona ekstrakcja metali w wodnym układzie dwufazowym na podstawie poli (tlenku etylenu) 1500 i azotanu sodu. Cząsteczki 2019, 24, 4078. MDPI odzyskało.com.
- Clements, W.T. i in. (2014). Spożycie azotanu: przegląd efektów zdrowotnych i fizycznych. Odżywki 2014, 6, 5224-5264. MDPI odzyskało.com.
- « 6 zalet i wady prezentacji cyfrowych
- Ewolucja konserwacji przemysłowej od pochodzenia do teraźniejszości »

