Mieszanina rankingowa kwartalna, przykłady
- 1402
- 429
- Bertrand Zawadzki
A Racmic Mix o Racmatics jest taki z dwóch enancjomerów w równych częściach, a zatem jest optycznie nieaktywny. Ta aktywność optyczna odnosi się do zdolności roztworów do obracania, w harmonogramie lub przeciwwniesieniu, wiązki spolaryzowanego światła, które przemieszcza się przez nie w kierunku.
Enancjomer ma zdolność obracania spolaryzowanego światła, powiedzmy, po lewej (Levógiro), więc jego czyste rozwiązanie będzie optycznie aktywne. Jeśli jednak to zacznie dodawać enancjomer, który obraca światło w prawo (dekstrogyry), jego aktywność optyczna zmniejszy się, aż zostanie inaktywowana.
 Klastry winogron, które dzielą pokrewieństwo z mieszaninami rankingowymi poza etymologią. Źródło: Pexels.
Klastry winogron, które dzielą pokrewieństwo z mieszaninami rankingowymi poza etymologią. Źródło: Pexels. Kiedy tak się dzieje, mówi się, że istnieją takie same ilości enancjomerów Levogiro i Dextrógiro; Jeśli cząsteczka złamała spolaryzowane światło w lewo, jego efekt zostanie natychmiast anulowany, gdy „potyka się” z inną cząsteczką, która obraca ją po prawej stronie. I tak dalej. Dlatego będziemy mieli mieszaninę rankingową.
Pierwsze obserwację ulepszenia dokonał francuski chemik Louis Pasteur w 1848 r., Który badał mieszaninę enancjomerycznych kryształów kwasu tartarowego (do tego czasu zwanego kwasem rankinowym). Kiedy ten kwas z winogron wykorzystywanych do produkcji wina, ta mieszanka zakończyła się w ogólnym stylu dla wszystkich cząsteczek.
[TOC]
Buty i chiralność
Po pierwsze, istnieje mieszanka rozumowania, musi istnieć dwa enancjomery (zwykłe), co oznacza, że obie cząsteczki są chiralami i że ich obrazy lustrzane nie są nakładane. Para butów ilustruje to doskonale: bez względu na to, ile lewy but jest próbowany po prawej stronie, nigdy nie mogą się dopasować.
Może ci służyć: słaby kwasPrawy but, jak powiedzieć, kieruje spolaryzowane światło w lewo; podczas gdy lewy but robi to po prawej stronie. W hipotetycznym rozwiązaniu, w którym buty są cząsteczkami, jeśli są tylko buty prawne, chirus, będzie to optycznie aktywne. W ten sam sposób, w jaki stanie się tak, jeśli w roztworze pozostaną tylko buty.
Jeśli jednak jest tysiąc lewych butów zmieszanych z tysiącami praw, istnieje wówczas mieszanka rankingowa, która jest również nieaktywna, ponieważ odchylenia doznane przez światło w środku są anulowane wzajemnie.
Gdyby zamiast butów były piłki, obiekty, które są akwiralne, nie byłoby możliwe, aby istniały ich mieszanki rankingowe, ponieważ nie byłyby w stanie istnieć jako pary enancjomeryczne.
Przykłady
Kwas winowy
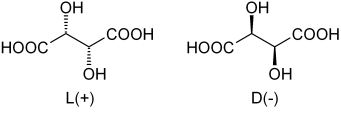 Enantimery kwasu tatarowego. Źródło: Dschanz [domena publiczna]
Enantimery kwasu tatarowego. Źródło: Dschanz [domena publiczna] Wracając do kwasu tatarowego, jego ranga była pierwsza, która spotkała. Na górnym obrazie pokazano jego dwa enancjomery, każdy zdolny do tworzenia kryształów z morfologicznymi twarzami „lewej” lub „prawej”. Pasteur, pomagając mikroskopowi i rygorystycznemu wysiłkowi, udało się oddzielić te enancjomeryczne kryształy od siebie.
Kryształy enancjomerów L (+) i D (-) osobno przedstawiają aktywność optyczną poprzez przekształcenie światła spolaryzowanego odpowiednio w prawej lub lewej stronie. Jeśli oba kryształy w tych samych proporcjach molowych rozpuszczają się w wodzie, uzyskano optycznie nieaktywną mieszaninę rankingową.
Zauważ, że oba enancjomery mają dwa chiralne węgle (z czterema różnymi podstawnikami). W L (+) OH znajdują się za płaszczyzną utworzoną przez szkielet węglowy i grupy COOH; Podczas gdy w d (-) te OH są powyżej wspomnianego samolotu.
Ci, którzy syntetyzują kwas tartarowy, uzyskają mieszaninę rankingową. Aby oddzielić enancjomer L (+) od D (-), konieczna jest rozdzielczość kwisowa, w której mieszanina ta reakcja jest reakcji z chiralną podstawą w celu wytworzenia soli diasteroizomerowych, zdolnych do rozdzielenia przez ułamkową krystalizację.
Może ci służyć: siarczek miedzi: struktura, właściwości, zastosowaniaChinina
 Szkielet strukturalny cząsteczki chininy. Źródło: Benjah-BMM27.
Szkielet strukturalny cząsteczki chininy. Źródło: Benjah-BMM27. W poprzednim przykładzie, w odniesieniu do mieszanki rankingu kwasu tatarowego, jest ona zwykle zapisywana jako kwas (±) -tartaric. Zatem w przypadku chininy (obraz górnego) będzie (±) -quinina.
Izomeria chininy jest złożona: ma cztery chiralne węgle, co daje szesnastu diasteroizomerów. Co ciekawe, dwa z jego enancjomerów (jeden z OH powyżej płaszczyzny i drugi poniżej), są w rzeczywistości diasthelisomerami, ponieważ różnią się konfiguracją innych chiralnych węgli (rower z atomem N N).
Teraz trudno jest określić, który ze stereoizomerów chininy skieruje spolaryzowane światło po prawej lub po lewej stronie.
Talidomid
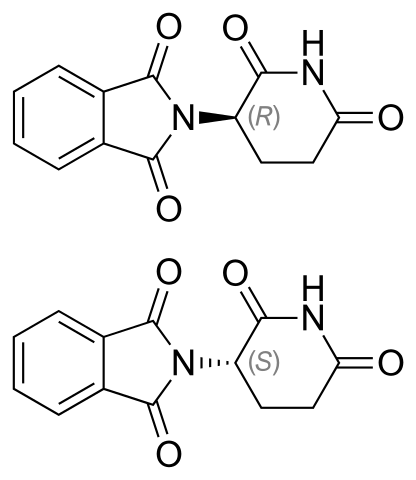 Enantimery Talaidomide. Źródło: szczepienia [domena publiczna]
Enantimery Talaidomide. Źródło: szczepienia [domena publiczna] Enancjomery talidomidów pokazano powyżej. Ma tylko quiralny węgiel: ten, który jest powiązany z azotem, który łączy oba pierścienie (jeden z ftalimidy i drugi z gluteramidu).
W enancjomorze R (o właściwościach uspokajających) pierścień ftalimidy (po lewej) jest zorientowany nad płaszczyzną; podczas gdy w enancjomeru (z właściwościami mutagennymi), poniżej.
Procent tych dwóch nie jest znany, który z dwóch kieruje światłem w lewo lub w prawo. To, co wiadomo, jest to, że mieszanina 1: 1 lub 50% obu enancjomerów tworzy mieszaninę rankinową (±) -Talidomid.
Jeśli chcesz jedynie sprzedawać talidomid jako hipnotyczny środek uspokajający, obowiązkowe jest przedłożenie swojej mieszanki rankingowej do już wspomnianej rozdzielczości chiralnej, tak aby otrzymywano czysty enancjomer.
Może ci służyć: związki czwartorzędowe: cechy, szkolenie, przykłady1.2-epoksypropan
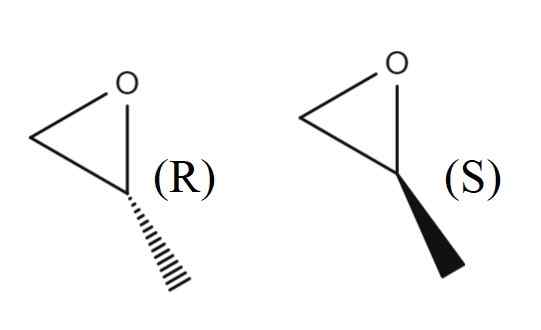 1,2-epoksypropan enancjomery. Źródło: Gabriel Bolívar.
1,2-epoksypropan enancjomery. Źródło: Gabriel Bolívar. Na górnym obrazie masz parę enancjomerów 1,2-epoksypropanu. Enancjomer R kieruje spolaryzowane światło w prawo, podczas gdy S kieruje je w lewo; Oznacza to, że pierwszym jest (R)-(+)-1,2-epoksypropano i drugi (s)-(-)-1,2 epoksypropano.
Mieszanina rankingowa z ich dwóch, ponownie, w stosunku 1: 1 lub 50%, staje się (±) -1,2 -epoksypropan.
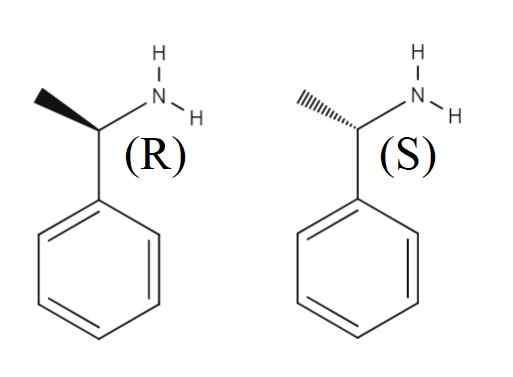
1-fenyloetyloamina
 Enancjomery 1-penyloetyloaminy. Źródło: Gabriel Bolívar.
Enancjomery 1-penyloetyloaminy. Źródło: Gabriel Bolívar. Pokazano górną kolejną mieszaninę rankingową utworzoną przez dwa enancjomery 1-feniletyloaminy. Enancjomer R to (R)-(+)-1-fenyloetyloamina i enancjomer S (s)-(-)-1-feniletylamina; Jeden ma grupę metylową, Cho3, wskazując na aromatyczną płaszczyznę pierścienia, a drugi wskazujący pod tym.
Należy zauważyć, że gdy konfiguracja jest R, czasami pokrywa się z faktem, że enantiómero obraca spolaryzowane światło po prawej stronie; Jednak nie zawsze ma to zastosowanie i nie można go traktować.
Ostateczny komentarz
Ważniejsze niż istnienie lub nie mieszanin ranking. Dotyczy to szczególnie związków o skutkach farmakologicznych, które zależą od takiego stereoizomu; To znaczy enancjomer może być korzystny dla pacjenta, podczas gdy drugi może na to wpłynąć.
Właśnie dlatego te chiralne rozdzielczości są stosowane do oddzielnych mieszanin rankingowych w swoich komponentach, a tym samym być w stanie sprzedawać je jako czyste leki wolne od szkodliwych zanieczyszczeń.
Bibliografia
- Morrison, r. T. i Boyd, R, N. (1987). Chemia organiczna. 5. edycja. Redakcja Addison-Wesley Inter-American.
- Carey f. (2008). Chemia organiczna. (Szósta edycja). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Chemia organiczna. Aminy. (10. edycja.). Wiley Plus.
- Steven a. Hardinger. (2017). Ilustrowany glosariusz chemii organicznej: mieszanka racemiczna. Departament Chemii i Biochemii, UCLA. Odzyskane z: chem.UCLA.Edu
- Nancy Devino. (2019). Mieszanka racemiczna: definicja i przykład. Badanie. Odzyskane z: Study.com
- James Ashenhurst. (2019). Stereochemia i chiralność: co to jest racemiczna mieszanka? Odzyskane z: MastorganicChemistry.com
- John C. Leffingwell. (2003). Chiralność i bioaktywność i.: Farmakologia. [PDF]. Odzyskany z: Leffingwell.com

