Hydroksiapatyt

- 1773
- 107
- Pani Waleria Marek
Wyjaśniamy, co to jest hydroksyloapatyt, jego struktura, jak jest syntetyzowany, jego zastosowania oraz właściwości fizyczne i chemiczne
 Hydroksiapatyt. Źródło: Rob Lavinsky, Irocks.COM-CC-BY-SA-3.0, CC BY-SA 3.0, Via Wikimedia Commons
Hydroksiapatyt. Źródło: Rob Lavinsky, Irocks.COM-CC-BY-SA-3.0, CC BY-SA 3.0, Via Wikimedia Commons Co to jest hydroksyapatyt?
Hydroksiapatyt Jest to minerał fosforanu wapnia, którego wzór chemiczny to CA10(PO4)6(OH)2. Wraz z innymi minerałami oraz organiczną i zagęszczoną materią organiczną, tworzy surowiec znany jako skała fosforowa. Termin hydroxi odnosi się do anionów oh-.
Gdyby zamiast tego anionu było fluorkiem, minerał nazywałby się fluoroapatita (ca10(PO4)6(F)2; I tak z innymi anionami (CL-, Br-, WSPÓŁ32-, itp.). Podobnie, hydroksyapatyt jest głównym nieorganicznym składnikiem kości i szkliwa zębów, głównie obecnym w krystalicznym.
Jest to ważny element w tkankach kostnych żywych istot. Jego wielka stabilność wobec innych fosforanów wapnia pozwala mu wspierać warunki fizjologiczne, nadając kości ich charakterystycznej twardości. Hydroksyiapatyt nie jest sam: wypełnia swoją funkcję towarzyszącą kolagenem, włóknistym białkiem tkanek spojówkowych.
Hydroksyapatyt (lub hydroksylapatyt) zawiera jony CA2+, Ale inne kationy mogą również pomieścić w swojej strukturze (Mg2+, Na+), Zanieczyszczenia zaangażowane w inne procesy biochemiczne kości (takie jak ich przebudowa).
Struktura hydroksyapatytu
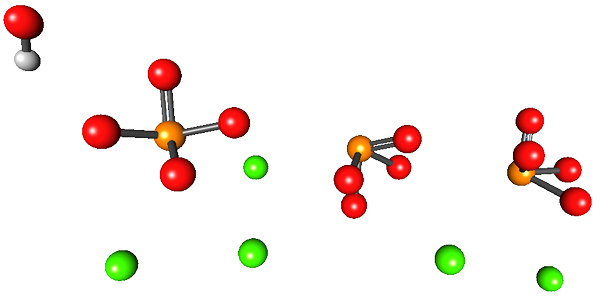
Najwyższy obraz ilustruje strukturę hydroksyapatytu wapnia. Wszystkie sfery zajmują objętość połowy sześciokątnej „szuflady”, w której druga połowa jest identyczna z pierwszą.
W tej strukturze zielone kule odpowiadają kationom CA2+, Podczas gdy czerwone kule do atomów tlenu, pomarańczowych do fosforu i białej atomu wodoru OH-.
Jony fosforany na tym obrazie mają wadę nie wykazywania geometrii czworościennej; Zamiast tego wydają się piramidy kwadratowe.
Może ci służyć: stan sztrowyOH- daje wrażenie, że znajduje się daleko od CA2+. Jednak jednostka krystaliczna może powtórzyć się na dachu pierwszego, pokazując w ten sposób bliską bliskość obu jonów. Ponadto jony te można zastąpić przez inne (na+ i f-, Na przykład).
Synteza hydroksylapatytu
Hydroksyloapatyt można zsyntetyzować przez reakcję wodorotlenku wapnia z kwasem fosforowym:
10 Ca (OH)2 + 6 godz3PO4 => Ca10(PO4)6(OH)2 + 18 godz2ALBO
Hydroksyiapatita (CA10(PO4)6(OH)2) jest wyrażany przez dwie jednostki CA Formuły5(PO4)3Oh.
Podobnie hydroksyapatyt można zsyntetyzować poprzez następującą reakcję:
10 Ca (nie3)2.4h2O + 6 NH4H2PO4 => Ca10(PO4)6(OH)2 + 20 NH4NIE3 + 52 godz2ALBO
Kontroluj prędkość opadów pozwala na generowanie nanocząstek hydroksyapatytu.
Kryształy hydroksyapatytu

Jony są zagęszczone i rosną, tworząc sztywne i odporne biokrytyczne. Jest to stosowane jako biomateriał mineralizacji kości.
Potrzebuje jednak kolagenu, wsparcia organicznego, które służy jako forma jego wzrostu. Te kryształy i ich skomplikowane procesy formowania będą zależeć od kości (lub zęba).
Kryształy te rosną impregnowane w materii organicznej, a zastosowanie technik mikroskopii elektronicznej opisują je w zębach jako agregaty z kształtami prętów zwanymi pryzmatami.
Zastosowanie hydroksylapatytu
Użycie medyczne i dentystyczne
Ze względu na podobieństwo wielkości, krystalografię i kompozycję z twardą ludzką tkanką, nanohydroksyapatyt jest atrakcyjny w stosowaniu w protezach. Ponadto nanohydroksyapatyt jest biokompatybilny, bioaktywny i naturalny, a także nie jest toksyczny lub zapalny.
W związku z tym ceramika nanohydroksyapatytu ma różne zastosowania, w tym:
- W chirurgii kości Tejido jest stosowany w wypełnianiu wnęk w operatach ortopedycznych, traumatologicznych, szczękowych i dentystycznych.
- Jest stosowany jako powłoka implantów ortopedycznych i dentystycznych. Jest to środek odczulający używany do wybielania dentystycznego. Jest również wykorzystywany jako środek reneralizacyjny w pastach dentystycznych i wczesnym leczeniu próchnicy.
- Implanty ze stali nierdzewnej i tytanu są często pokryte hydroksyapatytem, aby zmniejszyć ich prędkość odrzucania.
- Jest to alternatywa dla alogennych i ksenogenicznych przeszczepów kości. Czas gojenia jest krótszy w obecności hydroksyapatytu niż w jego nieobecności.
- Nanohidroksyapatytu syntetyczna mimetiza do hydroksyapatytu obecna naturalnie w zębinie i apatytowej enmaltic.
Inne zastosowania hydroksyapatytu
- Hydroksyapatyt jest stosowany w filtrach powietrza pojazdów silnikowych w celu zwiększenia ich wydajności w absorpcji i rozkładu tlenku węgla (CO). To zmniejsza zanieczyszczenie środowiska.
- Zsyntetyzowano kompleks alginianu-hydroksyapatytu.
- Hydroksyiapatyt jest stosowany jako pożywka chromatograficzna dla białek. Ma to pozytywne opłaty (CA++) i negatywne (PO4-3), dzięki czemu może oddziaływać z białkami naładowanymi elektrycznie i umożliwić jego separację przez wymianę jonową.
- Hydroksyapatyt został również zastosowany jako wspornik elektrofotycznych kwasów nukleinowych. Możliwe jest oddzielenie DNA od RNA, a także DNA prostej nici dwóch nici DNA.
Fizyczne i chemiczne właściwości
Hydroksyapatyt to biała substancja stała, która może zdobyć szare, żółte i zielonkawe tony. Podobnie jak krystaliczna substancja stała, przedstawia wysokie punkty fuzji, wskazujące na silne oddziaływania elektrostatyczne; W przypadku hydroksyapatytu jest to 1100 ° C.
Jest gęstszy niż woda, o gęstości 3,05 - 3,15 g/cm3. Ponadto jest praktycznie nierozpuszczalny w wodzie (0,3 mg/ml), co jest spowodowane jonami fosforanów.
Jednak w pożywkach kwaśnych (jak w HCl) jest rozpuszczalny. Ta rozpuszczalność jest spowodowana utworzeniem CACL2, Wysoce rozpuszczalna sól wodna. Podobnie fosforany są protonem (HPO42- i H2PO4-) i w interakcja w lepszym stopniu z wodą.
Rozpuszczalność kwaśnego hydroksyapatytu jest ważna w patofizjologii próchnicy. Bakterie w jamie jamy ustnej wydzielają kwas mlekowy, produkt fermentacji glukozy, który zmniejsza pH powierzchni dentystycznej do mniejszej niż 5, więc hydroksyapatyt zaczyna rozpuszczać.
Może ci służyć: sublimacja: koncepcja, proces i przykładyFluor (f-) Możesz wymienić jony OH- W strukturze krystalicznej. Kiedy tak się dzieje, zapewnia odporność na hydroksyapatyt szkliwa zębów przed kwasami.
Być może opór ten może wynikać z nierozpuszczalności CAF2 uformowane, odmawiając „opuszczenia” szkła.
Bibliografia
- Shiver & Atkins. (2008). Chemia nieorganiczna. (Czwarty ed., P. 349, 627). MC Graw Hill.
- Fluidinova. (2017). Hydroksylapatyt. Pobrano z Fluidinova.com
- Gaiabulbanix. (5 listopada 2015). Hydroksyapatyt. [Postać]. Wyzdrowiał z Commons.Wikimedia.org
- Jaskółka oknówka.Neitsov. (25 listopada 2015). Hüdroksüapatiidi Kristallid. [Postać]. Wyzdrowiał z Commons.Wikimedia.org
- Wikipedia. (2018). Hydroksylapatyt. Odzyskane z.Wikipedia.org
- Fiona Petchey. Kość. C14Dating odzyskano.com

