Cykliczna struktura węglowodorów, właściwości, przykłady
- 2540
- 390
- Filip Augustyn
Cykliczne węglowodory Są to związki organiczne składające się z atomów węgla i wodoru, które są powiązane z powodem pierścieni lub cyklicznych struktur. Istnieją głównie trzy typy: aliakomia, aromatyczne i wielopierścieniowe.
Tego rodzaju węglowodory mogą następnie składać się z zamkniętych wersji alkanów, alkenów i alkin; mają pierścienie z układami aromatycznymi, takimi jak benzen i jego pochodne; lub przedstawiają skomplikowane i fascynujące struktury. Spośród nich Alicyclics są najprostsze i są zwykle reprezentowane przy użyciu wielokątów.
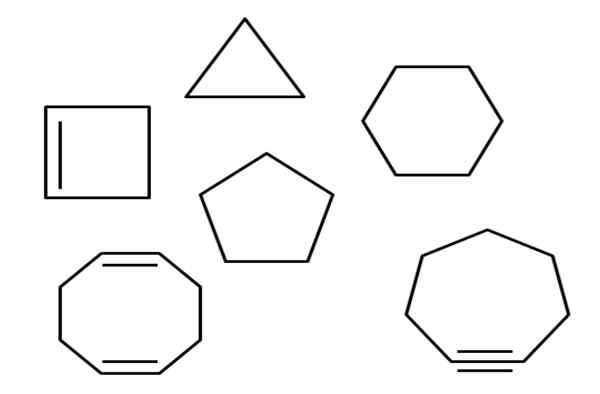
 Alicykliczne węglowodory. Źródło: Gabriel Bolívar.
Alicykliczne węglowodory. Źródło: Gabriel Bolívar. Powyżej, na przykład, istnieje kilka alicyklicznych węglowodorów. Wydają się proste wielokąty: kwadrat, trójkąt, pentagon, sześciokąt itp. Gdyby jedno z jego linków C-C można było wyciąć nożyczkami, wynik byłby alkan, alkene (jeśli ma podwójne linki) lub alquino (jeśli masz linki potrójne).
Jego właściwości nie różnią się zbytnio od węglowodorów z otwartym łańcuchem, z których pochodzą; Chociaż chemicznie, im większy, tym bardziej stabilny, a jego interakcja z pożywką molekularną staje się najbardziej wyraźna (dla największego obszaru kontaktowego).
[TOC]
Struktura
Idąc prosto do sprawy, która dotyczy ich struktur, należy wyjaśnić, że nie są one płaskie, nawet gdy w ich reprezentacji wielokątów wydają się tak. Jedyny wyjątek od tego twierdzenia znajduje się w cyklopropanie.
Konieczne jest również wyjaśnienie, że terminy „cykle” i „pierścieni” są często wymienne; Pierścień nie musi się krążyć, a zatem może zdobyć niekończące się geometrie, o ile jest to zamknięta struktura. Następnie mówi się, że cyklopropan ma pierścień lub trójkątny cykl.
Wszystkie węgle mają hybrydyzacje SP3, Tak więc ich geometrie są czworościami, a ich powiązania muszą być idealnie oddzielone kątem 109,5 °; Nie jest to jednak możliwe w przypadku struktur tak zamkniętych jak cyklobutanu (kwadrat) lub cyklopentano (Pentagon).
Może ci służyć: benzimidazol (C7H6N2): historia, struktura, zalety, wadyNastępnie mówi się o napięciu, które destabilizuje cząsteczkę i jest określana eksperymentalnie przez pomiar średnich cieplnych cieplnych cieplnych w każdej grupie2.
Konformacje
I co się stanie, gdy są podwójne lub potrójne linki? Napięcie wzrasta, ponieważ tam, gdzie jest jeden z nich, konstrukcja będzie zmuszona do „zmniejszenia” i pozostania płaskim; które, kolejno, wymusiłyby konformację nad innymi, prawdopodobnie przyćmiewając sąsiednie atomy wodoru.
 Konformery dla cykloheksanu. Źródło: Sponk [domena publiczna]
Konformery dla cykloheksanu. Źródło: Sponk [domena publiczna] Na górnym obrazie pokazano dwa zorganizowania cykloheksanu, aby próbować wyjaśnić powyższe. Atomy, które są w pozycjach Do albo I Mówi się, że są odpowiednio osiowe lub równikowe. Zauważ, że zamiast płaskiego sześciokąta masz krzesło (po lewej) i łódź (po prawej).
Struktury te są dynamiczne i ustalają między nimi równowagę. Jeśli atomy w Do Są bardzo nieporęczne, pierścień „pomieści”, aby ustawić je w pozycjach równikowych; ponieważ są one zorientowane w kierunku boków pierścienia (które wzmacniałyby lub zaszkodziłoby interakcjom międzycząsteczkowym).
Jeśli obserwujemy każdy węgiel osobno, okaże się, że są to tetrahedral. Nie byłoby tak, gdyby istniała podwójna więź: jego hybrydyzacje SP2 zmusiliby strukturę do spłaszczenia; i posiadanie potrójnego linku, aby wyrównać. Płaska struktura benzenu jest maksymalną reprezentacją tego.
Nieruchomości
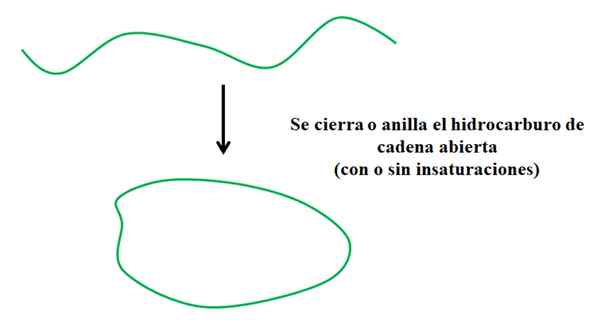 Uproszczony proces, w którym powstaje cykliczny węglowodór. Źródło: Gabriel Bolívar.
Uproszczony proces, w którym powstaje cykliczny węglowodór. Źródło: Gabriel Bolívar. Załóżmy, że masz węglowodorów otwartego łańcucha (z lub bez nienaturowania lub konsekwencji). Gdybyśmy mogli dołączyć do ich końców, powstanie pierścień lub cykl (np. Na górnym obrazie).
Z ekologicznej optyki syntezy nie zdarza się to już; Na końcach łańcucha muszą istnieć dobre grupy wychodzące, które po wyjściu promują, że łańcuch zamyka się (jeśli rozwiązanie jest bardzo rozcieńczone).
Może ci służyć: heptano (C7H16): struktura, właściwości i zastosowaniaMając to na uwadze, można zauważyć, że węglowodor zielonego skoku cierpi tylko transformacja w odniesieniu do jego struktury; Bez przerwy lub dodania nowych linków z innymi atomami. Oznacza to, że chemicznie nadal jest taki sam przed i po zamknięciu lub dzwonieniu.
Dlatego właściwości chemiczne lub fizyczne tych węglowodorów allicylowych nie różnią się zbytnio od właściwości. Oba są odczynnikami dla tego samego gatunku (powiedzieć, halogeny pod światłem Utraviolet) i mogą cierpieć silne utlenianie lub spalanie poprzez uwalnianie.
Siły międzycząsteczkowe
Istnieje niezaprzeczalny fakt: pierścień ma większy obszar kontaktu niż otwartym łańcuchem, a zatem jego interakcje międzycząsteczkowe są silniejsze.
W rezultacie jego punkty gotowania i fuzji są zwykle większe, podobnie jak ich gęstości. Można zauważyć wiele różnic w ich szybkościach refrakcji lub ciśnienia pary.
Nomenklatura
Wracając do przykładu węglowodorów z zielonym skokiem, jego nomenklatura pozostaje niezmieniona po zamknięciu się (jako wąż, który gryzie własnego ogona). Dlatego reguły nomenklatury pozostają takie same; O ile nie zostaną rozwiązane węglowodory policykliczne lub aromatyczne.
Trzy związki pokazano poniżej, które otrzymają odpowiednie nazwy:
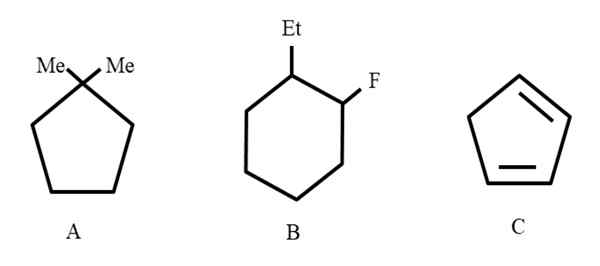 Trzy przykłady cyklicznych węglowodorów do przypisania ich nomenklatury. Źródło: Gabriel Bolívar.
Trzy przykłady cyklicznych węglowodorów do przypisania ich nomenklatury. Źródło: Gabriel Bolívar. Na początek, gdy są to zamknięte struktury, cykl prefiksu służy do nich (tutaj pierścień słów jest przeniesiony).
Od lewej do prawej mamy: cyklopentano, cykloheksan i inny cyklopentano. Węgle są wymienione w taki sposób, że drobne liczby są przypisywane do zamienników, a także są wymienione w kolejności alfabetycznej.
Może ci służyć: renio: odkrycie, właściwości, struktura, zastosowaniaZatem staje się: 1.1-dimetylocyklopentano. W B zaczyna się od wymienienia podstawnika etylowego przed fluorem, więc nazywa się: 1-etylo-2-fluorcicloheksano. A następnie dla C podwójne wiązania są traktowane jako podstawniki, liczbę tworzących się węgli należy wskazać: 1.3-Cyclopentadieno.
Przykłady
W całym artykule wspomniano o kilku cyklicznych węglowodorach. Na pierwszym obrazie można je znaleźć: Cycloopropan, cyklobutan, cyklopentano, cykloheksan, cykloheptan i cyklooktan.
Od nich można uzyskać szeroki zakres pochodnych i wystarczy umieścić podwójne lub potrójne linki, aby mieć odpowiednio cykloalki lub cykloalquiny. W odniesieniu do aromatycznych węglowodorów wystarczy, aby pamiętać o pierścieniu benzenowym i zastąpić go lub odtworzyć w dwóch wymiarach.
Jednak najbardziej niezwykłe (i problematyczne, gdy rozumieją ich nomenklaturę) to wielopierścieniowe węglowodory; Oznacza to, że nie wystarczy proste wielokąty, nawet aby je reprezentować w prosty sposób. Trzy z nich warto wspomnieć: kubańskie, kosz i pagodano (niższe obrazy).
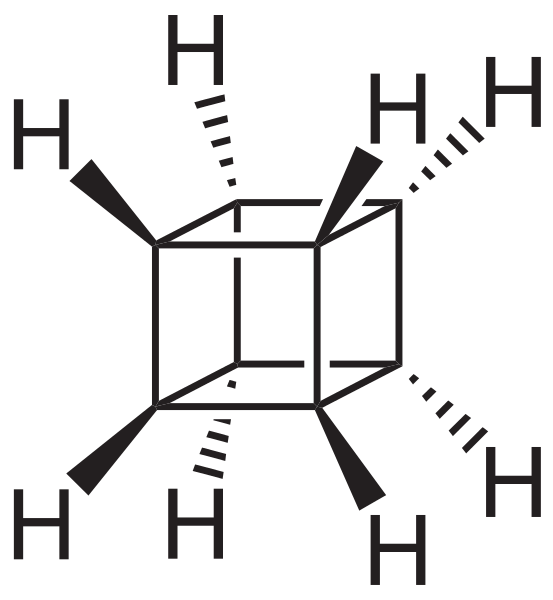 Szkielet kubański. Źródło: Neuropoger [domena publiczna].
Szkielet kubański. Źródło: Neuropoger [domena publiczna].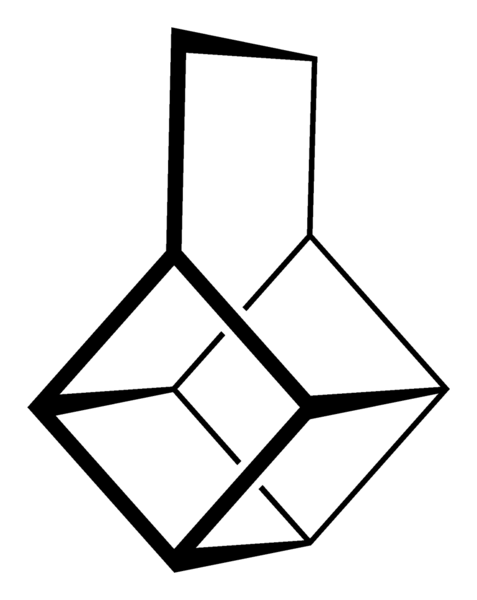 Szkielet Canastano. Źródło: Benjah-BMM27 [domena publiczna].
Szkielet Canastano. Źródło: Benjah-BMM27 [domena publiczna]. Szkielet Pagodano. Źródło: Puppy8800 [domena publiczna]
Szkielet Pagodano. Źródło: Puppy8800 [domena publiczna]
Każdy z nich ma swoją złożoną metodologię syntezy, swoją historię, sztukę i ukrytą fascynację nieskończonymi możliwościami strukturalnymi, do których mogą dotrzeć proste węglowodory.
Bibliografia
- Morrison, r. T. i Boyd, R, N. (1987). Chemia organiczna. 5. edycja. Redakcja Addison-Wesley Inter-American.
- Carey f. (2008). Chemia organiczna. (Szósta edycja). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Chemia organiczna. Aminy. (10. edycja.). Wiley Plus.
- Reid Danielle. (2019). Cykliczne węglowodory: definicja i przykład. Badanie. Odzyskane z: Study.com
- Fundacja CK-12. (5 czerwca 2019). Cykliczne węglowodory. Chemia librettexts. Odzyskane z: chem.Librettexts.org
- Wikipedia. (2019). Cykliczny związek. Źródło: w:.Wikipedia.org
- Miguel Cowboy. (2019). Cykliczne węglowodory. Odzyskane z: decyas.internet

