Struktura fosfatydilinozytolu, trening, funkcje
- 3542
- 469
- Gabriela Łuczak
On fosfatydilinozytol Jest to fosfolipid rodziny glicerofosfolipidów lub fosfoglicerydów, które są obecne w błonach biologicznych. Stanowi około 10% całkowitej zawartości fosfolipidów w przeciętnej komórce.
Jest to powszechne w wewnętrznej powierzchni błony plazmatycznej wielu eukariotów i prokariotów. U ssaków i innych kręgowców szczególnie wzbogaca błony komórek mózgowych; I to było w tych tkaninach, gdzie po raz pierwszy zaobserwowano Folch i Woooley w 1942 roku.
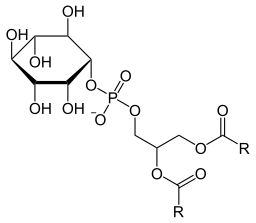
 Klasyczna reprezentacja fosfatydyloinitolu (źródło: neurotoger [domena publiczna] za pośrednictwem Wikimedia Commons)
Klasyczna reprezentacja fosfatydyloinitolu (źródło: neurotoger [domena publiczna] za pośrednictwem Wikimedia Commons) Jego struktura chemiczna, a także struktura niektórych fosforylowanych pochodnych, została określona przez grupę badawczą Ballou w latach 1959–1961.
Ma ważne funkcje strukturalne, związane z jego obfitością w błonach, ale jest również ważnym źródłem drugiego posłańców, które mają ważne implikacje w procesach sygnalizacji komórkowej, które są wystrzelone przez liczne i różne specjalne bodźce.
Ich glikozylowany kształt uczestniczy w kowalencyjnej modyfikacji białka, która pozwala im dołączyć do błon przez struktury lipidowe zwane „kotwicami” GPI (glikosylofosfatydyloinozytol).
[TOC]
Struktura
Podobnie jak większość lipidów membranowych, fosfatydyloinozytol jest cząsteczką amfipatyczną, to znaczy jest cząsteczką z końcem polarnym hydrofilowym i kolejnym szczodłym końcem natury hydrofobowej.
Jego ogólna struktura opiera się na szkielecie 3-fosforanowej 1,2-DIACOl ”, reprezentuje region polarny.
Grupa Cabeza: inozytol
Zjednoczona cząsteczka inozytolu za pomocą wiązania fosfodiéster z grupą fosforanową w węglu w pozycji 3 cząsteczki glicerolu reprezentuje grupę „głowy” tego fosfolipidu.
Może ci podać: gruczoły solneInozytol jest pochodną cykloheksanu, który ma wszystkie jego atomy węgla (6) zjednoczone z grupą hydroksylową. Może pochodzić z żywności spożywanej w diecie, z trasy syntezy Novo lub twój własny recykling. Komórki mózgowe, a także inne tkanki w mniejszej proporcji, wytwarzają z 6-fosforanu glukozy.
Struktura wielu pochodnych fosfatydyloinolu jest niczym więcej niż cząsteczką fosfatydyloinitolu, do której dodano grupy fosforanowe w dowolnej z grup hydroksylowych części inozytolu.
Niepolaryczne kolejki
Łańcuchy węglowodorów o ogonach apolarnych mogą mieć zmienne długości od 16 do około 24 atomów węgla, w zależności od tego ciała.
Łańcuchy te mogą być nasycone (prosty węgiel - węgiel) lub nienasycony (węgiel - węgiel; monoundynowany lub wielonienasycony). Zazwyczaj jest nienasycony.
Zwykle te lipidy mają łańcuchy kwasu tłuszczowego odpowiadające kwasowi stearynowe i kwasu arachidonowego, 18 i 20 atomów węgla, jeden nasycony, a drugi nienasycony, odpowiednio.
Szkolenie
Fosfatydyloinozytol, podobnie jak inne fosfolipidy, powstaje z kwasu fosfatydowego, prostego fosfolipidu, którego struktura charakteryzuje się dwoma ogonami niepolowymi.
Synteza Novo
Dla edukacji Novo fosfatydyloinozytolu kwas fosfatydowy reaguje z CTP (tryfosforan cytydyny), cząsteczką o wysokiej energii analogicznej do ATP oraz postaci CDP-dicyloglicerolu, który jest powszechnym prekursorem w trasie fosfatydyloinolowej i pochodnymi pochodnymi fosfatydyloglicerolem i dwubera.
Może ci służyć: prionsReakcja, o której mowa, jest katalizowana przez syntazę CDP-dicyloglicerolu, która ma podwójną lokalizację subkomórkową, która obejmuje frakcję mikrosomalną i wewnętrzną błonę mitochondrialną.
Fosfatydyloinozytol wynika później z reakcji kondensacji między cząsteczką inozytolu a jedną z CDP-dicyloglicerolu wynikającego z poprzedniego przejścia.
Ten etap jest katalizowany przez syntazę fosfatydyloinozytolu (CDP-diacyloglicerolu: transfraza 3-fosfatydylowa mioinozytolowa), enzym związany z błoną retikulum endoplazmatycznego komórek ssaków.
Reakcją reprezentującą ograniczający etap tego procesu jest w rzeczywistości formacja inozytolu z 6-fosforanowej glukozy, która musi wystąpić „powyżej” trasy biosintetycznej.
Synteza jego pochodnych
Fosfatydyloinozytolowe pochodne fosforylowane są wytwarzane przez grupę enzymów zwanych kinazami fosfatydyloinozytolowymi, które są odpowiedzialne za łączenie grup fosforanowych z grupami hydroksylowymi części inozytolu w części lipidu prekursorowego lipidu.
Funkcje
Strukturalny
Podobnie jak fosfatydyloseryna i fosfatydyloglicerol, fosfatydyloinozytol wypełnia wiele funkcji. Ma ważne implikacje strukturalne, ponieważ jest częścią koni lipidowych, które składają się na różne i wielofunkcyjne błony biologiczne.
Wiele białek jest „wiążących się” z błonami komórkowymi poprzez tak zwane „kotwice GPI”, które są niczym więcej niż glikozylowanymi pochodnymi fosfatydylinitolu, które zapewniają białka hydrofobowy „kotwica”, która trzyma je na powierzchni błony.
Niektóre białka cytoszkieletu wiążą się z pochodnymi fosfatydyloinitolowymi, a ten typ lipidów służy również jako jądro do tworzenia kompleksów białkowych zaangażowanych w egzocytozę.
W sygnalizacji komórkowej
Na przykład jego pochodne są drugim posłańcami w wielu procesach sygnalizacyjnych związanych z hormonami u ssaków.
Może ci służyć: zwierzęta z LDwa z najważniejszych wtórnych przekaźników, które pochodzą z tak zwanego „systemu fosfatydyloinozytolu wrażliwego na hormony”, to 1,4,4-trifosforan inozytolu (IP3 lub inozytolowy tryposforan) i diacyloglicerolu, który wypełnia różne funkcje „poniżej”. w wodospadzie.
IP3 bierze udział w hormonalnym wodospadzie sygnalizacyjnym używanym przez drugie systemy komunikatora, takie jak adrenalina.
Inozytol jest rozpuszczalnym posłańcem, który wykonuje swoje funkcje w cytosolu, podczas gdy diaclglycerol jest rozpuszczalny w tłuszczu i pozostaje połączony w membranie, gdzie wykonuje również funkcje komunikatora.
W ten sam sposób w roślinach ustalono, że pochodne fosfatydyloinozytolu mają również ważne funkcje w komórkowych wodospadach sygnalizacyjnych.
Bibliografia
- Antonsson, ur. (1997). Syntaza fosfatidyloinozytolu z tkanek ssaków. Biochimica et biophysica acta.
- Luckey, m. (2008). BIOLOGIA Membrana strukturalna: z podstawami biochemicznymi i biofizycznymi. Cambridge University Press.
- Murray, r., Bender, d., Botham, k., Kennelly, s. 1., Rodwell, v., I Weil, p. (2009). Ilustrowana biochemia Harpera (28. wyd.). McGraw-Hill Medical.
- Nelson, zm. L., & Cox, m. M. (2009). Zasady biochemii lehninger. Omega Editions (Ed.).
- Vance, J. I., & Vance, D. I. (2008). Biochemia lipidów, lipoprotein i błon. W Nowe zrozumienie Biochemistry vol. 36 (Wydanie 4.). Elsevier.

