Struktura krystaliczna
- 2842
- 776
- Maksymilian Kępa
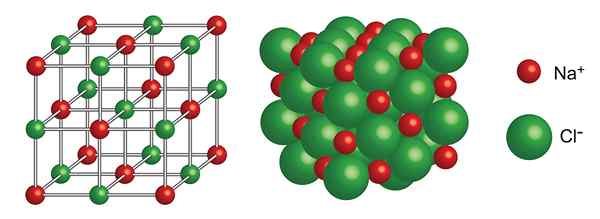
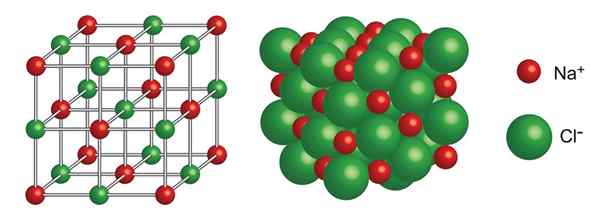 Krystaliczna struktura chlorku sodu
Krystaliczna struktura chlorku sodu Jaka jest krystaliczna struktura?
Struktura krystaliczna Odnosi się do sposobu, w jaki atomy, jony lub cząsteczki są zorganizowane lub pakowane w krystaliczne stałe, takie jak diamenty, sól (chlorek sodu) lub cukier (sacharoza).
Krystaliczne stałe powstają trzy wymiarowe sieci identycznych jednostek zwanych komórkami jednostkowymi. Przypominają one małe identyczne bloki konstrukcyjne (takie jak Layo), które wiążą się ze sobą, tworząc kryształy, które możemy zobaczyć z nagim okiem.
Struktura krystaliczna składa się z opisu kształtu tej jednolitej komórki i dokładnej pozycji, którą każdy atom ma w wspomnianej komórce.
Charakterystyka struktury krystalicznej
Są tworzone przez powtarzane komórki jednostkowe
Struktura krystaliczna polega na powtórzeniu komórki elementarnej we wszystkich kierunkach. Komórki te składają się z trzech wymiarów równoległości, których kształt i rozmiar są zdefiniowane przez trzy nazywane wektory a, b I C, i pod kątem między tymi wektorami, zwane α, β i γ.
Są to wysoce uporządkowane struktury
Struktura krystaliczna charakteryzuje się jednym z najbardziej uporządkowanych stanów. Kryształy są tak uporządkowane, że przy znajomości struktury komórki elementarnej, która zawiera tylko garść atomów, można odbudować całą strukturę szkła utworzonego przez miliony atomów, jonów lub cząsteczek.
Prezentują symetrię
Większość komórek jednostkowych, z którymi można zbudować krystaliczne stałe, ma pewien rodzaj symetrii. Oznacza to, że zawartość części komórki jest powtarzana w innej części po przeprowadzeniu rotacji, refleksji lub inwestycji.
Może ci służyć: suszarka do obrotowej: operacja, do czego jest, części, aplikacjeNa przykład, jeśli komórka jednostkowa ma płaszczyznę symetrii, oznacza to, że połowa komórki jest odzwierciedleniem drugiej.
Zależność między właściwościami materii a strukturą krystaliczną
Istnieje wiele właściwości fizycznych i chemicznych, które zależą od struktury krystalicznej:
Gęstość
W zależności od sposobu pakowania atomów w strukturze krystalicznej można uzyskać bardziej zwarte struktury lub struktury. W pierwszym przypadku uzyskano gęstą i ciężką substancję stałą, ponieważ więcej atomów jest pakowanych w mniejszą objętość.
-
Przykład
Jeśli porównamy trzy sześcienne struktury krystaliczne zwane prostymi sześciennymi (P), sześciennymi wyśrodkowanymi na twarzach (FCC) i sześciennych wyśrodkowanych na ciele (BCC) dla równych atomów, struktura BCC to 2 to 2.6 razy gęstsze niż FCC, a FCC to 1.4 razy gęstsze niż P.
Krystaliczna postać
Kształt kryształów, które możemy zobaczyć z nagim okiem, jest odbiciem struktury krystalicznej, aw szczególności komórki jednolitej. W zależności od struktury jednolitej komórki kryształy będą rosły bardziej w jednym kierunku niż w innych, co powoduje kryształy o różnych kształtach, takich jak igły, kwoty, kryształy sześciokątne itp.
Anizotropia
Właściwości fizyczne, takie jak przewodność termiczna lub elektryczna i właściwości magnetyczne materii, są często większe w kierunku materialnym niż w innym.
Nazywa się to anizotropią, a efekty te są szczególnie intensywne w strukturach krystalicznych, ponieważ są to bardzo uporządkowane i regularne struktury.
Może ci służyć: diastreomerRodzaje struktury krystalicznej
Struktury krystaliczne można klasyfikować według rodzaju komórki elementarnej, według której są one uformowane. Charakteryzują się trzema stronami, które łączą się z jedną z jego krawędzi (zwanych A, B i C) oraz kątami między tymi stronami (zwanymi α, β i γ).
Daje to 7 systemów krystalicznych. W każdym z tych krystalicznych układów można rozróżnić różne rodzaje komórek jednostkowych. W sumie istnieje 14 różnych komórek jednostkowych, które są nazywane 14 sieciami Bravais i są reprezentowane poniżej:
System sześcienny
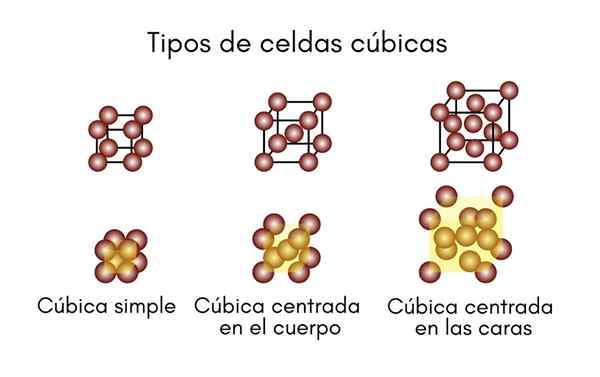
Jak sama nazwa wskazuje, komórka jednostkowa składa się z idealnej kostki. Trzy strony, A, B i C są sobie równe, a ich trzy kąty to 90 °. Ten system składa się z komórek:
- Prosty lub prymitywny sześcien.
- Sześcienne wyśrodkowane w ciele (BCC).
- Sześcienne skupione na twarzach (FCC).
System tetragonalny
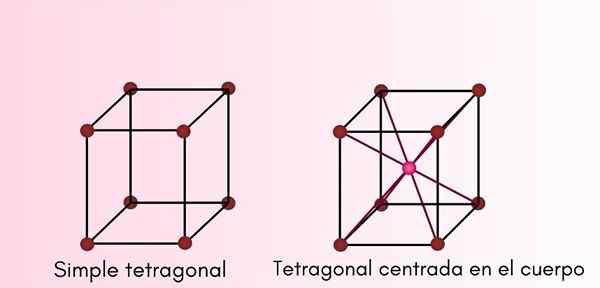
W tego rodzaju strukturze krystalicznej A i B są takie same, ale C jest inne, ale wszystkie pozostają prostopadłe do siebie. Komórki tetragonalne mogą być:
- Proste lub prymitywne tetragonalne.
- Ciało tetragonalne.
System ortorombowy
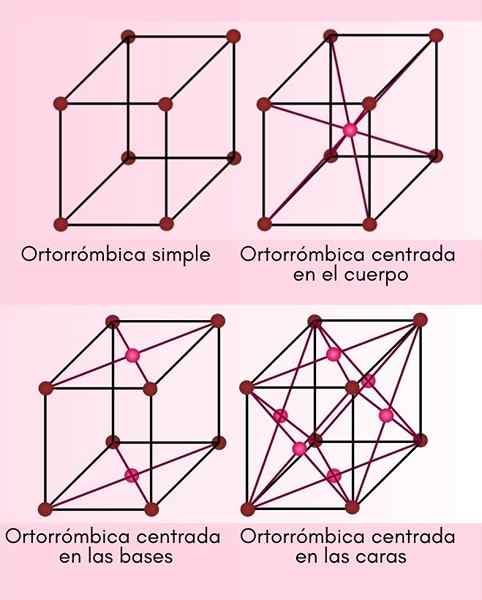
W tym systemie krystalicznym A, B i C są różne, ale nadal są do siebie prostopadłe. Istnieją 4 różne komórki ortorombowe:
- Prymitywne lub proste ortorombowe.
- Orthrome skoncentrowany na ciele.
- Baza skoncentrowana na ortermie.
- Skoncentrowany na twarzy ortorombic.
System monokliniczny
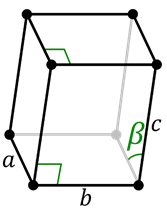 Prymitywna komórka monokliniczna
Prymitywna komórka monokliniczna 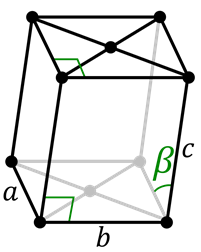 Komórka monokliniczna skoncentrowana
Komórka monokliniczna skoncentrowana System monokliniczny jest podobny do sześciokątnej, z wyjątkiem faktu, że wszystkie jego strony są różne. Istnieją dwie komórki dla układu monoklinicznego:
- Prymitywne monokliniczne.
- Podstawa monokliniczna.
System trójklinowy
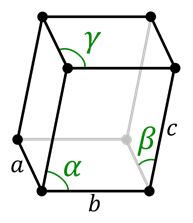 Komórka trójklinowa
Komórka trójklinowa W systemie trójkołowym nie ma symetrii. Wszystkie kąty różnią się od siebie i niekoniecznie muszą mieć 90 °. Wszystkie jego strony są również różne.
System sześciokąta
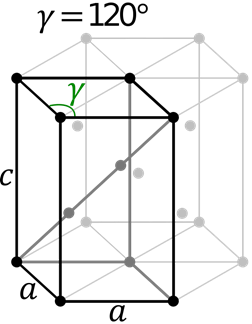 Komórka sześciokątna
Komórka sześciokątna Ta komórka zawiera boki A i B różne i różne strony C. Kąty α i β są 90 °, podczas gdy γ = 120 °.
System trygonalny lub romboyan
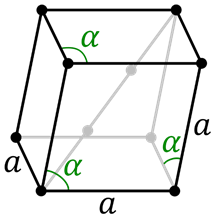 Komórka trygonalna lub romboedyczna
Komórka trygonalna lub romboedyczna Jest to szczególny rodzaj struktury podobnej do przyjmowania wiadra i rozciągania go wzdłuż dwóch przeciwnych wierzchołków. Wszystkie strony są takie same, a także ich kąty, ale nie są to 90 °.
Przykłady krystalicznych struktur
Chlorek sodu
Jego krystaliczna struktura składa się z sieci sześciennej skoncentrowanej na twarzach z 4 jednostkami NaCl dla każdej komórki elementarnej,
Żelazo alfa
Żelazo krystalizuje żelazo alfa w 768 ° C. Jego struktura jest sześcienna wyśrodkowana w ciele z 2 -krawędzią 2.86 Å (lub 286 pm)
Żelazo gamma
Jest to żelaza, która występuje między 910 ° C a 1400 ° C i ma sześcienną strukturę krystaliczną wyśrodkowaną na twarzach 3.64 Å (364 pm) krawędzi.
Diament
Diament jest jedną z najcenniejszych form węglowych i ma sześcienną strukturę krystaliczną wyśrodkowaną na twarzach (FCC), która zawiera dwa atomy węgla i 3 krawędź 3.75 Å (375 pm).
Grafit
Grafit to kolejny bardzo powszechny węgiel. W tym przypadku są to arkusze atomów węgla razem, tworząc 6 -osobowe pierścienie, co powoduje heksagonalną strukturę krystaliczną.

