Stałe formuł antoine, równania, przykłady
- 983
- 200
- Filip Augustyn
Stałe Antoine Istnieją trzy parametry, które pojawiają się w empirycznej zależności między ciśnieniem pary nasycenia a temperaturą dla czystych substancji. Zależą od każdej substancji i powinny być stałe w określonym zakresie temperatur.
Z tego zakresu stałe antoine zmieniają swoją wartość. Stałe są powiązane poprzez równanie utworzone w 1888 r. Przez francuskiego inżyniera Louisa Charlesa Antoine'a (1825–1897).
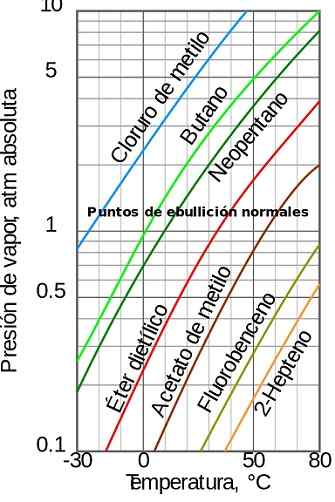
 Rysunek 1. Ciśnienie pary w zależności od temperatury. Źródło: Wikimedia Commons
Rysunek 1. Ciśnienie pary w zależności od temperatury. Źródło: Wikimedia Commons [TOC]
Wzory i równania
Najbardziej typowym sposobem wyrażania funkcji Antoine'a jest:

W tym wzorze P reprezentuje ciśnienie pary nasycenia wyrażone w milimetrach rtęci (MMHG), T jest temperaturą, która jest zmienną niezależną i jest wyrażona w ℃.
A, B i C są stałymi lub parametrami formuły antoine.
Znaczenie tego wzoru, które pomimo tego, że jest empiryczna, daje prostą ekspresję analityczną, którą można łatwo wykorzystać w obliczeniach termodynamicznych.
Formuła Antoine'a nie jest unikalna, istnieją bardziej precyzyjne wyrażenia, które są rozszerzeniami tej formuły, ale z wadą, które mają sześć lub więcej parametrów, a ich matematyczna ekspresja jest bardziej złożona, co sprawia, że są one bardzo praktykami do stosowania w obliczeniach termodynamicznych.
Para nasycenia
Ponieważ formuła Antoine mierzy nacisk pary nasycenia, konieczne jest wyjaśnienie, z czego składa się.
W szklanym ampułce lub innym pojemniku umieszczana jest płyn. Całe powietrze jest wydobywane. Zestaw jest umieszczony w kąpieli termicznej, aż do osiągnięcia równowagi.
Na początku wszystko jest płynne, ale ponieważ istnieje próżnia, najszybsze cząsteczki zaczynają rezygnować z cieczy, tworząc gaz tej samej substancji cieczy.
Może ci służyć: jednolity ruch prostoliniowy: cechy, wzory, ćwiczeniaPoprzedni proces to odparowanie A wraz ze wzrostem ciśnienia pary.
Niektóre cząsteczki pary tracą energię i wracają do fazy ciekłej substancji, jest to proces kondensacja.
Następnie dwa procesy, odparowanie i kondensacja występują jednocześnie. Kiedy pojawia się ta sama liczba ciekłych cząsteczek, które są do niego włączone, równowaga dynamiczna I w tym czasie występuje maksymalne ciśnienie pary znane jako ciśnienie nasycenia.
To to ciśnienie nasycenia pary przewiduje wzór antoine dla każdej substancji i każdej temperatury.
W niektórych ciałach stałych istnieje podobne zjawisko, gdy przechodzi z fazy stałej do sody bezpośrednio bez przechodzenia przez fazę ciekłą, w tych przypadkach można również zmierzyć ciśnienie pary nasycenia.
Nie jest łatwo ustalić model teoretyczny zaczyna się od wczesnych zasad, ponieważ zaangażowane są zmiany energii kinetycznej molekularnej, które mogą być translacyjne, obrotowe i wibracyjne, z wewnętrzną energią wiązania molekularnego. Z tego powodu stosowane są formuły empiryczne.
Jak ma stałą antoine?
Nie ma teoretycznej metody uzyskania stałych antoine, ponieważ jest to związek empiryczny.
Są one uzyskiwane z danych eksperymentalnych każdej substancji i dostosowują trzy parametry A, B i C, aby minimalizować różnicę kwadratową (metoda minimum kwadratowego) prognozy za pomocą danych eksperymentalnych.
Dla użytkownika końcowego, którzy są na ogół inżynierami chemicznymi, w instrukcjach chemii znajdują się tabele, w których podawane są stałe dla każdej substancji wskazującej maksymalne i minimalne zakres.
Może ci służyć: termometr oporności: charakterystyka, operacja, użyciaDostępne są również usługi online, które podają wartości stałych A, B i C, jak ma to miejsce w przypadku usług DDBST GMBH.
W przypadku tej samej substancji może istnieć więcej niż jeden zakres temperatur ważności. Następnie w zależności od zasięgu roboczego wybiera się jedna lub inna grupa stałych.
Trudności mogą pojawić się, jeśli zakres pracy temperatury wynosi między dwoma zakresami ważności stałych, ponieważ prognozy ciśnienia wzoru nie pokrywają się w strefie granicznej.
Przykłady
Przykład 1
Znajdź ciśnienie pary wodne przy 25 ℃.
Rozwiązanie
Skonsultowaliśmy się z tabelami w celu ustalenia stałych Antoine.
Istnieją dwa zakresy wody:
Od 1 ℃ do 100 ℃ i od 99 ℃ do 374 ℃.
Ponieważ jesteśmy zainteresowani 25 ℃, bierzemy pierwszy zakres, w którym wartość stałych Antoine są:
A = 8.07131
B = 1730,63
C = 233 426
P = 10^(8 07131 - 1730,63/(25 + 233 426))
Obliczenie wykładnika
Najpierw obliczmy wykładnik: 1 374499
P = 10^1 374499 = 23 686 mmHg = 0,031166 ATM
Analiza wyników
Te wyniki są interpretowane w następujący sposób:
Załóżmy, że czysta woda jest umieszczana w hermetycznym pojemniku, do którego powietrze zostało wyodrębnione przez pompę próżniową.
Pojemnik z wodą jest umieszczany w kąpieli termicznej w temperaturze 25 ℃, aż do osiągnięcia równowagi termicznej.
Woda w hermetycznym pojemniku odparowuje częściowo, aż do osiągnięcia ciśnienia pary nasycenia, co jest niczym innym jak ciśnieniem, w którym ustalona jest równowaga dynamiczna między fazą ciekłej wody a fazą pary.
Może ci służyć: Model atomowy Dirac Jordan: Charakterystyka i postulatyTa presja w tym przypadku okazała się 0,031166 atm na 25 ℃.
Przykład 2
Znajdź ciśnienie pary wodne przy 100 ℃.
Rozwiązanie
Skonsultowaliśmy się z tabelami w celu ustalenia stałych Antoine. Istnieją dwa zakresy wody:
Od 1 ℃ do 100 ℃ i od 99 ℃ do 374 ℃.
W tym przypadku temperatura zainteresowania jest w dwóch zakresach.
Używamy pierwszego z zakresów [1 ℃, 100 ℃]
A = 8.07131
B = 1730,63
C = 233 426
P = 10^(8 07131 - 1730,63/(100 + 233,426))
Obliczenie wykładnika
Najpierw obliczmy wykładnik: 2.8808
P = 10^1 374499 = 760,09 mmHg = 10001 atm
Następnie używamy drugiego zakresu [99 ℃, 374 ℃]
W takim przypadku stałe są
A = 8 14019
B = 1810.94
C = 244.485
P = 10^(8.14019 - 1810.94/(100 + 244.485))
Najpierw obliczmy wykładnik: 2.88324
P = 10^2.88324 = 764.2602 mmHg = 1 0056 atm
Istnieje różnica procentowa między dwoma wynikami 0,55%.
Bibliografia
- Zastosowanie praw Raoult i Dalton oraz równanie Antoine. Źródło: mój własny i starożytny.WordPress.com
- Kalkulator online formuły antoine. Odzyskane z: ddbonline.DDBST./antoinekalcion/antoinecalculaticgi.exe
- Gecousb. Termodynamika i tabele pary / stała od Antoine. Odzyskany z: gecousb.com.Iść
- Właściwości termiczne materii. Odzyskane z: WebServer.DMT.UPM.Jest
- Yaws i Yang. Stały antoine dla ponad 700 związków organicznych. Odzyskane od: użytkownika.Eng.Umd.Edu
- Wikipedia. Równanie antoine. Wyzdrowiał z Wikipedii.com
- Wikipedia. Równanie Clausius-Capeyron. Wyzdrowiał z Wikipedii.com
- WISNIAK J. Historyczny rozwój równania ciśnienia pary z Dalton Toy Antoine. Odzyskane z: link.Skoczek.com

