Ketogeneza typów ciał, synteza i degradacja
- 3596
- 586
- Herbert Wróblewski
Ketogeneza Jest to proces, w którym uzyskuje się acetooctate, β-hydroksybutiran i aceton, które razem nazywane są ciałami ketonowymi. Ten złożony i drobno regulowany mechanizm przeprowadza się w mitochondriach, z katabolizmu kwasów tłuszczowych.
Uzyskanie ciał ketonowych ma miejsce, gdy ciało podlega wyczerpującym okresom postu. Chociaż te metabolity są głównie syntetyzowane w komórkach wątroby, znajdują się je jako ważne źródło energii w różnych tkankach, takich jak mięsień szkieletowy oraz w tkankach serca i mózgu.
 Źródło: SAV VAS [CC0]
Źródło: SAV VAS [CC0] Β-hydroksybutiran i acetooctan to metabolity stosowane jako substraty w mięśniach sercowych i kory nerki. W mózgu ciała ketonowe stają się ważnymi źródłami energii, gdy ciało wyczerpało rezerwę glukozy.
[TOC]
Ogólne cechy
Ketogeneza jest uważana za bardzo ważną drogę fizjologiczną lub metaboliczną. Zasadniczo mechanizm ten jest przeprowadzany w wątrobie, chociaż wykazano, że można go przeprowadzić w innych tkankach zdolnych do metabolizowania kwasów tłuszczowych.
Tworzenie ciał ketonowych jest głównym metabolicznym wyprowadzeniem acetylo-CoA. Ten metabolit uzyskuje się z trasy metabolicznej znanej jako β-utlenianie, która jest degradacją kwasów tłuszczowych.
Dostępność glukozy w tkankach, w których występuje β-utlenianie, determinuje cel metaboliczny acetylo-CoA. W szczególności sytuacje utlenione kwasy tłuszczowe są prawie całkowicie skierowane do syntezy ciał ketonowych.
Rodzaje i właściwości ciał ketonowych
Głównym korpusem ketonicznym jest acetooctan lub kwas acetooctowy, który jest w większości syntetyzowany w komórkach wątroby. Z acetooctanu pochodzą inne cząsteczki tworzące ciała ketonowe.
Zmniejszenie kwasu acetooctowego powoduje powstanie D-β-hydroksybutiranu, drugiego ciała ketonicznego. Aceton jest trudnym związkiem do degradacji i jest wytwarzany przez spontaniczną reakcję dekarboksylacyjną acetooctanu (więc nie wymaga interwencji żadnego enzymu), gdy występuje w wysokich stężeniach we krwi we krwi.
Nominowanie ciał ketonowych zostało ułożone przez konwencję, ponieważ ściśle mówiąc β-hydroksybutiran nie ma funkcji ketonowej. Te trzy cząsteczki są rozpuszczalne w wodzie, co ułatwia transport krwi. Jego główną funkcją jest zapewnienie energii niektórym tkankom jako mięśni szkieletowych i serca.
Enzymy zaangażowane w tworzenie ciał ketonowych znajdują się głównie w wątrobie i nerkach, co wyjaśnia, że te dwie lokalizacje są głównymi producentami tych metabolitów. Jego synteza występuje tylko i wyłącznie w matrycy mitochondrialnej komórek.
Może ci służyć: sporulacja: w roślinach, w grzybach i w bakteriachPo zsyntetyzowaniu tych cząsteczek przechodzą do krwioobiegu, zwracając się do tkanek, które ich wymagają.
Synteza ciał ketonowych
Warunki ketogenezy
Metaboliczne miejsce docelowe acetylo-CoA z β-oksydacji zależy od wymagań metabolicznych organizmu. Jest to utleniane do CO2 i H2Lub za pomocą cyklu kwasu cytrynowego lub syntezy kwasów tłuszczowych, jeśli metabolizm lipidów i węglowodanów jest stabilny w organizmie.
Gdy organizm potrzebuje węglowodanów, szczawian jest stosowany do produkcji glukozy (glukoneogeneza) zamiast uruchamiania cyklu kwasu cytrynowego. Dzieje się tak, jak wspomniano, gdy ciało ma pewną niezdolność do uzyskania glukozy, w przypadkach takich jak przedłużony post lub obecność cukrzycy.
Z tego powodu do produkcji ciał ketonowych stosuje się acetylo-CoA wynikające z utleniania kwasów tłuszczowych.
Mechanizm
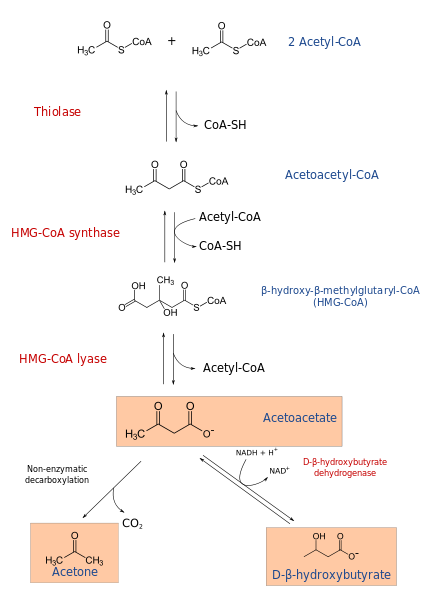
Proces ketogenezy rozpoczyna się od produktów β-utleniania: acetacetylo-CoA lub acetylo-CoA. Gdy substrat jest acetylo-CoA, pierwszy krok składa się z kondensacji dwóch cząsteczek, reakcji transferazy acetylo-CoA, w celu wytworzenia acetacetylo-CoA.
Acetacetylo-CoA jest skondensowany trzecim acetylo-CoA przez działanie syntazy HMG-COA w celu wytworzenia HMG-COA (β-hydroksy-β-metyloglutarilililil-CoA). HMG-CoA jest zdegradowane do acetooctanu i acetylo-CoA przez działanie HMG-CoA Liasa. W ten sposób uzyskuje się pierwsze ciało ketoniczne.
Acetooctan jest zmniejszony do β-hydroksybutiranu przez interwencję dehydrogenazy β-hydroksybutiratów. Ta reakcja zależy od NADH.
Głównym korpusem ketonicznym acetooctanu jest β-cetoacid, który doświadcza dekarboksylacji nieenzymatycznej. Ten proces jest prosty i produkuje aceton i co2.
Ta seria reakcji skutkuje zatem w ciałach ketonowych. Te rozpuszczalne w wodzie mogą być transportowane w prosty sposób przez krążenie krwi, bez potrzeby zakotwiczenia do struktury albuminy, podobnie jak w przypadku kwasów tłuszczowych, które są nierozpuszczalne w środkowej części wodnej.
Β-utlenianie i ketogeneza są powiązane
Metabolizm kwasu tłuszczowego wytwarza substraty ketogenezy, więc te dwa sposoby są funkcjonalnie powiązane.
Acetoacetylo-CoA jest inhibitorem metabolizmu kwasów tłuszczowych, ponieważ zatrzymuje aktywność dehydrogenazy acylo-CoA, która jest pierwszym enzymem β-oksydacji. Ponadto ćwiczy również hamowanie transferu acetylo-CoA i syntazy HMG-COA.
Enzym syntazy HMG-CoA, podlegający CPT-I (enzym zaangażowany w produkcję acyl karnityny w β-oksydacji), stanowi ważną rolę regulacyjną w tworzeniu kwasów tłuszczowych kwasów tłuszczowych.
Może ci służyć: flora i fauna Zacatecas: bardziej reprezentatywne gatunkiRegulacja β-oksydacji i jej wpływ na ketogenezę
Karmienie organizmu reguluje złożony zestaw sygnałów hormonalnych. Węglowodany, aminokwasy i lipidy spożywane w diecie osadzają się w postaci triacyloglicereno w tkance tłuszczowej. Insulina, hormon anaboliczny, interweniuje w syntezie lipidów i tworzeniu triacyloglicerel.
Na poziomie mitochondrialnym β-utlenianie jest kontrolowane przez wejście i udział niektórych substratów w mitochondriach. Enzym CPT I syntetyzuje acyl karnityny z cytozolowy ACIL ACIL.
Gdy ciało jest karmione, karboksylaza acetylo-CoA i cytrynian zwiększają poziomy CPT I, a jednocześnie zmniejsza jego fosforylację (reakcja zależna od AMP (reakcja cykliczna).
Powoduje to akumulację COA malonilu, która stymuluje syntezę kwasów tłuszczowych i blokuje jego utlenianie, zapobiegając wygenerowaniu daremnego cyklu.
W przypadku postu aktywność karboksylazy jest bardzo niska, ponieważ poziomy enzymu CPT I zostały zmniejszone, a także fosforylowane, aktywując i promując utlenianie lipidów, co następnie pozwoli na tworzenie ciał ketonowych przez acetylu -Coa.
Degradacja
Ciała ketonowe rozprzestrzeniły się poza komórkami, w których zostały zsyntetyzowane i są transportowane do tkanek obwodowych przez krwioobieg. W tych tkankach można je utleniać przez cykl kwasów trikarboksylowych.
W tkankach obwodowych β-hydroksybutiran jest utleniony do acetooctanu. Następnie obecny acetooctan jest aktywowany przez działanie enzymu transferazy 3-ZAA.
Succynil-Coa działa jako dawca CoA, który staje się bursztynianem. Aktywacja acetooctanu występuje, aby zapobiec sucynylo-CoA.
Powstały Aceoacetylo-CoA cierpi z pęknięciem tiolitycznym, powodując dwie cząsteczki acetylo-CoA, które są włączone do cyklu kwasów trikarboksylowych, lepiej znanych jako cykl Krebsa.
Komórki wątrobowe nie mają transferu 3-cotoacil-CoA, zapobiegając aktywowaniu tego metabolitu w tych komórkach. W ten sposób gwarantowane jest, że ciała ketonowe nie utleniają się w komórkach, w których zostały wyprodukowane, ale można je przenieść na tkanki, w których wymagana jest ich aktywność.
Znaczenie medyczne ciał ketonowych
W ludzkim ciele wysokie stężenia ciał ketonowych we krwi mogą powodować szczególne warunki zwane kwasicą i ketonemią.
Może ci służyć: Sphingomyeline: co to jest, struktura, funkcje, syntezaProdukcja tych metabolitów odpowiada katabolizmowi kwasów tłuszczowych i węglowodanów. Jedną z najczęstszych przyczyn stanu patologicznej ketogenezy jest wysokie stężenie ocetycznej fragmentów dikarbonikowanymi, które nie degradują na drodze utleniania kwasów trikarboksylowych.
W konsekwencji istnieje wzrost poziomu ciał ketonowych krwi powyżej 2 do 4 mg/100 N i ich obecność w moczu. Przekłada się to na zakłócenie metabolizmu pośredniego tych metabolitów.
Niektóre wady w czynnikach neuroglandularnych przysadki, które regulują degradację i syntezę ciał ketonowych, wraz z zaburzeniami metabolizmu węglowodorów, są przyczyną stanu hipercetonemii.
Cukrzyca i akumulacja ciał ketonicznych
Cukrzyca (typ 1) jest chorobą hormonalną, która powoduje wzrost produkcji ciał ketonowych. Niewystarczająca produkcja insuliny wyłącza glukozę do mięśni, wątroby i tkanki tłuszczowej, gromadząc w ten sposób we krwi.
Komórki z brakiem glukozy rozpoczynają proces glukoneogenezy i degradacji tłuszczu i białek w celu przywrócenia ich metabolizmu. W konsekwencji stężenia szczawiki zmniejszają się i zwiększają utlenianie lipidów.
Zachodzi akumulacja acetylo-CoA, która przy braku szczawiki nie może podążać ścieżką kwasu cytrynowego, a następnie powodując wysokie produkcje ciał ketonowych, charakterystyczne dla tej choroby.
Akumulacja acetonu jest wykrywana przez jego obecność w moczu i wdech ludzi, którzy przedstawiają ten stan, i w rzeczywistości jest jednym z objawów wskazujących na objawy tej choroby.
Bibliografia
- Blázquez Ortiz, C. (2004). Ketogeneza w astrocytach: charakterystyka, regulacja i możliwy papier cytoprotekcyjny (Rozprawa doktorska, Complutense University of Madryt, Publications Service).
- Devlin, t. M. (1992). Podręcznik biochemii: z korelacjami klinicznymi.
- Garrett, r. H., I Grisham, C. M. (2008). Biochemia. Thomson Brooks/Cole.
- McGry, J. D., Mannaerts, g. P., & Foster, D. W. (1977). Możliwa rola malonylo-CoA w regulacji utleniania i ketogenezy kwasu tłuszczowego wątroby. The Journal of Clinical Investigation, 60(1), 265-270.
- Melo, v., Ruiz, v. M., I cuamatzi, lub. (2007). Biochemia procesów metabolicznych. Rectte.
- Nelson, zm. L., Lehninger, a. L., & Cox, m. M. (2008). Zasady biochemii lehninger. Macmillan.
- Pertierra, a. G., Gutiérrez, c. V., I inne, c. M. (2000). Podstawy biochemii metabolicznej. Redakcyjny Tébar.
- Voet, d., & Voet, J. G. (2006). Biochemia. Wyd. Pan -american Medical.
- « Śniadanie kontynentalne, co jest i jakie jedzenie zawiera?
- Właściwości nadtlenku wapnia (CAO2), ryzyko i zastosowania »

