Benzylodorowe bencil, karbokacje, rodniki benzylowe

- 3886
- 1074
- Arkady Sawicki
On Benchilo lub benzyl Jest to powszechna grupa zastępcza w chemii organicznej, której wzorem jest C6H5Ch2- lub Bn-. Strukturalnie po prostu składa się ze połączenia grupy metylenowej, Cho2, Z grupą fenylową, c6H5; To znaczy sp3 Połączone bezpośrednio z pierścieniem benzenowym.
Dlatego grupa benchilo może być postrzegana jako aromatyczny pierścień przymocowany do małego łańcucha. W niektórych tekstach korzystanie z skrótu BN jest preferowane zamiast C6H5Ch2-, Łatwo rozpoznać go w dowolnym związku; zwłaszcza gdy jest powiązany z atomem tlenu lub azotu, O-BN lub NBN2, odpowiednio.
 Grupa Bencilo. Źródło: Ingraralhaosului [domena publiczna]
Grupa Bencilo. Źródło: Ingraralhaosului [domena publiczna] Ta grupa jest również domyślnie w serii powszechnie znanych związków. Na przykład do kwasu benzoesowego, c6H5Cooh, można uznać za benchilo, którego węgiel samochodowy3 doznał wyczerpującego utleniania; lub benzaldehyd, c6H5Cho, częściowe utlenianie; i alkohol benzylowy, c6H5Ch2Och, nawet mniej utleniony.
Kolejnym nieco oczywistym przykładem tej grupy jest tolueno, c6H5Ch3, które mogą ponieść pewną liczbę reakcji po niezwykłej stabilności wynikającej z rodników lub karbokacji benzylowych. Jednak grupa Bencilo służy ochronie grup OH lub NH2 reakcji, które niewykorzystujące produkt w celu syntezy.
[TOC]
Przykłady związków z benchilo Grupo
 Związki grupy Bencilo. Źródło: Jü [domena publiczna]
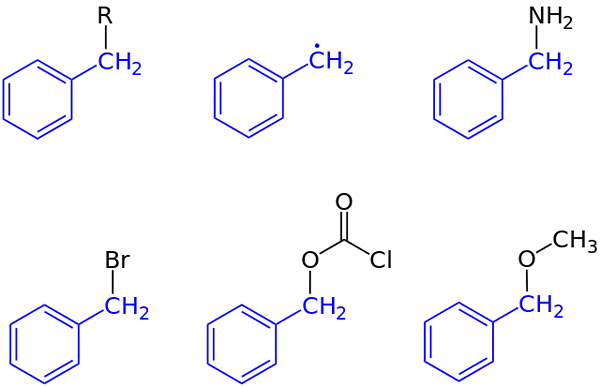
Związki grupy Bencilo. Źródło: Jü [domena publiczna] Na pierwszym obrazie pokazano ogólną reprezentację związku z grupą bencil: C6H5Ch2-R, gdzie R może być dowolnym innym fragmentem molekularnym lub atomem. Zatem różnorodne R może uzyskać dużą liczbę przykładów; Niektóre proste, inne tylko dla określonego regionu struktury lub większego zestawu.
Na przykład alkohol benzylowy wywodzi się z zastąpienia R OH: C6H5Ch2-Oh. Jeśli zamiast OH, jest to grupa NH2, Następnie powstaje związek bencelaminy: c6H5Ch2-NH2.
Może ci służyć: borobilowodorek sodu (NABH4): struktura, właściwości, zastosowaniaJeśli atom zastępujący r jest BR, powstał związek, jest bromek z ławki: C6H5Ch2-Br; R przez co2CL pochodzi z estru, chlorokarbonanu (chlorek karobenzoksylu); i och3 Pochodzi eter metylowy benzil, c6H5Ch2-Och3.
Nawet (choć w ogóle nie poprawnie), R można założyć przez samotny elektron: rodnik benzylowy, C6H5Ch2· Produkt uwalniania radykalnego R ·. Innym przykładem, chociaż nie jest on uwzględniony na obrazie, jest fenyloacetonitryl lub cyjanku, c6H5Ch2-Cn.
Istnieją związki, w których grupa łazienkowa ledwo reprezentuje określony region. Kiedy tak, skrót BN jest zwykle używany do uproszczenia struktury i jej ilustracji.
Hydrogeny benzylowe
Powyższe związki mają wspólne nie tylko pierścień aromatyczny lub fenylowy, ale także hydrogeny benzylowe; To są te, które należą do węgla SPO3.
Takie hydrogeny mogą być reprezentowane jako: Bn-ch3, Bn-ch2R lub BN-chr2. Związek BN-CR3 Brakuje mu wodoru benzylowego, a zatem jego reaktywność jest mniejsza niż reakcja.
Te hydrogeny różnią się od tych, które są zwykle powiązane z węglowym3.
Rozważmy na przykład metan, cho4, które można również napisać jako Cho3-H. Aby złamać link Cho3-H W heterolitycznym pęknięciu (tworzenie radykalne) należy dostarczyć pewną ilość energii (104 kJ/mol).
Jednak energia dla tego samego pęknięcia wiązania C6H5Ch2-H jest niższe w porównaniu z metanem (85 kJ/mol). Będąc mniej energii, oznacza, że radykalne c6H5Ch2· Jest bardziej stabilny niż Cho3·. To samo dzieje się w większym lub mniejszym stopniu z innymi hydrogenami benzylowymi.
W konsekwencji hydrogeny benzylowe są bardziej reaktywne przy generowaniu rodników lub karbokacji bardziej stabilnych niż wywołane przez inne hydrogeny. Ponieważ? Na pytanie jest odpowiedzią w następnej sekcji.
Może ci służyć: kwas benzoesowy (C6H5COOH)Benzyczne karbokacje i radykałki
Radykalne C zostało już rozważane6H5Ch2·, Brakujący karbokacja benzylowa: C6H5Ch2+. W pierwszym jest zniknięty i samotny elektron, aw drugim niedobór elektroniczny. Dwa gatunki są bardzo reaktywne i reprezentują związki przejściowe, z których pochodzą końcowe produkty reakcji.
Carbon sp3, Po utracie jednego lub dwóch elektronów w celu utworzenia odpowiednio rodnika lub karbokacji, możesz przyjąć hybrydyzację SP2 (płaszczyzna trygonalna), tak że istnieje najmniej możliwe odpychanie wśród grup elektronicznych. Ale jeśli stanie się SP2, Podobnie jak węgle pierścienia aromatycznego, może wystąpić koniugacja? Odpowiedź brzmi tak.
Rezonans w grupie Bencilo
Ta koniugacja lub rezonans jest kluczowym czynnikiem wyjaśniającym stabilność tych gatunków benzylowych lub bencil. Na poniższym obrazie ilustruje takie zjawisko:
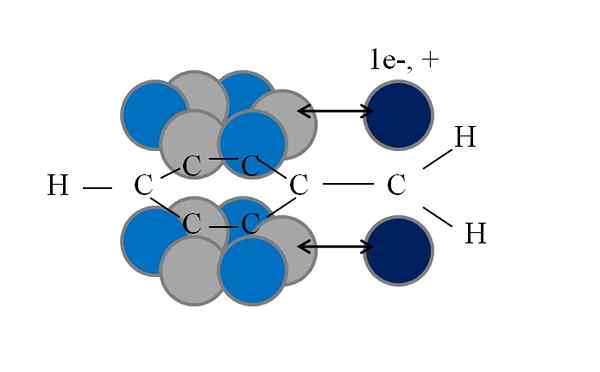 Koniugacja lub rezonans w grupie Benchilo. Pozostałe hydrogeny zostały pominięte w celu uproszczenia obrazu. Źródło: Gabriel Bolívar.
Koniugacja lub rezonans w grupie Benchilo. Pozostałe hydrogeny zostały pominięte w celu uproszczenia obrazu. Źródło: Gabriel Bolívar. Zauważ, że gdzie jeden z hydrogenów benzylowych był orbitalem P Z znikniętym elektronem (radykalne, 1e-) lub pustka (karbokacja, +). Jak widać, ten orbital P Jest równolegle do układu aromatycznego (szare i niebieskie kółka), a podwójna strzałka wskazuje na początek koniugacji.
Zatem zarówno zniknięty elektron, jak i obciążenie dodatnie mogą być przenoszone lub rozproszone przez pierścień aromatyczny, ponieważ równoległość jego orbitali sprzyja mu geometrycznie. Jednak nie znajdują się one na żadnym orbicie P pierścienia aromatycznego; Tylko u osób należących do węgli w pozycjach orto i dla CH2.
Może ci służyć: analiza ilościowa w chemii: pomiary, przygotowanieDlatego wyraźne niebieskie kółka wyróżniają się nad szarościami: w nich ujemna lub dodatnia gęstość rodnika lub karbokacji jest odpowiednio skoncentrowana.
Inne radykałowie
Warto wspomnieć, że ta koniugacja lub rezonans nie mogą wystąpić w węgle SP3 bardziej odległe od aromatycznego pierścienia.
Na przykład radykalne c6H5Ch2Ch2· Jest o wiele bardziej niestabilny, ponieważ znikniętym elektronem nie można sprzężyć z pierścieniem po złożeniu grupy2 pomiędzy i z hybrydyzacją SP3. To samo dotyczy C6H5Ch2Ch2+.
Reakcje
Podsumowując: hydrogeny benzylowe są podatne na reagowanie, albo generując radykalne lub karbokacja, co z kolei kończy się produktem końcowym reakcji. Dlatego reagują przez mechanizm SN1.
Przykład polega na bromacji toluenowej pod promieniowaniem ultrafioletowym:
C6H5Ch3 + 1/2br2 => C6H5Ch2Br
C6H5Ch2BR + 1/2BR2 => C6H5Chbr2
C6H5Chbr2 + 1/2br2 => C6H5CBR3
W rzeczywistości w tej reakcji istnieją rodniki Br ·.
Z drugiej strony sama grupa benchilo reaguje w celu ochrony grup OH lub NH2 W prostej reakcji zastępczej. Zatem alkohol Roh może być „benziladem” za pomocą bromku benchilo i innych odczynników (Koh lub Nah):
ROH + BNBR => Robn + HBR
Robn jest eterem benzylowym, do którego jego początkowa grupa OH może zostać zwrócona, jeśli zostanie poddany medium redukcyjnego. Ten eter musi pozostać niezmieniony, podczas gdy inne reakcje są przeprowadzane w związku.
Bibliografia
- Morrison, r.T. I Boyd, r. N. (1987). Chemia organiczna. (Edycja 5). Addison-Wesley Iberoamericana.
- Carey, f. DO. (2008). Chemia organiczna. (6. edycja). McGraw-Hill, Intermerica, redakcje.DO.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Chemia organiczna. Aminy. (10. edycja.). Wiley Plus.
- Wikipedia. (2019). Grupa benzylowa. Źródło: w:.Wikipedia.org
- Dr. Donald L. Robertson. (5 grudnia 2010). Fenyl lub benzyl? Odzyskane z: dom.Miracosta.Edu
- Gamini Gunawardena. (12 października 2015 r.). Karbokacja benzyliczna. Chemia librettexts. Odzyskane z: chem.Librettexts.org
- « Wyjaśnienie proporcjonalności kompozytowej, trzy złożone reguły, ćwiczenia
- Funkcje układu hematopoyetycznego, tkaniny, histologii, narządów »

