Tlenek potasu (K2O)
- 1042
- 294
- Bertrand Zawadzki
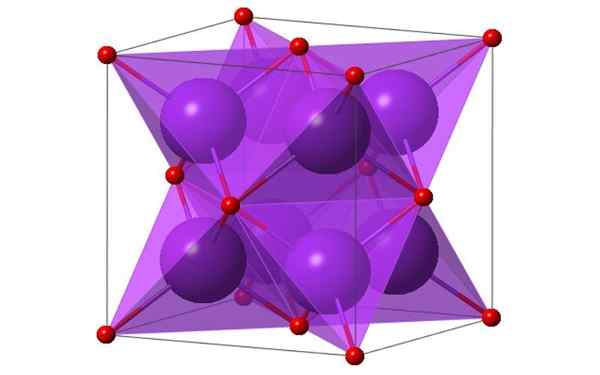
 Projekt sześcienny 4 cząsteczek tlenku potasu. Źródło: Ktlabe, Wikimedia Commons
Projekt sześcienny 4 cząsteczek tlenku potasu. Źródło: Ktlabe, Wikimedia Commons Co to jest tlenek potasu?
On Tlenek potasu, Nazywany również tlenkiem dipotazowym, jest to jonowy tlen i sól potasowa, o wzorze K2ALBO. Jest to najprostszy tlenek potasu, wysoce reaktywny i rzadko spotykany. Niektóre materiały handlowe, takie jak nawozy i cement2ALBO.
Tlenek potasu jest wytwarzany z wodorotlenku potasu (potasów kaustycznych) i metalicznego potasu 450 ° C, wytwarzając wodór molekularny zgodnie z równaniem:
2K + 2KOH ⇌ 2K2Lub + h2 (450 ° C).
Uzyskuje się również przez zmniejszenie nadtlenku potasu zgodnie z reakcją:
2K2ALBO2 → K2Lub + o2 (530 ° C).
Inną metodą uzyskiwania tlenku potasu jest podgrzewanie węglanu potasu w wysokiej temperaturze, na co wskazuje następująca reakcja:
K2WSPÓŁ3 ⇌ k2O + co₂ (t> 1200 ° C).
Jednak głównym sposobem uzyskania tlenku potasu jest ogrzewanie azotanu potasu, uzyskanie azotu cząsteczkowego, jak wskazuje następująca reakcja:
2KNO3 + 10K → 6K2Lub + n2
Fizyczne i chemiczne właściwości
- Są to kryształy czworościenne, żółtawe, bez charakterystycznego aromatu.
- Ma masę cząsteczkową 94,2 g/mol i gęstość 2,13 g/ml w 24 ° C.
- Ma temperaturę topnienia 740 ° C, chociaż zaczyna rozkładać się w 300 ° C.
- Jest odporny na ciepło i rozpuszczalny w etanolu i eterze. K2Lub krystalizuj w strukturze antyfluorytowej. Z tego powodu pozycje anionów i kationów są inwestowane w stosunek do ich pozycji w CAF2, z skoordynowanymi jonami potasowymi do 4 jonów tlenku i jonów tlenkowych koordynowanych przy 8 potasu.
- Jest to podstawowy tlenek i gwałtownie reaguje z wodą, aby wytworzyć żrący wodorotlenek potasu. Jest delikatne i pochłania wodę z atmosfery, rozpoczynając tę energiczną reakcję.
Może ci podać: azotan wapnia (CA (NO3) 2)- Utlenia odwracalnie do nadtlenku potasu w 350 ° C, reaguje gwałtownie kwasami, takimi jak kwas solny, tworząc sole potasu zgodnie z reakcją:
K2O + 2HCl → 2KCl + H₂O.
- Reaguje z dwutlenkiem azotu, tworząc azotan i azotyn potasu w temperaturach od 150 do 200 ° C:
K2O + 2no2 = Kno2 + Kno3
- Reaguj w niskich temperaturach z amoniakiem, tworząc się według reakcji i wodorotlenku potasu w zależności od reakcji:
K2O + nh3 (L) → KNH2↓ + KOH (-50 ° C).
Ryzyko
Tlenek potasu jest niestabilną substancją. Łatwo utlenia inne tlenki potasu, nadtlenku lub kwasu potasowego (KHO) (KHO). Związek nie jest paliwem, ale reaguje energicznie i egzotermicznie z wodą z tworzeniem wodorotlenku potasu (KOH).
Roztwór tlenku potasu w wodzie jest silną zasadą, reaguje gwałtownie kwasem i jest żrący. Reaguje gwałtownie z wodą wytwarzającą wodorotlenek potasu. Atakuje wiele metali w obecności wody.
Substancja jest żrący dla oczu, skóry i dróg oddechowych, a także przez spożywanie. Wdychanie aerozolu może powodować obrzęk płuc, którego objawy są często objawiane po kilku godzinach i są pogarszane przez fizyczny wysiłek.
W przypadku kontaktu wzrokowego musisz sprawdzić, czy soczewki kontaktowe są używane i natychmiast je usunąć. Oczy należy myć bieżącą wodą przez co najmniej 15 minut, z otwartymi powiekami. Można użyć zimnej wody, a nie maści o oko.
Jeśli chemikalia zetknie się z ubraniami, zachowaj je tak szybko, jak to możliwe, chroniąc własne ręce i ciało. Umieść ofiarę pod prysznicem bezpieczeństwa.
Jeśli chemikalia gromadzi się w odsłoniętej skórze, takiej jak dłonie, skóra zanieczyszczona bieżącą wodą i mydłem niebrazowym jest delikatnie myte i ostrożnie. Można użyć zimnej wody. Jeśli podrażnienie utrzymuje się, szukaj pomocy medycznej. Umyj zanieczyszczone ubrania przed ponownym użyciem.
Może ci służyć: Rubidio: History, właściwości, struktura, pozyskiwanie, użyciaJeśli kontakt skóry jest poważny, należy go umyć mydłem dezynfekującym i przykryć skórę zanieczyszczoną kremem przeciwbakteryjnym.
W przypadku inhalacji ofiara powinna mieć możliwość stania w dobrze wentylowanym obszarze. Jeśli inhalacja jest poważna, ofiara musi zostać jak najszybciej ewakuowana na bezpieczny obszar.
Poluzuj ciasne ubrania, takie jak szyje koszuli, pasy lub krawat. Jeśli ofiara jest trudna do oddychania, należy podać tlen. Jeśli ofiara nie oddycha, powstaje resuscytacja usta.
Zawsze biorąc pod uwagę, że może być niebezpieczne dla osoby, która zapewnia pomoc w resuscytacji usta, gdy wdychany materiał jest toksyczny, zaraźliwy lub żrący.
W przypadku spożycia nie wywołuje wymiotów. Poluzuj ciasne ubrania. We wszystkich przypadkach należy szukać natychmiastowej pomocy medycznej.
Aplikacje
- Wzór chemiczny K2Lub (lub po prostu k) jest używany w kilku kontekstach przemysłowych: liczby N-P-K dla nawozów, wzorów cementu i formuł szklanych.
Często nie jest używany bezpośrednio w tych produktach, ale ilość potasu jest zgłaszana pod względem równoważnym K2Lub dla każdego rodzaju stosowanych związków potasowych, takich jak węglan potasowy.
- Tlenek potasu wynosi około 83% potasu, podczas gdy chlorek potasu wynosi tylko 52%. Chlorek potasu zapewnia mniej potasu niż równa ilość tlenku potasu.
Dlatego, jeśli nawóz ma 30% chlorku potasu, jego standardowy wskaźnik potasu, oparty na tlenku potasu, wynosiłby tylko 18,8%. Jest produkowany i/lub od 10 do 100 ton rocznie tej substancji w europejskiej przestrzeni ekonomicznej.
Może ci służyć: chemia w życiu codziennym: +30 Przykłady- Substancja ta jest stosowana w chemikaliach laboratoryjnych, nawozach, polimerach i produktach fitosanitarnych. K2O Ma zastosowanie przemysłowe, które powodują produkcję innej substancji (stosowanie produktów pośrednich).
- Tlenek potasu jest stosowany w obszarach mieszanki i/lub rolnictwa, preparatu leśnictwa i połowów. Służy do produkcji chemikaliów, produktów z tworzyw sztucznych i produktów mineralnych (na przykład tynku, cementu).
- Jest używany na zewnątrz w długoterminowych materiałach z niskim uwalnianiem prędkości, na przykład w materiałach konstrukcyjnych metalu, drewna i plastiku.
- Wewnętrzne, długoterminowe materiały są stosowane z niską prędkością, takie jak meble, zabawki, materiały budowlane, zasłony, obuwie, produkty skórzane, produkty papierowe i kartonowe, sprzęt elektroniczny.
- Substancję tę można znaleźć w produktach z kamiennym materiałem, gipsem, cementu, szkła lub ceramicznym (na przykład płyty, garnki / patelnie, pojemniki do przechowywania żywności, materiał konstrukcyjny i izolacyjny).
- Tlenek potasu jest stabilnym termicznie, wysoce nierozpuszczalnym źródłem, odpowiednim do zastosowań szkła, optycznych i ceramicznych. Związki tlenkowe nie prowadzą energii elektrycznej.
- Jest również stosowany w jasnych elementach strukturalnych w zastosowaniach lotniczych i elektrochemicznych, takich jak akumulatory paliwowe, w których przewodność jonowa wykazuje.
Bibliografia
- Elementy amerykańskie (s.F.). Tlenek potasu. Odzyskane z amerykańskich.com.
- Tlenek dipasowy. Wyzdrowiał z Echę.Europa.UE.

