Struktura tlenku cynku (ZnO), właściwości, zastosowania, ryzyko
- 2283
- 139
- Maksymilian Kępa
On tlenek cynku Jest to związek nieorganiczny, którego wzorem chemicznym jest ZnO. Składa się tylko z jonów Zn2+ I2- w stosunku 1: 1; Jednak jego krystaliczna sieć może stanowić wakat lub2-, który daje wady strukturalne miejsce zdolne do zmiany kolorów jego syntetycznych kryształów.
W handlu jest nabywana jako zakurzona biała stała (niższy obraz), który występuje bezpośrednio z utleniania metalicznego cynku przez proces francuski; lub podlega zmniejszeniu węgla do rudy cynku, tak aby ich opary utleniają się i zakończyć zestalanie.
 Zegar z tlenkiem cynku. Źródło: Adam Rędzikowski [CC BY-SA 4.0 (https: // creativeCommons.Org/licencje/nabrzeże/4.0)]
Zegar z tlenkiem cynku. Źródło: Adam Rędzikowski [CC BY-SA 4.0 (https: // creativeCommons.Org/licencje/nabrzeże/4.0)] Inne metody przygotowania ZnO składają się z wytrącania ich wodorotlenku, Zn (OH)2, Z wodnych roztworów soli cynku. Również drobne filmy lub zróżnicowane morfologicznie nanocząstki mogą być syntetyzowane za pomocą bardziej wyrafinowanych technik, takich jak osadzanie chemiczne ich oparów.
Ten metaliczny tlenek znajduje się w naturze jako minerał zinitowy, którego kryształy są zwykle żółte lub pomarańczowe z powodu zanieczyszczeń metali. Kryształy ZnO charakteryzują się byciem piezoelektrycznym, termochromatycznym, luminescencyjnym, polarnym, a także bardzo szerokim pasmem energii we właściwościach półprzewodników.
Strukturalnie, jest izomorficzny do siarczku cynku, Zns, przyjmuje kryształy sześciokątne i sześcienne, podobne do odpowiednio Wurzita i Blenda. W nich istnieje pewien kowalencyjny charakter w interakcjach między Zn2+ I2-, co powoduje heterogeniczny rozkład obciążeń w krysztale ZnO.
Badania właściwości i zastosowania ZnO obejmują pola fizyki, elektroniki i biomedycyny. Jego najprostsze i najbardziej codzienne zastosowania pozostają niezauważone w składzie kremów do twarzy i produktów higieny osobistej, a także w filmie przeciwsłonecznym.
[TOC]
Struktura
Polimorfy
ZnO krystalizuje w normalnych warunkach ciśnienia i temperatury w strukturze sześciokątnej Wurzytu. W tej strukturze jony Zn2+ I2- Są one ułożone w alternatywne warstwy, dzięki4 lub Ozn4, odpowiednio.
Ponadto, stosując „szablon” lub podtrzymanie sześcienne, ZnO można krystalizować w sześciennej strukturze mieszanki cynku; który, podobnie jak Wurzita, odpowiada strukturom izomorficznym (identycznym w przestrzeni, ale z różnymi jonami) siarczku cynkowego, Zns.
Oprócz tych dwóch struktur (Wurzita i Blenda), ZnO pod wysokim ciśnieniem (około 10 GPa) krystalizuje się w strukturze SAL GEMA, tak samo jak NaCl.
Może Ci służyć: elektroda odniesienia: charakterystyka, funkcja, przykładyInterakcje
Interakcje między Zn2+ I2- Prezentują pewien charakter kowalencji, więc częściowo występuje wiązanie kowalencyjne Zn-O (oba atomy z hybrydyzacją SP3), a ze względu na zniekształcenie tetrahedry przejawiają moment dipolowy, który dodaje do jonowych atrakcji kryształów ZnO.
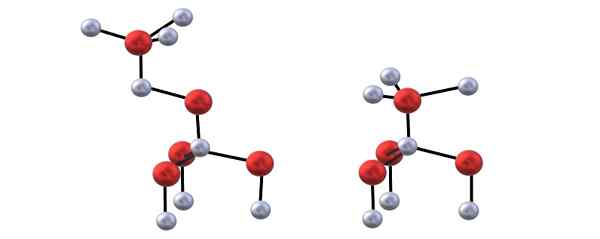
 Struktura Blenda (po lewej) i Wurzita (po prawej) ZnO. Źródło: Gabriel Bolívar.
Struktura Blenda (po lewej) i Wurzita (po prawej) ZnO. Źródło: Gabriel Bolívar. Masz górny obraz, aby wizualizować wyżej wymienione tetrahedry dla struktur ZnO.
Różnica między strukturami Blenda i Wurzita również polega na tym, co widać z góry. Na przykład w Wurzicie widać, że białe kule (Zn2+) są tuż nad czerwonymi kulami (lub2-). Z drugiej strony w sześciennej strukturze Blenda nie zdarza się, ponieważ istnieją trzy warstwy: a, b i c zamiast dwóch.
Morfologia nanocząstek
Kryształy Zno, chociaż mają tendencję do wurzan sześciokątnych, jeśli chodzi o morfologię ich nanocząstek to inna historia. W zależności od parametrów i metod syntezy mogą one przyjmować formy tak różnorodne, jak pręty, płytki, liście, kule, kwiaty, pasy, igły, między innymi.
Nieruchomości
Wygląd fizyczny
Solidny biały, toalety i gorzki smak solidny. W naturze można go skrystalizować, z zanieczyszczeniami metali, jako minerał cynkuta. Jeśli takie kryształy są białe, mają termochromizm, co oznacza, że kiedy zmieniają zabarwienie: od białego na żółty.
Podobnie, ich syntetyczne kryształy mogą prezentować czerwonawe lub zielonkawe zabarwienie w zależności od ich stechiometrycznego składu tlenu; to znaczy dziury lub wolne miejsca spowodowane brakiem anionów lub2- bezpośrednio wpływa na sposób interakcji światła z sieciami jonowymi.
Masa cząsteczkowa
81 406 g/mol
Temperatura topnienia
1974 ºC. W tej temperaturze rozkład termiczny cierpi przez uwalnianie cynku i tlenu cząsteczkowego lub tlenu gazowego.
Gęstość
5.1 g/cm3
Rozpuszczalność wody
ZnO jest praktycznie nierozpuszczalne w wodzie, ledwo powodując roztwory o stężeniu od 0,0004% do 18 ° C.
Anfoteryzm
ZnO może reagować zarówno z kwasami, jak i zasadami. Kiedy reaguje z kwasem w roztworze wodnym, jego rozpuszczalność wzrasta, gdy powstaje rozpuszczalna sól w miejscu, w którym Zn2+ kończy się kompleks z cząsteczkami wody: [Zn (OH2)6]2+. Na przykład reaguje z kwasem siarkowym, wytwarzając siarczan cynku:
ZnO + H2południowy zachód4 → Znso4 + H2ALBO
Podobnie reaguje z kwasami tłuszczowymi dla tworzy ich odpowiednie sole, takie jak stearynian i cynk palmitynian.
Może ci służyć: nieodwracalna reakcja: cechy i przykładyA kiedy reaguje z podstawą, w obecności wody, powstają sole wirowe:
ZnO + 2NAOH + H2O → na2[Zn (OH)4]
Pojemność cieplna
40,3 j/k · mol
Bezpośrednia luka energetyczna
3,3 eV. Wartość ta jest dokonana przez szerokopasmowy półprzewodnik, zdolny do działania pod intensywnymi pólami elektrycznymi. Przedstawia również cechy bycia półprzewodnikiem typu N, który nie był w stanie wyjaśnić powodów, dla których istnieje dodatkowy udział elektronów w jego strukturze.
Tlenek ten wyróżnia się jego właściwościami optycznymi, akustycznymi i elektronicznymi, dzięki któremu jest uważany za kandydata do potencjalnych zastosowań związanych z opracowaniem urządzeń optoelektronicznych (czujniki, lasery, komórki fotowoltaiczne). Powód takich nieruchomości wymyka się z dziedziną fizyki.
Aplikacje
Leczniczy
Pięć tlenków zastosowano jako dodatek w licznych białych kremach do leczenia podrażnień, acnes, zapalenia skóry, otarcia i pęknięć w skórze. W tym obszarze jego zastosowanie do złagodzenia podrażnień spowodowanych pieluchami u skórki dla dzieci jest popularne.
Jest także elementem kremu przeciwsłonecznego, ponieważ wraz z nanocząstkami dwutlenku tytanu2, Pomóż zablokować promieniowanie ultrafioletowe słońca. Podobnie działa jako grubszy środek, więc jest w pewnym wyraźnym makijażu, balsamach, emaliach, talkach i mydłach.
Z drugiej strony ZnO jest piętnastu źródłem stosowanym w suplementach diety i produktach witaminowych, a także w zbóż.
Przeciwbakteryjny
Zgodnie z morfologią jego nanocząstek, ZnO można aktywować pod promieniowaniem ultrafioletowym w celu wytworzenia nadtlenków wodoru lub gatunków reaktywnych, które osłabiają błony komórkowe mikroorganizmów.
Kiedy tak się dzieje, pozostałe nanocząstki ZnO przekraczają cytoplazma i zaczynają oddziaływać z kompendium biomolekuł, które tworzą komórkę, w wyniku czego w konsekwencji apoptoza.
Dlatego nie wszystkie nanocząstki mogą być stosowane w kompozycjach filtrów przeciwsłonecznych, ale tylko te, które nie mają aktywności przeciwbakteryjnej.
Produkty z tego typu ZnO są przydzielane, pokryte rozpuszczalnymi materiałami polimerowymi, do leczenia infekcji, ran, wrzodów, bakterii, a nawet cukrzycy.
Pigmenty i powłoki
Pigment znany jako Cinco Blanco to ZnO, który jest dodawany do kilku obrazów i powłok w celu ochrony metalowych powierzchni przed korozją, gdzie są one nakładane. Na przykład uzależnione powłoki ZnO są używane do ochrony ocynkowanego żelaza.
Z drugiej strony powłoki te zostały również zastosowane na szklance okien, aby zapobiec penetrowaniu ciepła (jeśli jest za granicą) lub wejść (jeśli w środku). Chroni także niektóre materiały polimeryczne i tekstylne przed pogorszeniem się przez działanie promieniowania słonecznego i ciepła.
Może ci podać: potas (k)Bioobrazowanie
Luminescencja nanocząstek ZnO została zbadana tak, aby była stosowana w bioimarowaniu, badając w ten sposób przez niebieskie, zielone lub pomarańczowe światła, które promieniują, wewnętrzne struktury komórek.
Przyłączeniowy
ZnO uważa również, że zastosowanie jako dodatek w gumach, cementach, materiałach zębowych, szkła i ceramice, ze względu na niższą temperaturę topnienia, a zatem zachowuje się jak środek założycielski.
Eliminator siarkowodoru
ZnO eliminuje nieprzyjemne gazy H H2S, pomaganie w odejściu do niektórych emanacji Gase:
ZnO + H2S → Zns + H2ALBO
Ryzyko
Tlenek zięba jako taki jest nietoksycznym i nieszkodliwym związkiem, więc ostrożna manipulacja jego stałą nie reprezentuje żadnego ryzyka.
Problem leży jednak w jego dymie, ponieważ chociaż w wysokich temperaturach rozkłada się, opary RAV kończą zanieczyszczenie płuc i powodują rodzaj „metalowej gorączki”. Ta choroba charakteryzuje się objawami kaszlu, gorączki, poczuciem ucisku w klatce piersiowej i ciągłym metalicznym smakiem w ustach.
Cancerigen nie jest też, a kremów, które go zawierają, nie wykazały, że zwiększają wchłanianie cynku w skórze, tak aby słońce oparte na ZnO są uważane za bezpieczne; chyba że istnieją reakcje alergiczne, które w tym przypadku muszą powstrzymać jego użycie.
Jeśli chodzi o niektóre nanocząstki przeznaczone do zwalczania bakterii, mogą one wywierać negatywne skutki, jeśli nie zostaną odpowiednio przetransportowane do miejsca działania.
Bibliografia
- Shiver & Atkins. (2008). Chemia nieorganiczna. (Czwarta edycja). MC Graw Hill.
- Wikipedia. (2019). Tlenek cynku. Źródło: w:.Wikipedia.org
- Hadis Morkoç i ümit Özgur. (2009). Tlenek cynku: fundamentalna, materiały i technologia urządzeń. [PDF]. Odzyskane z: aplikacja.Wiley-vch.z
- Parihar, m. Raja i R. Paulose. (2018). Krótki przegląd właściwości strukturalnych, elektrycznych i elektrochemicznych nanocząstek tlenku cynku. [PDF]. Odzyskane z: ipme.Ru
- DO. Rodnyi i ja. V. Khodyuk. (2011). Właściwości optyczne i luminescencyjne tlenku cynku. Odzyskane z: arxiv.org
- Siddiqi, k. S., Ur Rahman, do., Tajuddin i Husen, a. (2018). Właściwości nanapartów tlenku cynku i aktywności ES przeciwko drobnoustrojom. Nanoscale Research Letters, 13 (1), 141. Doi: 10.1186/S11671-018-2532-3
- Chemikalia. (2019). Tlenek cynku. Odzyskane z: chemicalsafetyfacts.org
- Jinhuan Jiang, Jiang PI i Jiye Cai. (2018). Postęp nanocząstek tlenku cynku do zastosowań biomedycznych. Chemia i zastosowania bioinorganic, vol. 2018, identyfikator artykułu 1062562, 18 stron. doi.Org/10.1155/2018/1062562
- « Struktura nadtlenku wodoru (H2O2), właściwości, stosowanie, uzyskiwanie
- Struktura siarczanu sodu (Na2SO4), właściwości, stosowanie, uzyskiwanie »

