Co to jest, schemat energii molekularnej i ćwiczenia
- 3156
- 206
- Matylda Duda
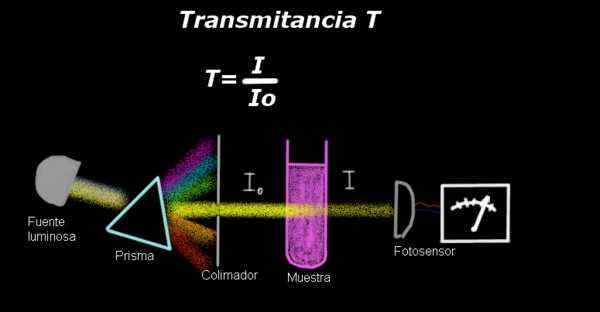
transmitancja Optyka to iloraz między wschodzącą intensywnością światła a incydentem o intensywności światła na próbce półprzezroczystego roztworu, który został oświetlony światłem monochromatycznym.
Nazywa się fizyczny proces przejścia światła przez próbkę Lumowinous Transmission i transmitancja Jest to miara transmisji światła. Przekazanie jest ważną wartością do określenia stężenia próbki, która jest ogólnie rozpuszczona w rozpuszczalniku, takim jak woda lub alkohol, między innymi.
 Rysunek 1. Montaż do pomiaru transmitancji. Źródło: f. Zapata.
Rysunek 1. Montaż do pomiaru transmitancji. Źródło: f. Zapata. Electro-fotometr mierzy prąd proporcjonalny do intensywności światła, który wpływa na jego powierzchnię. Aby obliczyć transmitancję, sygnał intensywności odpowiadający samemu rozpuszczalnikowi jest ogólnie mierzony Io.
Następnie próbka rozpuszczona w rozpuszczalniku z tymi samymi warunkami oświetlenia, a zmierzony sygnał przez elektrootometr jest oznaczony, ponieważ jest oznaczona jako Siema, Wówczas przekaz jest obliczany zgodnie z następującym wzorem:
T = i / ialbo
Należy zauważyć, że transmitancja jest bezwymiarową ilością, ponieważ jest miarą intensywności światła próbki w stosunku do intensywności transmisji rozpuszczalnika.
[TOC]
Co to jest transmitancja?
Wchłanianie światła w medium
Gdy światło przechodzi przez próbkę, część energii światła jest wchłaniana przez cząsteczki. Transmitancja jest makroskopową miarą zjawiska, które występuje na poziomie molekularnym lub atomowym.
Światło to fala elektromagnetyczna, energia, którą transportuje, znajduje się w polu elektrycznym i magnetycznym fali. Te pola oscylacyjne oddziałują z cząsteczkami substancji.
Może ci służyć: Rutherford Atomic Model: History, Experiments, PostulatesEnergia transportu fali zależy od jej częstotliwości. Światło monochromatyczne ma tylko jedną częstotliwość, a białe światło ma zakres częstotliwości lub spektrum.
Wszystkie częstotliwości fali elektromagnetycznej podróżują w próżni z tą samą prędkością 300000 km/s. Jeśli oznaczamy przez C Przy prędkości światła w próżni związek między częstotliwością F i długość fali λ Jest:
C = λ⋅f
Jak C Jest to stała przy każdej częstotliwości odpowiada jej odpowiednim długości fali.
Aby zmierzyć transmitancję substancji, stosuje się regiony widocznego widma elektromagnetycznego (380 nm przy 780 nm), obszar ultrafioletowy (180 do 380 nm) i w podczerwieni (780 nm do 5600 nm)
Prędkość propagacji światła w pożywce materiałowej zależy od częstotliwości i jest mniejsza niż C. To wyjaśnia dyspersję w pryzmatach, z którym częstotliwości tworzące białe światło można oddzielić.
Molekularna teoria absorpcji światła
Atomy i cząsteczki mają kwantyzowane poziomy energii. W temperaturze pokojowej cząsteczki są na najniższym poziomie energii.
Foton jest cząsteczką kwantową związaną z falą elektromagnetyczną. Energia fotonowa jest również kwantyzowana, to znaczy foton częstotliwości F Ma energię podaną przez:
E = H⋅f
Gdzie H Jest to stała Plancka, której wartość wynosi 6,62 × 10^-34 jhy.
Światło monochromatyczne to wiązka fotonów o częstotliwości i danej energii.
Cząsteczki pochłaniają fotony, gdy ich energia pokrywa się z różnicą niezbędną do przeniesienia cząsteczki do wyższego poziomu energii.
Przejścia energii przez wchłanianie fotonów w cząsteczkach mogą być kilku rodzajów:
Może ci służyć: silnik klatki wiewiórki1- Przejścia elektroniczne, gdy elektrony orbitali molekularnych przechodzą na orbital o większej energii. Przejścia te zwykle występują w zakresie widzialnym i ultrafioletowym i są najważniejsze.
2- Przejścia wibracyjne, energie wiązań molekularnych są również kwantyzowane, a gdy foton obszaru podczerwieni jest wchłaniany, cząsteczka przechodzi do wyższego stanu energii wibracyjnej.
3- Przejścia obrotowe, gdy wchłanianie fotonu prowadzi do cząsteczki do stanu obrotowego większej energii.
Schemat energii molekularnej
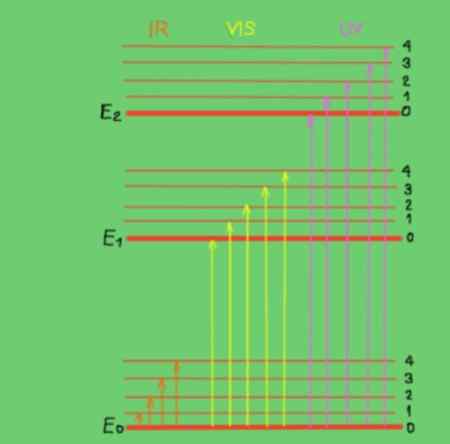
Przejścia te są lepiej rozumiane z diagramem energii molekularnej pokazanym na rycinie 2:
 Rysunek 2. Schemat energii molekularnej. Źródło: f. Zapata.
Rysunek 2. Schemat energii molekularnej. Źródło: f. Zapata. Na schemacie linie poziome reprezentują różne poziomy energii molekularnej. Linia E0 jest fundamentalnym lub niższym poziomem energii. Poziomy E1 i E2 to poziomy wzbudzone większej energii. Poziomy E0, E1, E2 odpowiadają stanom elektronicznym cząsteczki.
Podpokłania 1, 2, 3, 4 w ramach każdego poziomu elektronicznego odpowiadają różnym stanom wibracji odpowiadające każdemu poziomowi elektronicznemu. Każdy z tych poziomów ma najlepsze podziały, które nie są pokazane, które odpowiadają stanom obrotowym związanym z każdym poziomem wibracyjnym.
Schemat pokazuje pionowe strzałki reprezentujące energię fotonów w zakresie podczerwieni, widocznych i ultrafioletowych. Jak widać, fotony w podczerwieni nie mają wystarczającej energii, aby promować przejścia elektroniczne, zamiast widzialnego promieniowania i ultrafioletu Tak.
Gdy padające fotony wiązki monochromatycznej pokrywają się w energii (lub częstotliwości) z różnicą energii między stanami energii molekularnej, wówczas zachodzi wchłanianie fotonów.
Może ci służyć: skale termometryczneCzynniki w zależności od transmitancji
Zgodnie z tym, co zostało powiedziane w poprzedniej sekcji, przekazanie będzie następnie zależeć od kilku czynników, w których możemy wymienić:
1- częstotliwość, z jaką próbka oświetla.
2- Rodzaj cząsteczek, które chcesz przeanalizować.
3- Stężenie roztworu.
4- Długość ścieżki przejechana przez wiązkę światła.
Dane eksperymentalne wskazują, że przekazanie T zmniejsza się wykładniczo wraz ze stężeniem C I z długością L ścieżki optycznej:
T = 10-A⋅C⋅l
W poprzednim wyrażeniu Do Jest to stała, która zależy od częstotliwości i rodzaju substancji.
Ćwiczenie rozwiązane
Ćwiczenie 1
Próbka wzoru określonej substancji ma stężenie 150 mikromole na litr (μM). Po mierzeniu transmisji z 525 nm, uzyskuje się transmisja 0 0.4.
Inna próbka tej samej substancji, ale o nieznanym stężeniu ma transmitancję 0.5, mierzone przy tej samej częstotliwości i z tą samą grubością optyczną.
Obliczyć stężenie drugiej próbki.
Odpowiedź
Transmitancja t rozpada wykładniczo ze stężeniem C:
T = 10-B⋅l
Jeśli weźmiesz logarytm poprzedniej równości, pozostaje to:
log t = -B⋅c
Podzielanie członka na członka poprzedniej równości zastosowanej do każdej próbki i wyczyszczenie nieznanego stężenia pozostaje:
C2 = c1⋅ (log t2 / log t1)
C2 = 150 μm⋅ (log 0.5 / log 0.4) = 150 μm⋅ (-0.3010 / -0.3979) = 113.5 μm
Bibliografia
- Atkins, str. 1999. Chemia fizyczna. Omega Editions. 460-462.
- Przewodnik. Transmitancja i absorbancja. Odzyskane z: chemii.Laguia2000.com
- Toksykologia środowiskowa. Transmitancja, absorbancja i prawo Lamberta. Odzyskane z: repozytorium.Innovationumh.Jest
- Fizyka przygodowa. Absorbancja i transmitancja. Odzyskane z: rpfisica.Blogspot.com
- Sistofotometria. Odzyskane z: chem.Librettexts.org
- Toksykologia środowiskowa. Transmitancja, absorbancja i prawo Lamberta. Odzyskane z: repozytorium.Innovationumh.Jest
- Wikipedia. Transmitancja. Odzyskane z: Wikipedia.com
- Wikipedia. Spektrofotometria. Odzyskane z: Wikipedia.com

