Döbereiner triady
- 867
- 112
- Paweł Malinowski
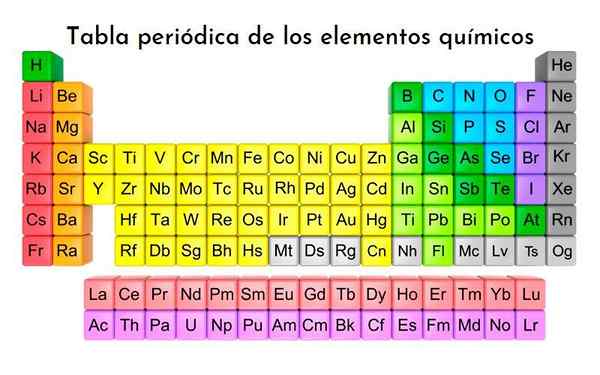
 Okresowa tabela pierwiastków, wszystkie odkryte dotychczasowe elementy chemiczne są klasyfikowane. Z licencją
Okresowa tabela pierwiastków, wszystkie odkryte dotychczasowe elementy chemiczne są klasyfikowane. Z licencją Jakie są triady Döbereinera?
Döbereiner triady Są pierwszym eksperymentem, w którym pogrupowano trzy elementy chemiczne, które mają podobne cechy, łącząc je z ciężarami atomowymi. Są częścią 118 pierwiastków chemicznych, będąc różnorodnością pokazanych reakcji i ich związków ich najbardziej znaczący wygląd.
Ideą klasyfikacji elementów jest właściwe radzenie sobie z ich właściwościami chemicznymi bez opracowywania zestawu reguł i teorii dla każdego z nich.
Jego okresowa klasyfikacja dała niezwykle użyteczne systematyczne ramy do ich skorelowania zgodnie z kilkoma bardzo prostymi i logicznymi wzorami.
Elementy są systematycznie ułożone w rzędach i kolumnach o rosnących liczbach atomowych, a przestrzeń do nowych odkryć została zarezerwowana.
W 1815 r. Znano tylko około 30 elementów. Chociaż dostępnych było wiele informacji na temat tych i ich związków, nie było widocznego porządku.
Podjęto kilka prób znalezienia zamówienia, jednak było to trudne.
Odkryj triady Döbereinera
Naukowiec Johann Wolfgang Döbereiner (1780–1849) dokonał ważnych ustaleń dotyczących regularności liczbowej wśród ciężarów atomowych pierwiastków. Jako pierwszy zauważył istnienie kilku grup trzech elementów, które nazwał Triady, które wykazały podobieństwa chemiczne.
Elementy te ujawniły ważną relację liczbową, ponieważ kiedyś zamówiły się zgodnie z ich równoważną lub atomową masą, waga elementu centralnego okazała się przybliżoną średnią z dwóch pozostałych elementów w triadzie.
Może ci służyć: fosforan sodu: struktura, właściwości, synteza, zastosowaniaW 1817 r.
Zatem, gdy uwzględniono tlenki wapnia, strontu i baru, równoważna masa tlenku strontu była w przybliżeniu średniej tlenku wapnia i tlenku baru. Mówi się, że trzy elementy, o których mowa, stront, wapń i bar, tworzą triadę.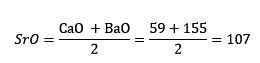
Chociaż Döbereiner pracował z pesos, które zostały wydedukowane z niewielkich rygorystycznych metod eksperymentalnych, ale na razie obowiązują, ich wartości są ściśle dobre.
Obserwacja Döbereinera miała niewielki wpływ na świat chemiczny, ale potem stała się bardzo wpływowa. Obecnie jest to uważane za jednego z pionierów rozwoju systemu okresowego.
Dwanaście lat później, w 1829 r., Döbereiner dodał trzy nowe triady, które pokazano poniżej:
Grupa halogenowa
Chlor, brom i jod mają podobne właściwości chemiczne i tworzą triadę. Te elementy są bardzo reaktywnymi metaliami. Jeśli są wymienione w kolejności rosnącej masy względnej, są one w kolejności malejącej reaktywności. Bromo ma pośrednią masę atomową między chlorem i jodem.

Masa atomowa średniej bromu.
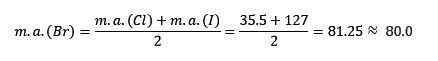
Średnia uzyskana wartość jest zbliżona do masy atomowej bromu (BR).
Podobieństwa w właściwościach chemicznych:
1. Wszystkie są nie -metalowe.
2. Wszystkie reagują z wodą w celu tworzenia kwasów (na przykład w: HCl, HBR, HF).
Może ci służyć: biodiesel: historia, właściwości, typy, zalety, wady3. Każdy ma walencję jednego (na przykład w: HCL, HBR, HF).
4. Wszystkie reagują z metali alkalicznych, tworząc sole neutralne (na przykład NaCl, Nabab, Nai)
Grupa metali alkalicznych
Lit, sód i potas mają podobne właściwości chemiczne i tworzą triadę. Te elementy są miękkie i lekkie, ale bardzo reaktywne metale.
Jeśli są wymienione w kolejności rosnącej względnej masy atomowej, są one również w kolejności rosnącej reaktywności. Sód ma pośrednią masę atomową między litem a potasem.

Masa atomowa pierwiastka środkowego sodu (Na) jest równa średniej masy atomowej litu (Li) i potasu (K).
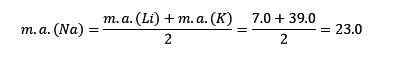
Podobieństwa w właściwościach chemicznych:
1. Wszystkie są metale.
2. Wszystkie reagują z wodą, tworząc roztwory alkaliczne i wodorowe.
3. Każdy ma Valencia de One (na przykład w: Licl, NaCl, KCl).
4. Jego węglany są odporne na rozkład termiczny.
Grupa Calcogenów lub amfumów
Siarka, selen i teluro mają podobne właściwości chemiczne i tworzą triadę. Selen ma pośrednią masę atomową między siarką a teluro.

Masa atomowa średniego elementu selenu (SE) jest równa średnim masom atomowym siarki i teluro (TE).
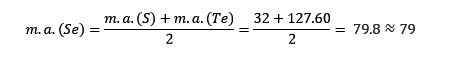
Po raz kolejny uzyskana średnia wartość jest zbliżona do ciasta atomowego selenu (SE).
Podobieństwa w właściwościach chemicznych:
1. Kombinacje z hydrogenami tych elementów powodują toksyczne gazy.
2. Każdy z tych elementów ma 6 elektronów walencyjnych.
3. Cechy metalu rosną wraz ze wzrostem liczby atomowej.
Döbereiner ostrzegł również, że aby być ważnym, Triady musiały ujawnić relacje chemiczne między elementami, a także relacje liczbowe.
Może ci podać: chloran potasowy (KCLO3)Z drugiej strony odmówił grupowania fluoru wraz z chlorem, bromem.
Niechętnie rozważał pojawienie się triadów między elementami odmiennymi, takimi jak azot, węgiel i tlen, chociaż wykazali znaczącą triadyczną zależność liczbową.
Praca Döbereinera koncentrowała się na relacjach między elementami triady, ale nie dała pojęcia o związku między nimi.
Wystarczy powiedzieć, że dochodzenie Döbereinera określiło pojęcie triadów jako potężnej koncepcji, które wkrótce wzięło pod uwagę kilka innych chemikaliów.
W rzeczywistości triady Döbereiner reprezentowały pierwszy krok do grupowania elementów w kolumny pionowe w tabeli okresowej, a tym samym ustanowić system wyjaśniający właściwości chemiczne i ujawnia fizyczne relacje pierwiastków.
Ekspansja triad
Inne chemikalia rozszerzyły triady Döbereinera o więcej niż oryginalne trzy elementy. Na przykład fluorek dodano do górnej części triadowej zawierającej chlor, brom i jod.
Wystąpiły inne „triady”, takie jak ten, który zawierał tlen, siarka, selen i telurio. Ale nie było systemu, który koreluje ich jak całość.
Jedną z głównych niedogodności było to, że wiele względnych mas atomowych było nadal błędnych.
Bibliografia
- Johann Wolfgang Döbereiner. Odzyskane z Britannica.com.
- Jaka jest grupa 16 stolika okresowego? Jak używane są te elementy? Odzyskano z Quora.com.

