Struktura pentahydratu siarczanu miedzi, właściwości,

- 3224
- 378
- Paweł Malinowski
On Siarczan miedzi pentahydrate Jest to związek nieorganiczny utworzony przez miedź (Cu), siarkę, tlen (O) i wodę (H (H (H2ALBO). Zawiera jony miedzi (II) (Cu2+) i siarczan (więc42-). Jego formuła chemiczna to cuso4 •5h2ALBO.
W naturze tworzy Chalcantita lub Mineral Calcant, zwany także Chalclasa lub Calclasa. Jest to niebieska krystaliczna substancja stała.
 Siarczan miedzi siarczan miedzi4 •5h2ALBO. Autor: überraschungsbilder. Źródło: Wikimedia Commons.
Siarczan miedzi siarczan miedzi4 •5h2ALBO. Autor: überraschungsbilder. Źródło: Wikimedia Commons. Jest stosowany jako uzupełnienie odżywcze dla niektórych zwierząt, takich jak przeżuwacze, świnie i drobi. W rolnictwie służy jako pestycyd. W działaniach wydobywczych pozwala odzyskać inne metale.
Za niebieski odcień służy do zabarwienia tkanin i metali. Został użyty do osadzania metalicznej miedzi na włókna celulozowe w celu uzyskania tkanin przewodzących energię elektryczną. Służy również do przygotowywania nanocząstek miedzi i jego tlenków, z różnorodnymi aplikacjami.
W wysokich stężeniach może być toksyczny dla fauny i flory, więc czasami służy do eliminowania szkodników (zwierząt lub roślin) środowisk wodnych, takich jak laguny i naturalne stawy.
[TOC]
Struktura
Związek ten powstaje przez element miedzi w jego stanie utleniania +2 i anion siarczanu. Ten ostatni ma atom siarki z Walencją +6 otoczony czterema atomami tlenu, każdy z Walencją -2. W ten sposób jon siarczanu ma dwa ładunki ujemne.
Ma również 5 cząsteczek wody w swojej strukturze. Na poniższej liczbie widać sposób, w jaki różne atomy w szkle są ułożone.
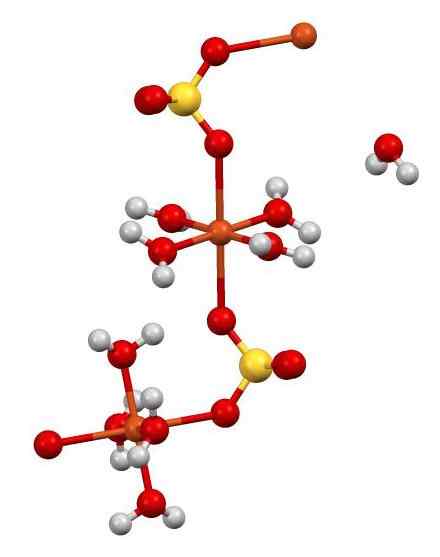 Struktura CUO4 •5h2ALBO. Autor: Smokefoot. Źródło: Wikimedia Commons.
Struktura CUO4 •5h2ALBO. Autor: Smokefoot. Źródło: Wikimedia Commons. Cu2+ (kule pomarańczowe) jest jednocześnie koordynowana z 4 -godzinnymi cząsteczkami2O (tlen = czerwony; wodór = biały) i z 2 atomami tlenu SOS42- (siarka = żółta). Na rysunku jedna z cząsteczek H2O jest w pozornej swobodzie, ale jest częścią krystalicznej struktury.
Nomenklatura
 Minerał z Chalcantita cuso4 •5h2ALBO. Autor: Archaeodontosaurus. Źródło: Wikimedia Commons.
Minerał z Chalcantita cuso4 •5h2ALBO. Autor: Archaeodontosaurus. Źródło: Wikimedia Commons. - Siarczan miedzi pentahydrate
- Cierpienie miedzi (ii) pentahydrat
- Bluejack
- Niebieski kamień (angielski Niebieski kamień)
- Chalcantita, Calcantita, Chalclasa lub Calclasa
Nieruchomości
Stan fizyczny
Niebieski krystaliczny stał.
Waga molekularna
249 686 g/mol
Temperatura topnienia
Po osiągnięciu 110 °.
Gęstość
2286 g/cm3
Rozpuszczalność
Rozpuszczalna woda: 22,0 g/100 g wody w temperaturze 25 ° C. Rozpuszczalny metanol (wybierz3OH). Nieco rozpuszczalne w etanolu (wybierz3Ch2OH).
Właściwości chemiczne
Ten związek po kontakcie z wodą jest rozpuszczany, tworząc jony cu2+ A więc42-. Jego rozpuszczalność w wodzie znacznie się zmniejsza, jeśli kwas siarkowy występuje w wodzie.
Może ci serwować: alkohol z kamforyki: struktura, formuła, właściwości i zastosowaniaH2południowy zachód4 Zapewnia jony42- A jego obecność generuje efekt „wspólnego jonu”, ponieważ jon ten występuje w siarczanie miedzi pentahydratowym. Rozwiązanie można wyrazić w następujący sposób:
Cuso4 •5h2Lub (stałe) + woda ⇔ cu2+ + południowy zachód42- + woda
Dlatego jeśli SO jest już obecne w rozwiązaniu42- kwasu siarkowego, równowaga przesuwa się w lewo, to znaczy w kierunku tworzenia stałego, a zatem rozpuszczalność zmniejsza się.
Uzyskanie
Jednym ze sposobów uzyskania siarczanu miedzi pentahydratu jest rozpuszczenie minerału Malachite w wodnym roztworze kwasu siarkowego (H (H H2południowy zachód4) w kontrolowanej temperaturze. Malquita zawiera Cu2(OH)2WSPÓŁ3 Z innymi zanieczyszczeniami, takimi jak żelazo.
Nieczysty roztwór miedzi (II) traktuje się nadtlenkiem wodoru (H2ALBO2) Aby zapewnić, że zanieczyszczenia żelaza (ii) (wiara2+) stać się żelazem (iii) (wiara3+). Ten ostatni jest wykonany w postaci wodorotlenku żelazowego (wiara (OH)3) Za pomocą wodorotlenku sodu (NaOH).
Osad oznacza, że cząstki nierozpuszczalnego ciała stałego powstają w roztworze, który spada na dno zawierającego go pojemnika.
 Wygląd skoncentrowanego roztworu CUSO4 •5h2ALBO. Autor: Public DomeAnpartures. Źródło: Pixabay.
Wygląd skoncentrowanego roztworu CUSO4 •5h2ALBO. Autor: Public DomeAnpartures. Źródło: Pixabay. Powstała mieszanina jest filtrowana w celu usunięcia stałego wiary (OH)3 A pozostała płyn jest traktowana etanolem (c2H5Och), metanol (wybierz3OH) lub kwas siarkowy w celu wytrącania wszystkich jonów Cu2+ cuo4 •5h2ALBO.
Podczas dodawania na przykład etanolu dostępnych jest mniej wody dla jonów Cu2+ A więc42- są w roztworze i zwykle łączą się. Działa jak odwodnienie. Im bardziej etanol jest dodawany bardziej solidny.
Wytrącone substancje stałe można rekrutować, aby ją oczyścić. Aby to zrobić, rozpuszcza się w wodzie w temperaturze 80-90 ° C, a następnie roztwór chłodzi się w 25-30 ° C. Związek Pentahydrate ponownie pędza, a zanieczyszczenia pozostają w roztworze.
Aplikacje
Ma szeroki okres zastosowań komercyjnych.
W obszarze rolnictwa służy jako pestycyd, środki owadobójcze, herbicyd, grzybobójczy, blemucide i addytyw gleby. W terapiach weterynaryjnych jest stosowany jako przeciwgąciowy, grzybobójczy i emético (powodujący wymioty).
Jest używany jako niebieski lub zielony pigment w barwnikach i barwnikach, jako mordant w kolorze tkanin i metali. Także jako toner wrażeń na zdjęciach i jako odczynnik zintensyfikowania negatywów.
Może ci służyć: skuteczne obciążenie nuklearneJest stosowany w działaniach wydobywczych jako odczynnik flotacyjny w celu odzyskiwania cynku i ołowiu. Służy do produkcji innych związków miedzianych, jest stosowany w opalenizny.
W żywności dla zwierząt
Ten związek jest stosowany w diecie świń w bardzo małych ilościach jako promotor wzrostu, szczególnie w fazie tylnej. Mechanizm, za pomocą którego ma ten efekt, jest nadal nieznany.
Niektórzy badacze twierdzą, że zmniejsza populację patogennych lub szkodliwych bakterii w jelicie zwierząt, a w konsekwencji sprzyja ich wzrostowi.
 Z cuso4 •5h2O możesz faworyzować rozwój świni odsadzonych. Autor: Mabelamber. Źródło: Pixabay.
Z cuso4 •5h2O możesz faworyzować rozwój świni odsadzonych. Autor: Mabelamber. Źródło: Pixabay. Inni uczeni wskazują, że poprawia zdrowie jelit tych zwierząt, ale niektóre badania wskazują, że wstrzyknięcie dożylne miedzi również poprawia jego wzrost.
Był również używany do tego samego celu w drobiu i był używany w niedoborze miedzian przeżuwaczy.
W syntezie nanocząstek
Siarczan miedzi pentahydrate zastosowano do uzyskania mieszanych nanocząstek miedzi i tlenku miedzi (I) (Cu/Cu2ALBO).
Nanocząstki to wyjątkowo małe struktury, które można zobaczyć tylko za pomocą mikroskopu elektronicznego.
Pył Cu/cu2O W postaci nanocząstek, które stosuje w katalizie lub przyspieszeniu reakcji chemicznych, w półprzewodnikach i materiałach przeciwdrobnoustrojowych, między innymi.
W badaniach nad kontrolą szkodników
Cuso4 •5h2Lub został wykorzystany w doświadczeniach do oceny jego toksyczności wobec ślimaków gatunku Pomacea canaliculata.
Są to rodzime mięczaki z tropikalnych regionów Ameryki Południowej, które zamieszkują różne rodzaje ekosystemów, od bagien i lagun po jeziora i rzeki.
Są badane, ponieważ niektóre ludzkie pasożyty gospodarza, takie jak Schistosoma mansoni (Trematode, który powoduje chorobę Bilharzia). Karakole mogą być również szkodliwe dla upraw rolniczych w zalewanych regionach.
 Caparazones de los Caracoles Pomacea canaliculata. H. Zell/CC BY-SA (https: // creativeCommons.Org/licencje/by-sa/3.0). Źródło: Wikimedia Commons.
Caparazones de los Caracoles Pomacea canaliculata. H. Zell/CC BY-SA (https: // creativeCommons.Org/licencje/by-sa/3.0). Źródło: Wikimedia Commons.  Jaja osadzone przez ślimaki w roślinie wodnej. Te ślimaki czasami stanowią plagę, którą można kontrolować za pomocą CUSO4 •5h2ALBO. Shan LV, National Institute of Pasożyc Chorobes/CC Autor (https: // creativeCommons.Org/licencje/według/2.5). Źródło: Wikimedia Commons.
Jaja osadzone przez ślimaki w roślinie wodnej. Te ślimaki czasami stanowią plagę, którą można kontrolować za pomocą CUSO4 •5h2ALBO. Shan LV, National Institute of Pasożyc Chorobes/CC Autor (https: // creativeCommons.Org/licencje/według/2.5). Źródło: Wikimedia Commons. Według przeglądu badań, wodne roztwory siarczanu miedzi pentahydratu są wyjątkowo toksyczne dla tych ślimaków, więc ten związek można wykorzystać do wyeliminowania mięczaka z zarażonych obszarów.
Może ci służyć: reakcje spalaniaWedług niektórych dochodzeń dzieje się tak, ponieważ ślimak nie potrzebuje jonu miedzi, więc tylko kontakt z tym jonem byłby wystarczający, aby śmierć zwierzęcia nastąpiła.
W elektryczności przewodzących tkaniny
Ten związek został wykorzystany do uzyskiwania materiałów tekstylnych ze zintegrowanymi czujnikami energii elektrycznej. Ten rodzaj tkaniny ma zastosowanie w urządzeniach magazynowych elektrycznych, czujnikach ciśnienia, fotodetektora i ekranach emitujących światło.
Aby uzyskać tkaniny przewodzące energię elektryczną, metalowe włókno tkanin celulozy o nazwie „Lyocell” jest pokryte metaliczną miedzią. Powłoka wykonuje się w sposób nieelektrolityczny oparty na roztworze CUSO4 • 5H2O i innych pomocniczych związków chemicznych.
 Włókno Lyocell. Ten rodzaj tkaniny zastosowano w testach powlekania miedzi. Dobrozhinetsky/cc by-SA (https: // creativeCommons.Org/licencje/by-sa/3.0). Źródło: Wikimedia Commons.
Włókno Lyocell. Ten rodzaj tkaniny zastosowano w testach powlekania miedzi. Dobrozhinetsky/cc by-SA (https: // creativeCommons.Org/licencje/by-sa/3.0). Źródło: Wikimedia Commons. Tkanina uzyskana w ten sposób może przenieść sygnał elektryczny nawet w warunkach odkształcenia lub rozciągania, utrzymując wysoką przewodność.
Wpływ na środowisko
Jak wyjaśniono powyżej cuso4 •5h2Lub podczas rozpuszczania się w wodzie generuje jon miedzi (II).
Chociaż miedź jest niezbędna w niskich stężeniach dla aktywności komórkowej żywych organizmów, w wysokich stężeniach może być toksyczna, a nawet powodować śmierć.
Dlatego obecność tego jonu w środowisku stanowi ryzyko zwierząt i roślin. W ekosystemach wodnych może być bioakumulacja w żywych istotach i łańcuchu pokarmowym, powodując uszkodzenia.
 Cuso4 •5h2O może być szkodliwe dla środowisk wodnych. Autor: Jamesdemers. Źródło: Pixabay.
Cuso4 •5h2O może być szkodliwe dla środowisk wodnych. Autor: Jamesdemers. Źródło: Pixabay. W rzeczywistości w niektórych doświadczeniach stwierdzono, że zanieczyszczenie środowisk wodnych z siarczanem miedzi pentahydratowym powoduje, że biomasa niektórych roślin wodnych maleje.
Co oznacza, że rośliny rosną mniej w obecności tej soli w wysokich stężeniach.
Bibliografia
- Ołów, d.R. (redaktor) (2003). Podręcznik chemii i fizyki CRC. 85th CRC Press.
- Kokes, h. i in. (2014). Rozpuszczanie miedzi i żelaza z rudy malachitowej i precyzja pentahydratu siarczanu miedzi według procesu chemicznego. Inżynieria naukowa i technologia, międzynarodowy czasopismo. 2014; 17 (1): 39-44. Odzyskane z naukowym.com.
- Azevedo B Alves., J.P. i Peixoto, m.N. (2015). Zmniejszenie biomasy Irytująca Salvinia Narażony na pentahydrat siarczanu miedzi (cuo4.5h2ALBO). Obrót silnika. Otoczenia. Woda 2015; 10 (3): 520-529. Wyzdrowiał z DOAJ.org.
- Root, w. i in. (2019). Elastyczny czujnik odkształceń tekstylnych oparty na tkaninie celulozowej powleczonej miedzi. Polymers 2019, 11, 784. MDPI odzyskało.com.
- Pittelli, r.DO. i in. (2008). Ostra toksyczność siarczanu miedzi i wodny ekstrakt z wysuszonych liści neem na ślimakach (Pomacea canaliculata). Ustawa Sci. Biol. Sci. 2008; 30 (2): 179-184. Wyzdrowiał z DOAJ.org.
- Badawy, s.M. i in. (2015). Synteza, charakterystyka i aktywność katalityczna nanocząstek Cu/Cu2O przygotowane w środowisku wodnym. Biuletyn inżynierii i katalizy reakcji chemicznej. 2015; 10 (2): 169-174. Wyzdrowiał z DOAJ.org.
- Justel, f.J. i in. (2014). Rozpuszczalność i właściwości fizyczne nasyconych roztworów w siarczanie miedzi + kwas siarkowy + układ wodny morski w różnych temperaturach. Brazylijski Journal of Chemical Engineering. 2015; 32 (3): 629-635. Wyzdrowiał z DOAJ.org.
- Park, c.S. i Kim, B.G. (2016). In vitro Rozpuszczalność siarczanu miedzi (II) i trihydroksydę chlorku dikopper. Azjatyccy Austalas. J. Anim. Sci. 2016; 29 (11): 1608-1615. Wyzdrowiał z DOAJ.org.
- LUB.S. National Library of Medicine. (2019). Pentahydrat siarczanu miedzi. Odzyskane z Pubchem.NCBI.NLM.Nih.Gov.
- Wikipedia (2020). Chalcanthite. Odzyskane z.Wikipedia.org.
- « Charakterystyka biomów morskich, typy, flora, fauna
- Struktura wosków (biologiczna), właściwości, funkcja, typy »

