Synteza typów lipidów i ich głównych mechanizmów
- 3820
- 6
- Marianna Czarnecki
Synteza lipidów Składa się z szeregu reakcji enzymatycznych, za pomocą których węglowodory krótkoterminowe są skondensowane w celu utworzenia cząsteczek dłuższych łańcucha, które mogą następnie utrzymać różne modyfikacje chemiczne.
Lipidy są bardzo zróżnicowanym rodzajem biomolekuli syntetyzowanych przez wszystkie żywe komórki i są specjalizowane w wielu podstawowych funkcjach do utrzymania życia komórkowego.
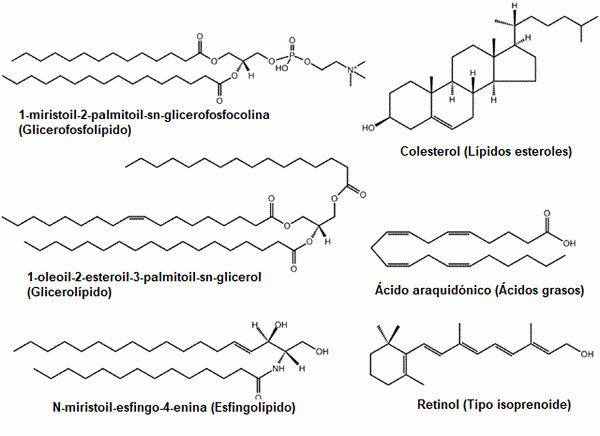 Niektóre przykłady typowych lipidów: glicerofosfolipidy, sterole, glicerolipidy, kwasy tłuszczowe, sfingolipidy i prenole (źródło: oryginalnym przesyłaniem było LMAPS na angielskiej Wikipedii. / GFDL 1.2 (http: // www.gnu antylopa.Org/licencje/stare licencje/FDL-1.2.html) przez Commons, zaadaptowane przez Raquel Parada)
Niektóre przykłady typowych lipidów: glicerofosfolipidy, sterole, glicerolipidy, kwasy tłuszczowe, sfingolipidy i prenole (źródło: oryginalnym przesyłaniem było LMAPS na angielskiej Wikipedii. / GFDL 1.2 (http: // www.gnu antylopa.Org/licencje/stare licencje/FDL-1.2.html) przez Commons, zaadaptowane przez Raquel Parada) Lipidy są głównymi składnikami błon biologicznych, co czyni je fundamentalnymi cząsteczkami dla istnienia komórek jako izolowanych bytów ich otoczenia.
Niektóre lipidy mają również wyspecjalizowane funkcje, takie jak pigmenty, kofakory, transportery, detergenty, hormony, posłańcy wewnątrzokomórkowe, kowalencyjne kotwice białek błonowych itp. Dlatego zdolność do syntezy różnych rodzajów lipidów ma kluczowe znaczenie dla przetrwania wszystkich żywych organizmów.
Ta duża grupa związków jest tradycyjnie podzielona na kilka kategorii lub podgrup: kwasy tłuszczowe (nasycone i nienasycone), lipidy złożone glicerydów (lipoproteiny).
[TOC]
Rodzaje lipidów i ich główne mechanizmy syntezy
Wszystkie sekwencje reakcji tras biosyntezy lipidów są endogoniczne i redukcyjne. Innymi słowy, wszyscy używają ATP jako źródła energii i zredukowanego transportera elektronów, takiego jak NADPH, jako moc zmniejszająca.
Następnie zostaną opisane główne reakcje tras biosyntetycznych głównych rodzajów lipidów, tj. Kwasów tłuszczowych i eikosanoidowych, triacylogliceroli oraz fosfolipidów i sterolu (cholesterol) (cholesterol).
- Synteza kwasów tłuszczowych
Kwasy tłuszczowe są niezwykle ważnymi cząsteczkami z punktu widzenia lipidowego, ponieważ są częścią najbardziej odpowiednich lipidów w komórkach. Jego synteza, wbrew temu, co wielu naukowców myślało podczas pierwszych badań, nie składa się z odwrotnej drogi ich β-utleniania.
W rzeczywistości ta trasa metaboliczna występuje w różnych przedziałach komórkowych i wymaga uczestnictwa pośrednika trzech atomów węgla znanego jako malonylo-CoA, co nie jest konieczne w utlenianiu.
 Malonylo-CoA. Neuropeker / pub domena
Malonylo-CoA. Neuropeker / pub domena Ponadto jest ściśle związany z grupami sulfodonowymi białkami znanymi jako transportery grupy acylowej (ACP, angielski Białka nośnika acylowego).
Zasadniczo synteza kwasów tłuszczowych, zwłaszcza długiego łańcucha, jest sekwencyjnym procesem, w którym powtarzane są cztery kroki w każdym „powrotu”, a podczas każdego powrotu istnieje grupa kwasu nasycona, która jest podłoże implikuje kolejną kondensację nową cząsteczką malonylo-CoA.
W każdej turze lub cyklu reakcji łańcuch kwasów tłuszczowych rozciąga się na dwa węgle, aż do osiągnięcia 16 atomów (palmitynian.
Formacja malonylo-CoA
Ten pośrednik trzech atomów węgla jest nieodwracalnie utworzony z acetylo-CoA dzięki działaniu enzymu karboksylazy acetylo-CoA, który ma grupę prostaty biotyny, która jest kowalencyjnie powiązana z enzymem i który uczestniczy w tej katalizie w tej katalizie w tym katalizie.
W tej reakcji grupa karboksylowa pochodząca z cząsteczki wodorowęglanowej (HCO3-) jest przenoszona do biotyny w postaci zależnej od ATP, w której grupa biotynylowa wypełnia funkcję „tymczasowego przenośnika” cząsteczki, podczas gdy transfery do acetylo-CoA, Produkcja malonylo-CoA.
Może ci służyć: Test oksydazy: podkład, procedura i zastosowaniaW sekwencji syntezy kwasów tłuszczowych zastosowanym środkiem redukującym jest NADPH, a grupy aktywujące to dwie grupy tiol (-SH), które są częścią kompleksu wielowo-emerycznego zwanego kwasem tłuszczowym syntazy, który jest najważniejszy w katalizie syntetycznej.
U kręgowców kompleks kwasu tłuszczowego syntazy jest częścią pojedynczego dużego łańcucha polipeptydowego, w którym reprezentowano 7 aktywności enzymatyczne charakterystyczne dla drogi syntezy, a także aktywność hydrolityczną niezbędną do uwolnienia pośredników na końcu syntezy.
 Struktura enzymu kwasu tłuszczowego Syntasa (źródło: Boehringer Ingelheim/CC BY-SA (https: // creativeCommons.Org/licencje/nabrzeże/4.0) Via Wikimedia Commons)
Struktura enzymu kwasu tłuszczowego Syntasa (źródło: Boehringer Ingelheim/CC BY-SA (https: // creativeCommons.Org/licencje/nabrzeże/4.0) Via Wikimedia Commons) 7 aktywności enzymatycznej tego kompleksu to: białko transportowe grupy acilo (ACP), transacetilas acetylo-CoA-ACP Cetoacil-ACP Reduktaza (KR), β-hydroksyacil-ACP dehydratasa (HD) i reduktaza Anger-ACP (ER).
Zanim nastąpi reakcje kondensacji w celu złożenia łańcucha kwasu tłuszczowego, dwie grupy tiol w kompleksie enzymatycznym są „ładowane” grupami acylowymi: przede wszystkim acetylo -CoA jest przenoszone do grupy -SH cystein W syntazie β-cetoacylo-ACP kompleksu reakcja katalizowana przez enzym transaketyloa (AT) (AT) (AT) (AT) (AT) (AT) (AT) (AT) (AT) (AT).
Następnie grupa maloniczna jest przenoszona z cząsteczki malonylo -CoA do grupy -SH przenośnika grupy ACILO (ACP) jest częścią syntazy kompleksu kwasów tłuszczowych.
Sekwencja czterech reakcji dla każdego „powrotu” cyklu reakcji jest następująca:
- Kondensacja: grupy acetylowe i malonylowe „załadowane” w enzymie są skondensowane w celu utworzenia cząsteczki acetoacetylo -ACP, która jest połączona z częścią ACP przez grupę -SH -SSH. W tym etapie znajduje się cząsteczka CO2 i jest katalizowana przez syntazę β-Zoacyl-ACP (grupa acetylowa zajmuje pozycję „końcowego metylu” kompleksu acetoacetylo-ACP).
- Zmniejszenie grupy karbonylowej: grupa karbonylowa w pozycji C3 acetoacetylo-ACP jest zmniejszona do wytworzenia d-β-hydroksybutiril-acp, reakcja katalizowana przez reduktazę β-cetoacylo-acp, której NADPH używa jako dawcy elektronów.
- Odwodnienie: węgle C2 i C3 d-β-hydroksybutiril-acp są pozbawione cząsteczek wody, tworząc podwójne wiązanie, które kończy się na wytwarzaniu nowego związku trans-∆2-butenoil-acp. W tym procesie pośredniczy enzym dehydrataza β-hydroksyacylu-ACP (HD) (HD).
- Zmniejszenie podwójnego wiązania: podwójne wiązanie związku utworzonego w etapie odwodnienia jest nasycone (zmniejszone), aby zwiększyć się butiril-acp przez reakcję katalizowaną przez reduktazę enzymu-ACP (ER), która również wykorzystuje NADPH jako środka redukującego.
Reakcje syntezy występują do momentu powstania cząsteczki palmitynianowej (16 atomów węgla), która jest hydrolizowana z kompleksu enzymatycznego i uwalniana jako możliwy prekursor kwasów tłuszczowych łańcuchów o większej długości, które są wytwarzane przez układy wydłużania kwasów tłuszczowych położonych w gładko część retikulum endoplazmatycznego i w mitochondriach.
Może ci służyć: fauna i flora morza peruwiańskiegoInne modyfikacje, które mogą cierpieć te cząsteczki, takie jak na przykład deatowanie, są katalizowane przez różne enzymy, które na ogół występują w gładkim retikulum endoplazmatycznym.
- Synteza eikozanoidów
Eikozanoidy to lipidy komórkowe, które mają funkcje, takie jak cząsteczki komunikatora „krótkie”, wytwarzane za pomocą niektórych tkanin do komunikacji z sąsiednimi tkaninami. Cząsteczki te są syntetyzowane z wielonienasyconych kwasów tłuszczowych 20 atomów węgla.
Prostaglandyny
W odpowiedzi na bodziec hormonalny enzym fosfolipazy atakuje fosfolipidy błonowe i uwalnia araquidonato z węgla glicerolu 2. Związek ten jest przekształcany w prostaglandyny dzięki enzymie gładkiego retikulum endoplazmatycznego o aktywności dwufunkcyjnej: cyklooksygenaza (COX) lub syntaza prostaglandyn H2.
Thromboxan
Prostaglandyny można przekształcić w trzurboksyany dzięki syntazie trromboxan w płytkach krwi (trombocyty). Te cząsteczki uczestniczą w początkowych etapach krzepnięcia krwi.
- Synteza triacylogliceroli
Kwasy tłuszczowe są fundamentalnymi cząsteczkami dla syntezy innych bardziej złożonych związków w komórkach, takich jak triacyloglicerole lub lipidowe lipidy glicerofosfolipidowe (procesy zależne od komórkowych potrzeb metabolicznych).
Zwierzęta wytwarzają triacyloglicereno i glyceofosfalipidy z dwóch popularnych prekursorów: acyl tłuszczowych L i 3-fosforan L-glicerol. Acyl fat-CoA jest wytwarzany przez syntezę acylo-CoA, które uczestniczą w β-utlenianiu, podczas gdy 3-fosforan L-glicerol jest uzyskiwana z glikolizy i działaniem dwóch alternatywnych enzymów: dehydrogenazy glicerolu 3-fosforan.
Triacyloglicerole powstają przez reakcję między dwiema cząsteczkami ACIL Flo-CoA i 3-fosforanową cząsteczką dicyloglicerolu; Te reakcje transferu są katalizowane przez określone transferazy.
W tej reakcji pojawia się początkowo kwas fosfatydowy, który jest defosforylowany przez fosfatazę kwasu fosfatydowego enzymu w celu wytworzenia 1,2-dicyloglicerolu, która jest ponownie zdolna do zaakceptowania trzeciej cząsteczki acylu tłuszczowego, wytwarzającego trialiwizę.
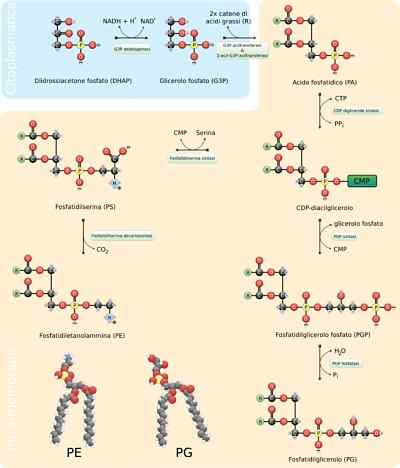
- Synteza fosfolipidów
Fosfolipidy są niezwykle zmiennymi cząsteczkami, ponieważ wiele różnych może tworzyć się przez kombinację kwasów tłuszczowych i grup „głowy” ze szkieletem glicerolu (gliceofosfolipidy) lub sfinozyny (sfingolipidy), które je charakteryzują.
Ogólne zgromadzenie tych cząsteczek wymaga syntezy szkieletu glicerolu lub sferycznego zjednoczenia z odpowiednimi kwasami tłuszczowymi, przez steryfikację lub amidację, dodanie hydrofilowej grupy „głowy” przez wiązanie fosfodiéster i, w razie potrzeby , zmiana lub wymiana tych ostatnich grup.
U eukariotów proces ten występuje w gładkim retikulum endoplazmatycznym, a także w wewnętrznej błonie mitochondrialnej, gdzie mogą pozostać na czas nieokreślony lub skąd można je przenieść do innych miejsc.
Kroki reakcji
Pierwsze etapy reakcji syntezy glicerofosfolipidów są równoważne z wytwarzaniem triacylogliceroli, ponieważ 3-fosforanowa cząsteczka glicerolu jest esteryfikowana do dwóch cząsteczek kwasu tłuszczowego w węgłach 1 i 2, tworząc fosfatyczne kwas fosfatydowy. Często można znaleźć fosfolipidy, które mają nasycone kwasy tłuszczowe w C1 i nienasycone w C2 glicerolu.
Może ci służyć: ResistinaKwas fosfatydowy może być również wytwarzany przez fosforylację cząsteczki diacyloglicerolu już zsyntetyzowanej lub „recyklingu”.
„Głowa” grupy polarne tych cząsteczek powstają przez połączenia fosfodiéster. Pierwszą rzeczą, która powinna się zdarzyć, aby ten proces był poprawnie „aktywacja” jednej z grup hydroksylowych, która uczestniczy w procesie za pomocą hydroksylu, która uczestniczy w reakcji.
Jeśli ta cząsteczka wiąże się z diacyloglicerolem, wówczas powstaje CDP-dicyloglicerol („aktywowany” kształt kwasu fosfatydowego), ale może się to również zdarzyć w grupie hydroksylowej grupy „głowicy” grupy „głowicy”.
Na przykład w przypadku fosfatydyloseryny diaklicerol jest aktywowany przez kondensację cząsteczki kwasu fosfatydowego z cząsteczką cytydyny trif-cytydyny (CTP), tworząc CDP-dicyloglicerol i eliminuje pirofosforanowe.
Jeżeli cząsteczka MMP (monofosforan cytydyny) przesuwa się przez nukleofilowy atak seryny lub hydroksylu hydroksylu w węgle 1 3-fosforan glicerolu. Fosforan wytwarzał fosfatydyloglicerolu.
Obie cząsteczki wytwarzane w ten sposób służą jako prekursory innych lipidów błonowych, które często dzielą od siebie trasy biosyntetyczne.
- Synteza cholesterolu
Cholesterol jest niezbędną cząsteczką dla zwierząt, które mogą być syntetyzowane przez jej komórki, więc nie jest niezbędna w codziennej diecie. Ta cząsteczka 27 atomów węgla jest wytwarzana z prekursora: octan.
Ta złożona cząsteczka powstaje z acetylo-CoA w czterech głównych stadiach:
- Kondensacja trzech jednostek octanu w celu utworzenia mevalonato, cząsteczki pośredniej 6 węgli (najpierw cząsteczka acetoacetylo-CoA powstaje z dwóch acetylo-CoA (enzym tiolazy), a następnie kolejną β-hydroksy-β-metyloglutarililililililil-CoA (HMG-enzym COA) (enzym synteta HMG-CoA). Mevalonato powstaje z HMG-CoA i dzięki enzymie reduktazy HMG-CoA.
- Konwersja mevalonato na jednostki izoprenowe. Pierwsze 3 grupy fosforanowe są przenoszone z 3 cząsteczek ATP do Mevalonato. Jeden z fosforanów jest tracony razem z sąsiednią grupą karbonylową i jest uformowany
- Polimeryzacja lub kondensacja 6 jednostek izoprenowych 5 atomów węgla z utworzeniem atomów 30 -węglowych (cząsteczka liniowa) ogolony (cząsteczka liniowa).
- Cykracja escualean w celu utworzenia 4 pierścieni rdzenia sterydowego cholesterolu i późniejszych zmian chemicznych: utleniania, migracja i eliminacja grup metylowych itp., Co daje cholesterol.
Bibliografia
- Garrett, r. H., I Grisham, C. M. (2001). Zasady biochemii: z ludzkim skupieniem. Brooks/Cole Publishing Company.
- Murray, r. K., Granner, zm. K., Mayes, str. DO., & Rodwell, V. W. (2014). Ilustrowana biochemia Harpera. McGraw-Hill.
- Nelson, zm. L., Lehninger, a. L., & Cox, m. M. (2008). Zasady biochemii lehninger. Macmillan.
- Jacquemyn, j., Cascaho, a., & Goodchild, r. I. (2017). Tajniki biosyntezy lipidowej endoplazmatycznej retikulum. Embo Reports, 18 (11), 1905-1921.
- Ohlrogge, j., I przeglądaj, j. (1995). Biosynteza lipidów. Komórka roślinna, 7 (7), 957.
- « José López Portillo Biografia, rząd i wkłady
- Tropikalna dżungla w Meksyku, lokalizacja, ulga, flora, fauna »

