Charakterystyka samario, struktura, uzyskiwanie, użycie

- 1506
- 218
- Eugenia Czapla
On samar Jest to element chemiczny należący do ziem rzadkich, w szczególności do Lanthanids, a którego symbolem jest SM. Jego imię pochodzi od Minerału Samarskita, na cześć pułkownika Vassili Samarsky'ego, który był rosyjskim oficerem górniczym i który przekazał próbki tego minerału na jego studia. Francuski chemik, Paul émile Lecoq, uzyskał tlenek i niektóre z jego soli z Samkary w 1879 roku, pracując w Paryżu.
Lecoq z Boisbaudran ma zwykle zasługę na odkrycie Samarium, chociaż istniały inne chemikalia i mineralogiczne, które wcześniej narysowały sposób na znalezienie. Dopiero w 1901 r.
 Samario Samario przechowywane szczelnie w blistrze. Źródło: Obrazy Hi-Res Elementów Chemicznych/CC (https: // CreativeCommons.Org/licencje/według/3.0)
Samario Samario przechowywane szczelnie w blistrze. Źródło: Obrazy Hi-Res Elementów Chemicznych/CC (https: // CreativeCommons.Org/licencje/według/3.0) Przyczyną tego opóźnienia w jego izolacji był fakt, że Samario jest względnie reaktywnym metalem, więc nie ma czystych natury, ale stanowi część wielu mas mineralnych. Podobnie utrzymuje bliski związek geologiczny z innymi elementami ziem rzadkich, takich jak Europium i Neodym, więc trudno jest oddzielić go od takich zanieczyszczeń.
Samario to metal o bardzo zróżnicowanych zastosowaniach, stosowany do raka, randki, reaktorów jądrowych, magnesów organicznych i katalizy.
[TOC]
Charakterystyka Samario
Fizyczny
Samario ma srebrny biały połysk, ale to szybko staje się złotem2ALBO3, który nazywa się Samaria. Jest to jeden z najtrudniejszych i najbardziej niestabilnych metali Lantanide, mające odpowiednio 1072 i 1900 ° C.
Utlenia się ze względną powolnością po wystawieniu na powietrze lub zanurzony w oleju mineralnym. Dlatego musi być przechowywany w pęcherzy lub w pojemnikach uszczelnionych argonem lub innym gazem obojętnym. Po podgrzaniu w temperaturze 150 °.
Może ci służyć: lutetecio: struktura, właściwości, użycia, uzyskiwanieChemikalia
Samario, podobnie jak inne Lantanids, wykazuje stan utleniania +3 w prawie wszystkich swoich związkach; Oznacza to, że znajduje się jako kation SM3+. Jest jednak również w stanie przyjąć status utleniania +2, SM2+, przebywanie w związkach takich jak SMO (tlenek samarium), SMS (monosulfid Samarium) i SMI2 (Samario Diyoduro).
Rozpuszcza się w gorącej wodzie, a zwłaszcza w rozcieńczonych kwasach, takich jak HCL, H2południowy zachód4 i rozdz3Cooh; Z wyjątkiem HF, ponieważ tworzy warstwę ochronną SMF3 Spowolnienie jego rozwiązania. Twój tlenek, SM2ALBO3, Jest umiarkowanie podstawowy, więc podczas rozpuszczania się w wodzie uwolni godne uwagi ilości jonów OH- Przez działanie wodorotlenku SM (OH)3.
Większość związków Samarium +3 charakteryzuje się żółt-zielonymi kolorami, a niektóre nawet wyróżniają.
Struktura chemiczna
W temperaturze pokojowej Samarium przyjmuje romboedralną strukturę krystaliczną, która odpowiada fazie polimorfu lub α. Po podgrzaniu w 731 °.
Kontynuując ogrzewanie w temperaturze 922 °.
Kryształy Samario mogą również ponieść inne przejścia, gdy są skompresowane pod wysokim ciśnieniem, w kolejności tysięcy kilobarów, będąc tetragonalnym i podwójnie zwartym sześciokątnym (DHCP) niektórymi strukturami uzyskanymi w tych badaniach.
Elektroniczna Konfiguracja
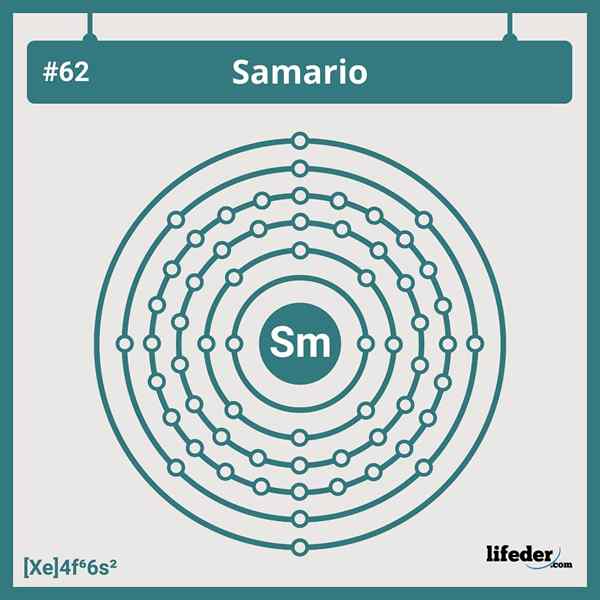 Konfiguracja elektroniczna Samario
Konfiguracja elektroniczna Samario Skrócona konfiguracja elektroniczna Samario to:
Może ci służyć: fosforan dihydroksyacetonu (DHAP): Charakterystyka i zastosowania[Xe] 6s24f6
Ma sześć elektronów w swoich orbitalach 4F, co zgadza się ze swoją pozycją w szóstej grupie Lantanowców. Dlatego jego konfiguracja elektroniczna nie dotyczy żadnego z wielu odchyleń, które widzimy w tabeli okresowej.
Uzyskanie
 Monazytowy piasek mineralny, główny surowiec do uzyskania samarium. Źródło: D. Kemp, a. C. Cilliersssssowo modyfikowane przez Gretarssona (zastąpiony czerwony, słabo widoczny pasek SCA przez biały)/cc by-SA (https: // creativeCommons.Org/licencje/nabrzeże/4.0)
Monazytowy piasek mineralny, główny surowiec do uzyskania samarium. Źródło: D. Kemp, a. C. Cilliersssssowo modyfikowane przez Gretarssona (zastąpiony czerwony, słabo widoczny pasek SCA przez biały)/cc by-SA (https: // creativeCommons.Org/licencje/nabrzeże/4.0) Mimo że jest częścią ziem rzadkich, obfitość Samario jest lepsza od obfitości cyny i innych metali. Jest to związane z rdzą metali ziem rzadkich, komponując te minerały, takie jak Cerita, La Gadolinita, La Monazita i La Bastnasita, monazit jest jednym z głównych źródeł mineralogicznych, ponieważ zawiera około 2.8% Samarium.
Istnieje kilka metod jego uzyskania. Jeden z nich polega na przetwarzaniu piasków monazytu i oddzieleniu jonów SM3+, albo przez rozwiązania i kolejne ekstrakcje rozpuszczalników, albo przy użyciu chromatografii wymiany jonowej.
Jony Samario są uzyskiwane jako SMCL3, Są poddawane elektrolizy z stopioną mieszaniną NaCl lub CACL2. Z drugiej strony, jeśli jony te zostaną uzyskane jako SM2ALBO3, Następnie tlenek jest zmniejszany w topnieniu tantalium za pomocą Lantano, gdzie opary samarium są destylowane ze względu na ich dolną temperaturę wrzenia. Równanie tej redukcji jest następujące:
CZŁEK2ALBO3 + 2LA → 2SM +2ALBO3
Redukcja jest przeprowadzana na gorąco (blisko 1400 ° C) i w obrębie piekarnika indukcyjnego próżniowego, co dodatkowo przyspiesza destylację oparów wynikających z samarium.
Używa/aplikacje Samario
Magnes
 Magnesy SMCO są używane jako część funkcjonalnych komponentów zegarków kwarcowych. Źródło: © 2010 autorstwa Tomasz Siemiecki [Użytkownik: TSCA, Mail: Tomasz.Siemiecki w Gmailu.com]/cc przez (https: // creativeCommons.Org/licencje/według/3.0)
Magnesy SMCO są używane jako część funkcjonalnych komponentów zegarków kwarcowych. Źródło: © 2010 autorstwa Tomasz Siemiecki [Użytkownik: TSCA, Mail: Tomasz.Siemiecki w Gmailu.com]/cc przez (https: // creativeCommons.Org/licencje/według/3.0) Samario jest stopowany kobaltem, aby wywołać stopy SMCO, których magnetyzacja jest trwała i około 10000 razy wyższa niż w przypadku żelaza.
Może Ci służyć: Operacje jednostkoweTe magnesy Samario-Colto są używane głównie w okiennikach kamer, słuchawek, silników, pigułek na gitarze elektrycznej, a także w zastosowaniach wojskowych, w których obsługują temperatury większe niż 400 ° C.
Medycyna
 Struktura molekularna Quadramet, 153Sm-EDTMP.
Struktura molekularna Quadramet, 153Sm-EDTMP. Sam Samario jest stosunkowo toksyczny. Jednak jeden z jego radioaktywnych izotopów, 153SM, narzekany cząsteczką EDTMP (etylediaminotetrametylen -fosfonian, obraz powyżej), służy do zwalczania bólu w leczeniu nowotworów prostaty, płuc i piersi. Ten lek nazywa się Leksidronam Samario (153SM), znany komercyjnie jako kwadramet.
Reaktor nuklearny
Izotop 149SM jest doskonałym chłonnością neutronów, więc jest stosowany w reaktorach jądrowych do kontrolowania reakcji i zapobiegania eksplozji.
elektronika
SMS -em stanowi różnicę temperatur w elektryczności, więc jest używany jako termoelektryczny w różnych urządzeniach. Ma również osobliwość stawania się metalicznym przy stosunkowo niskich ciśnieniach.
Randki
Rozpad alfa izotopu 147Ye (T1/2= 1.06 × 10jedenaście) do izotopu 143ND, jest używany do datowania próbek skał lub meteorytów wewnątrz lub na zewnątrz Ziemi. Ma tę zaletę, że atomy 147SM i 143Mają te same cechy geologiczne, to znaczy nie cierpią z powodu dużych separacji podczas procesów metamorficznych.
Kataliza
Samario jest stosowane w syntezie organicznej, takiej jak SMI2, działając jako środek redukujący w licznej syntezy syntetycznych wersji produktów naturalnych. Z drugiej strony SM2ALBO3 Jest to katalizatorem odwodnienia i odwodornienia etanolu.
Bibliografia
- Shiver & Atkins. (2008). Chemia nieorganiczna. (czwarta edycja). MC Graw Hill.
- Wikipedia. (2020). Samar. Źródło: w:.Wikipedia.org
- Oleg d. Neikov i Stanislav s. (2019). Podręcznik nieżelaznych proszków metalowych: technologie i zastosowania. (Druga edycja). Scientedirect.
- Redaktorzy Enyclopaedia Britannica. (2020). Samar. Odzyskane z: Britannica.com
- National Center for Biotechnology Information. (2020). Samar. Element Pubchem. Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov
- Dr. Doug Stewart. (2020). Fakty elementów samarium. Odzyskane z: Chemicool.com
- Strekopytov, s. (2016). Salutuj do Samarium. Nature Chem 8, 816. doi.Org/10.1038/NHEM.2565

