Charakterystyka rybozy, struktura i funkcje
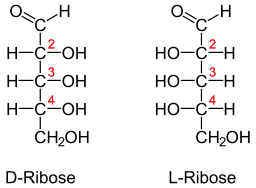
- 3934
- 374
- Maksymilian Kępa
Ribosa Jest to pięciokrębowy cukier, który jest obecny w rybonukleozydach, rybonukleotydach i jego pochodnych. Inne nazwy można znaleźć, takie jak β-d-lebrounosa, d-liboza i l-liboza.
Nukleotydy są składowymi „blokami” szkieletu kwasu rybonukleinowego (RNA). Każdy nukleotyd składa się z podstawy, która może być adenina, guanina, cytozyna lub uracyl, grupa fosforanowa i cukier, ryboza.
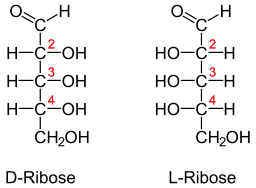 Projekcja Fishera dla D- i L-Libose (źródło: Neuropokeker [domena publiczna] za pośrednictwem Wikimedia Commons)
Projekcja Fishera dla D- i L-Libose (źródło: Neuropokeker [domena publiczna] za pośrednictwem Wikimedia Commons) Ten rodzaj cukru jest szczególnie obfity w tkankach mięśniowych, gdzie jest związany z rybonukleotydami, szczególnie z adenozyną lub Tryfosforanem ATP, który jest niezbędny do funkcjonowania mięśni.
D-rriboza została odkryta w 1891 r. Przez Emil Fischera, a od tego czasu zwrócono dużą uwagę na jego charakterystykę fizykochemiczną i rolę w metabolizmie komórek, to znaczy jako część szkieletu kwasu rybonukleinowego, ATP i kilku z kilku koenzymów.
Na początku uzyskano to tylko z hydrolizy RNA drożdży, aż w latach 50. XX wieku udało się zsyntetyzować z d-glukozy w mniej lub bardziej dostępnych ilościach, umożliwiając uprzemysłowienie jej produkcji.
[TOC]
Charakterystyka
Riboza jest powszechnie ekstrahowaną aldopentozą jako czystym związkiem chemicznym w postaci d-libozy. Jest to rozpuszczalna w wodzie substancja organiczna, biała i krystaliczna. Będąc węglowodanem, ryboza ma charakterystykę polarną i hydrofilową.
Riboza jest zgodna z powszechną zasadą węglowodanów: ma taką samą liczbę atomów węgla i tlenu i dwukrotnie więcej w atomach wodoru.
Poprzez atomy węgla w pozycjach 3 lub 5, cukier ten może dołączyć do grupy fosforanowej, a jeśli dołączy do jednej z azotowych zasad RNA, powstaje nukleotyd.
Najczęstszym sposobem znalezienia rybozy w naturze jest d-liboza i 2-deexy-d-liboza, są to składniki nukleotydów i kwasów nukleinowych. D-liboza jest częścią kwasu rybonukleinowego (RNA) i 2-disakssi-D-dibozy kwasu deoksyrybonukleinowego (DNA).
Może ci służyć: białko K: Charakterystyka, aktywność enzymatyczna, zastosowania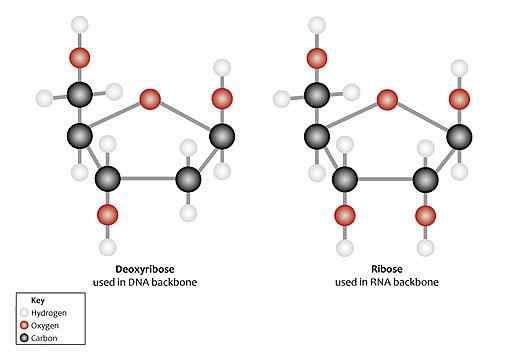 Różnice strukturalne między rybozą i deoksyrybozą (źródło: program edukacji genomiki [CC przez 2.0 (https: // creativeCommons.Org/licencje/według/2.0)] przez Wikimedia Commons)
Różnice strukturalne między rybozą i deoksyrybozą (źródło: program edukacji genomiki [CC przez 2.0 (https: // creativeCommons.Org/licencje/według/2.0)] przez Wikimedia Commons) W nukleotydach oba rodzaje pentozy znajdują się w postaci β-flubokiej (zamknięty pierścień pięciokątny).
W roztworze wolna ryboza jest w równowadze między aldehydem (łańcuch otwarty) a cyklicznym kształtem β. Jednak RNA zawiera tylko formę cykliczną β-D-Dribofuranosa. Biologicznie aktywną postacią jest zwykle d-liboza.
Struktura
La Ribosa to cukier pochodzący z glukozy, który należy do grupy Aldopentosa. Jego wzór cząsteczkowy to C5H10O5 i ma masę cząsteczkową 150.13 g/mol. Ponieważ jest to cukier monosacharydowy, jego hydroliza oddziela cząsteczkę w swoich grupach funkcjonalnych.
Ma, jak wskazuje jego wzór, pięć atomów węgla, które można znaleźć cyklicznie jako część pięciu lub sześciu członków pierścieni. Ten cukier ma grupę aldehydową w atomie węgla 1 i grupie hydroksylowej (-OH) w atomach węgla od pozycji 2 do pozycji 5 pierścienia Pontosa.
Cząsteczka rybozy może być reprezentowana w projekcji Fishera na dwa sposoby: d-liboza lub l-liboza, będąc formą L stereoizomer i enancjomer formy D i odwrotnie.
Klasyfikacja postaci D lub L zależy od orientacji grup hydroksylowych pierwszego atomu węgla po grupie aldehydu. Jeśli ta grupa jest zorientowana na prawą stronę, cząsteczka w imieniu Fishera odpowiada D-Riby.
Projekcja hawortkowa rybozy może być reprezentowana w dwóch dodatkowych strukturach w zależności od orientacji grupy hydroksylowej w atomie węgla, który jest anomerowy. W pozycji β hydroksyl jest zorientowany w kierunku górnej części cząsteczki, podczas gdy pozycja α prowadzi hydroksyl w kierunku dna.
Może ci służyć: flora i fauna Santa Fe: reprezentatywne gatunki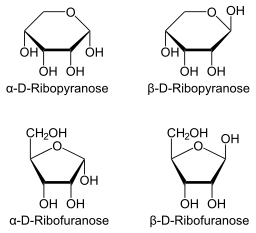 Projekcja Haworth dla Ribopyranosa i Ribofuranosa (źródło: Neurotokeker [domena publiczna] przez Wikimedia Commons)
Projekcja Haworth dla Ribopyranosa i Ribofuranosa (źródło: Neurotokeker [domena publiczna] przez Wikimedia Commons) Zatem, zgodnie z projekcją Hawortha, można przyjmować cztery możliwe sposoby: β-d-liboza, α-d-liboza, β-l-liboza lub α-l-liboza.
Gdy grupy fosforanowe są połączone z rybozą, zwykle nazywane są α, β i ƴ. Hydroliza Tryfosforanu nukleozydów zapewnia energię chemiczną do zwiększenia szerokiej gamy reakcji komórkowych.
Funkcje
Zaproponowano, że produkt fosforanu rybozy rozkładu rybonukleotydów jest jednym z głównych prekursorów furano i tiofenoli, które są odpowiedzialne za charakterystyczny zapach mięsa.
W komórkach
Plastyczność chemiczna rybozy powoduje, że cząsteczka jest zaangażowana w ogromną większość procesów biochemicznych wewnątrz wnętrza komórkowego, niektóre takie jak translacja DNA, synteza aminokwasów i nukleotydów itp.
Riboza działa stale jako nośnik chemiczny wewnątrz komórki, ponieważ nukleotydy mogą przedstawić jedną, dwie grupy fosforanowe zjednoczone kowalencyjnie ze sobą przez bezwodne wiązania. Są one znane odpowiednio jako mono-, di- i trifosforan.
Związek między rybozą a fosforanem jest typu estra, hydroliza tego łącza uwalnia około 14 kJ/mol w standardowych warunkach, podczas gdy każdy z bezwodnych wiązań uwalnia około 30 kJ/mol.
Na przykład w rybosomach grupa rybozy 2'-hydroksylowa może tworzyć wiązanie wodorowe z różnymi aminokwasami, zjednoczeniem, który umożliwia syntezę białek z TRNA we wszystkich znanych żywych organizmach.
Trucizna większości węży zawiera fosfodiesterazę, która hydrolizuje nukleotydy z końca 3 ', które mają swobodny hydroksyl, rozkładając związki między hydroksylowymi 3' rybozy lub deksrybosa.
Może ci służyć: glikoliza aerobia: co to jest, reakcje, pośredniki glikolityczneW medycynie
W kontekstach leczniczych służy do poprawy wydajności i wydajności poprzez zwiększenie energii mięśni. Zespół przewlekłego zmęczenia jest również traktowany tym sacharydem, a także fibromialgii i niektórymi chorobami tętnicy wieńcowej.
W kategoriach zapobiegawczych stosuje się do uniknięcia zmęczenia mięśni, skurczów, bólu i sztywności po wysiłku u pacjentów z dziedzicznym zaburzeniem niedoboru deaminazy mioadenylanowej lub niedoborem amp deaminazy AMP.
Bibliografia
- Alberts, ur., Johnson, a., Lewis, J., Morgan, zm., Raff, m., Roberts, k., & Walter, p. (2015). Biologia komórki molekularnej (6 wyd.). Nowy Jork: Garland Science.
- Angyal, s. (1969). Skład i konformacja cukrów. Angewandte Chemie - Edycja międzynarodowa, 8(3), 157-166.
- Foloppe, n., & Mackerell, a. D. (1998). Właściwości konformacyjne grupy deoksyrybozy i rybozy kwasów nukleinowych: badanie mechaniczne kwantowe, 5647(98), 6669-6678.
- Garrett, r., I Grisham, C. (2010). Biochemia (Wydanie 4.). Boston, USA: Brooks/Cole. Cengage Learning.
- Guttman, ur. (2001). Nukleotydy i nukleozydy. Academic Press, 1360-1361.
- Mathews, c., Van Holde, K., & Ahern, K. (2000). Biochemia (3 wyd.). San Francisco, Kalifornia: Pearson.
- Mottram, d. S. (1998). Formacja smaku w mięsie i produktach mięsnych: recenzja. Chemia gastronomiczna, 62(4), 415-424.
- Nechamkin, godz. (1958). Subskurencje etmologiczne pochodne terminologii chemicznej. Terminologia chemiczna, 1-12.
- Nelson, zm. L., & Cox, m. M. (2009). Zasady biochemii lehninger. Omega Editions (Ed.). https: // doi.Org/10.1007/S13398-014-0173-7.2
- Shapiro, r. (1988). Prebiotyczna synteza rybozy: analiza krytyczna. Pochodzenie życia i ewolucja biosfery, 18, 71-85.
- Indeks Merck Online. (2018). Pobrano z www.RSC.ORG/MERCK-INDEX/MONOGOG/M9598/DRIBOSE?Q = nieautoryzować
- Waris, s., Pischetsrianer, m., & Salemuddin, m. (2010). Uszkodzenie DNA przez rybozę: hamowanie przy wysokich stężeniach rybozy. Indian Journal of Biochemistry & Biophysics, 47, 148-156.
- Webmd. (2018). Pobrano 11 kwietnia 2019 r. Z WWW.Webmd.com/witaminy/ai/incredientmono-827/ribose
- Wulf, s. 1., & Vandamme i. (1997). Synteza mikrobiologiczna d-libozy: proces deregulacji i fermentacji metabolicznej. Postępy w stosowanej mikrobiologii, 4, 167-214.
- Xu, z., Sha i., Liu, c., Li, s., Liang, J., Zhou, J., & Xu, h. (2016). Izomeraza libozy i izomeraza mannozy -6 -6 -fosforan: właściwości i zastosowania do produkcji L -LIBOZA. Mikrobiologia stosowana i biotechnologia, 1-9.

