Struktura Ovoalbúmin, funkcje, denaturacja
- 2814
- 845
- Paweł Malinowski
Ovoalbúmina Jest to najliczniejsze białko „wyraźnego” ptaków ptaków. Należy do rodziny białek znanej jako „węża” lub „inhibitory proteas serynowych”, która jest niezwykle zróżnicowaną grupą eukariotów (obejmuje ponad 300 białek homologicznych).
Było to jedno z pierwszych izolowanych białek o wielkiej czystości, a dzięki zaskakującej liczebności w strukturach reprodukcyjnych ptaków jest to szeroko stosowane jako „model” w przygotowaniu „standardów” do badania struktury, właściwości, właściwości , właściwości, właściwości, synteza i wydzielanie wielu białek.
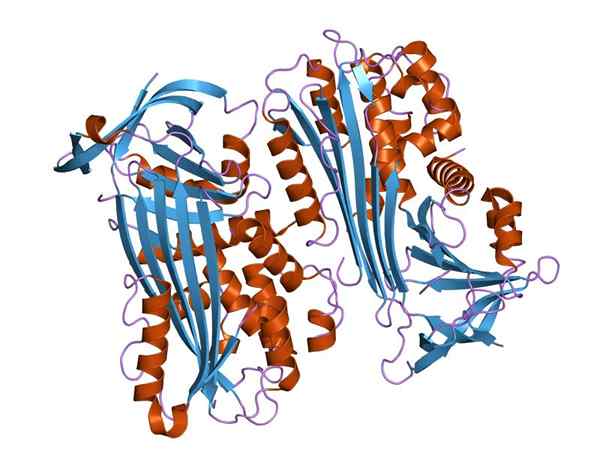
 Ovalbúmina Molecular Structure (Źródło: Jawahar Swaminathan i Personel MSD w European Bioinformatics Institute [Public Domena] za pośrednictwem Wikimedia Commons)
Ovalbúmina Molecular Structure (Źródło: Jawahar Swaminathan i Personel MSD w European Bioinformatics Institute [Public Domena] za pośrednictwem Wikimedia Commons) Pod względem procentowym, jajobumina obejmuje od 60 do 65% całkowitej zawartości białka białka w białku jaja, ale w przeciwieństwie do innych członków rodziny białek węża, nie ma aktywności jako inhibitor proteazy.
Jajka kurczaka mają również inne białka:
- Owotransferryna, zwana także Conalbúmina, która reprezentuje 13% całkowitej zawartości białka
- Jajukoid, glikoproteina, która obejmuje 11% całości
- Jajucyna, kolejna siarczkowa glikoproteina, która reprezentuje 3.5%
- Gładka lub muramidaza, która obejmuje również 3.5% czystego białka
- Globuliny, które reprezentują 4%
Synteza jajarza występuje z mieszaniny peptydów pośredniego podczas tranzytu jaja przez jajnik ptaków i istnieją doniesienia, że transkrypcja genów występuje tylko w odpowiedzi na obecność estrogenu, hormonu płciowego, hormonu płciowego.
[TOC]
Struktura
Ovoalbúmin jest monomeryczną fosfografią o masie cząsteczkowej około 45 kDa i punkcie izoelektrycznym blisko 4.5. Dlatego w swojej strukturze istnieje wiele miejsc do fosforylacji i glikozylacji, które są bardzo powszechnymi modyfikacjami po translacyjnej w białkach.
Może ci służyć: Biologia rozwoju: historia, jakie badania, aplikacjeTo białko jest kodowane przez 7 genów.700 par zasad, charakteryzującej się obecnością 8 eksonów przeplatanych 7 intronami, więc intuicja jest, że jego komunikator cierpi wiele modyfikacji posttranskrypcyjnych w celu wykonania dojrzałego białka.
Owalowa jaj kurzego ma 386 odpadów aminokwasowych i wykazano, że czysta postać tego białka składa się z trzech podklas zwanych A1, A2 i A3, charakteryzującym się odpowiednio dwóch, jednej i braku grupy fosforanowej.
Jeśli chodzi o strukturę trzeciorzędową, sekwencja aminokwasowa jajowowatą ujawnia obecność 6 reszt cysteinowych, wśród których powstają cztery mosty disiarczkowe. Ponadto niektóre badania strukturalne udowodniły, że N-końcowy koniec tego białka jest acetylizowany.
S-Ovoalbúmina
Gdy jaja są przechowywane, struktura jajbuminy jest modyfikowana, tworząc to, co jest znane w literaturze S-Ovalbumina, która jest bardziej stabilną formą przeciwko ciepłem i powstaje z powodu mechanizmów wymiany między disiarczkami i sulflorilami.
Oprócz temperatury przechowywania, ten „kształt” jajowód powstaje również w zależności od wewnętrznego pH jaj, czego można się spodziewać w dowolnym rodzaju białku w naturze.
S-Olbumina jest zatem, do której przypisywane są niektóre reakcje nadwrażliwości.
Funkcje
Chociaż jajowarka należy do rodziny białka charakteryzującego się jego aktywnością jako inhibitorów proteazy, nie ma aktywności hamującej, a jej funkcja nie została całkowicie wyjaśniona.
Jednak postawiono hipotezę, że potencjalną funkcją tego enzymu jest transport i przechowywanie jonów metali z i z zarodka. Inni autorzy zaproponowali, że działa to również jako źródło odżywcze zarodka podczas jego wzrostu.
Może ci służyć: noxaZ eksperymentalnego punktu widzenia Ovoalbúmina reprezentuje jedno z głównych białek „modelowych” dla różnych systemów badań strukturalnych, funkcjonalnych, syntezy i wydzielania białek, więc było bardzo ważne dla postępu w sprawach naukowych.
Funkcje dla przemysłu spożywczego
Ponadto, biorąc pod uwagę fakt, że jest to jedno z najliczniejszych białek w jajach kurze, jest to niezwykle ważne białko dla odżywiania ludzi i innych zwierząt, które żywią się jajami różnych ptaków.
W aspekcie kulinarnym jaja, a także reszta białek białek jaja są wykorzystywane do ich właściwości funkcjonalnych, szczególnie przez zdolność tworzenia pianki, proces, w którym polipeptydy są denaturowane, tworzą dyspersja.
Denaturacja
Ponieważ jajnik ma liczne grupy sulfodonowe, jest to dość reaktywne i łatwo denatulacyjne białko.
Temperatura denaturacji jajowskiej wynosi od 84 do 93 ° C, co stanowi 93, co charakteryzuje kształt S-Ovoalbúmin, który jest bardziej stabilny w wyższych temperaturach. Denaturacja jajowodu cieplnego powoduje tworzenie charakterystycznych białawych „żeli”, które są obserwowane podczas gotowania jaj.
 Smażone jaja (źródło: Whatmidoing [CC BY-SA 4.0 (https: // creativeCommons.Org/licencje/nabrzeże/4.0)] przez Wikimedia Commons)
Smażone jaja (źródło: Whatmidoing [CC BY-SA 4.0 (https: // creativeCommons.Org/licencje/nabrzeże/4.0)] przez Wikimedia Commons) PH jest również ważnym czynnikiem, gdy rozważana jest denaturacja tego białka, a także rodzaj i stężenie soli. W przypadku Ovoalbúmina pH denaturacji wynosi około 6.6.
Może ci służyć: dżungla tropikalna: flora, fauna, cechy, klimat, ulgaW różnych warunkach denaturacji cząsteczki jaja mają wysoką tendencję do dodawania, proces, który zwykle można przyspieszyć z dodaniem soli i wzrostem temperatury.
Zdolność jaja i innego białka białka jaja do tworzenia struktur typu żelowego, gdy są ogrzewane, a także ich zdolność do łączenia cząsteczek wody i funkcjonowania jako emulgatory, to te, które nadają im najważniejsze cechy funkcjonalne i powód, dla którego są one Tak wykorzystane szczególnie w branży spożywczej.
Proces denaturalizacji tego białka był bardzo przydatny do badania mechanizmów przejścia między stanami stałymi i żelowymi, a także do badania efektu, że różne typy soli mają różne stężenia (siła jonowa) na integralność integralności. białka.
Bibliografia
- Huntington, J. DO., & Stein, P. I. (2001). Struktura i właściwości owalbuminy. Journal of Chromatography B: Biomedical Sciences and Applications, 756 (1-2), 189-198.
- Koseki, t., Kitabatake, n., I doi i. (1989). Denaturacja i tworzenie liniowych agregatów jajarza. Hydrocolidy żywności, 3 (2), 123-134.
- Nisbet, a. D., Soundry, r. H., Moir, a. J., Fothergill, L. DO., & Fothergill, J. I. (1981). Całkowita sekwencja amino -kwas. European Journal of Biochemistry, 115 (2), 335-345.
- Phillips, g. ALBO., & Williams, p. DO. (Eds.). (2011). Podręcznik białek żywnościowych. Elsevier.
- Bold-o'donnell, e. (1993). Rodzina owalbuminy białek serpowych. FEBS Letters, 315 (2), 105-108.
- Sankar, zm. S., I Theis, H. W. (1959). Biosynteza owalbuminy. Nature, 183 (4667), 1057.
- Sharif, m. K., Salem, m., I Javed, K. (2018). Nauk o materiałach spożywczych w branży proszku jajowego. W roli nauk materiałowych w bioinżynierii żywności (PP. 505-537). Academic Press.
- Weijers, m., Barneveld, s. 1. DO., Cohen Stuart, m. DO., & Visschers, r. W. (2003). Denaturacja indukowana ciepłem i agregacja owalbuminy przy neutralnym pH opisanym przez nieodwracalną kinetykę ludź. Protein Science: A Publication of the Protein Society, 12 (12), 2693-2703.

