Struktura Notruro de Boro (BN), właściwości, uzyskiwanie, użycia
- 4936
- 237
- Filip Augustyn
On Azotek boru Jest to nieorganiczna substancja stała utworzona przez połączenie atomu boru (B) z atomem azotowym (N). Jego formuła chemiczna jest BN. Jest to bardzo odporna biała stała w wysokich temperaturach i jest dobrym kierowcą cieplnym. Jest używany na przykład do produkcji krzyżowców laboratoryjnych.
Boro nitrruro (BN) jest odporny na wiele kwasów, jednak ma pewną osłabienie ataków kwasu fluorowego i stopionego zasady. To dobry izolator elektryczny.
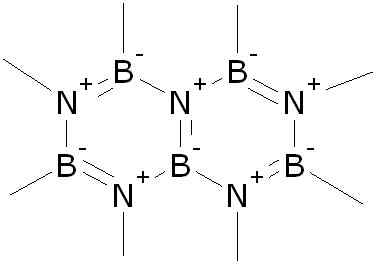
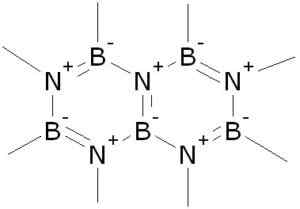 Struktura azotku boro (BN). Akeramop [domena publiczna]. Źródło: Wikimedia Commons.
Struktura azotku boro (BN). Akeramop [domena publiczna]. Źródło: Wikimedia Commons. Jest uzyskiwany w różnych strukturach krystalicznych, z których najważniejsze są sześciokątne i sześcienne. Struktura sześciokątna przypomina grafit i jest śliska, więc jest używana jako smar.
Struktura sześcienna jest prawie tak trudna jak diament i służy do produkcji narzędzi tnących i do poprawy twardości innych materiałów.
Za pomocą azotku boru można wyprodukować mikroskopijne rurki (wyjątkowo cienkie) zwane nanorurkami, które mają zastosowania medyczne, takie jak transport w ciele i uwalnianie leków przeciwko guzom raka.
[TOC]
Struktura
Boro nitrruro (BN) to związek, w którym atomy boru i azotu są łączone kowalencyjnie z potrójnym ogniwem.
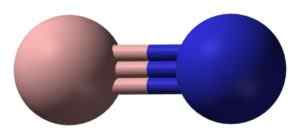 Izolowana cząsteczka azotku boru ma atom azotowy zjednoczony z potrójnym ogniwem. Benjah-BMM27 [domena publiczna]. Źródło: Wikimedia Commons.
Izolowana cząsteczka azotku boru ma atom azotowy zjednoczony z potrójnym ogniwem. Benjah-BMM27 [domena publiczna]. Źródło: Wikimedia Commons. W fazie stałej BN powstaje przez równą liczbę atomów boru i azotu w postaci 6 elementów.
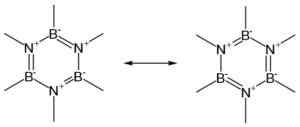 Struktury rezonansowe pierścienia BN. Autor: Teachi. Źródło: Wikimedia Commons.
Struktury rezonansowe pierścienia BN. Autor: Teachi. Źródło: Wikimedia Commons. Bn istnieje w czterech postaciach krystalicznych: sześciokątnych (H-BN) podobnych do grafitu, sześciennego (C-BN) podobnego do Diamond, Rhomboédica (R-BN) i Wurtzita (W-BN).
Struktura H-BN jest podobna do struktury grafitu, to znaczy ma heksagonalne płaszczyzny, które mają alternatywne atomy boru i azotu.
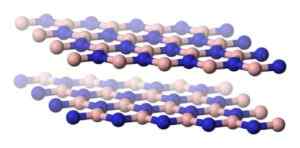 Struktura w postaci oddzielnych płaszczyzn sześciokątnego azotku boru. Benjah-BMM27 [domena publiczna]. Źródło: Wikimedia Commons.
Struktura w postaci oddzielnych płaszczyzn sześciokątnego azotku boru. Benjah-BMM27 [domena publiczna]. Źródło: Wikimedia Commons. Wśród samolotów H-BN istnieje duża odległość, która sugeruje, że są one zjednoczone tylko przez siły van der Waals, które są bardzo słabymi siłami przyciągania, a plany mogą z łatwością zsunąć się na siebie.
Może ci służyć: słońceZ tego powodu H-BN jest niezadowolony w dotyku.
Struktura sześciennego BN C-BN jest podobna do diamentu.
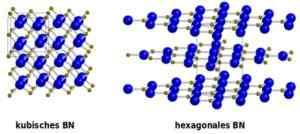 Porównanie sześciennego nitruro (po lewej) i sześciokątnej (po prawej). Od: Benutzer: Oddball, wersja wektorowa Chris 論 [domena publiczna]. Źródło: Wikimedia Commons.
Porównanie sześciennego nitruro (po lewej) i sześciokątnej (po prawej). Od: Benutzer: Oddball, wersja wektorowa Chris 論 [domena publiczna]. Źródło: Wikimedia Commons. Nomenklatura
Azotek boru
Nieruchomości
Stan fizyczny
Tłuste lub śliskie białe stałe do dotknięcia.
Waga molekularna
24,82 g/mol
Temperatura topnienia
Sublima w około 3000 ° C.
Gęstość
Heksagonalny BN = 2,25 g/cm3
Cubic BN = 3,47 g/cm3
Rozpuszczalność
Lekko rozpuszczalny w gorącym alkoholu.
Właściwości chemiczne
Z powodu silnego związku między azotem azotu i boru (potrójne wiązanie) ma wysoką odporność na atak chemiczny i jest bardzo stabilny.
Jest nierozpuszczalny w kwasach, takich jak kwas hydrochlorowy HCl, kwas azotowy HNO3 i kwas siarkowy H2południowy zachód4. Ale jest rozpuszczalny w stopionych zasadach, takich jak litotlenek litu, wodorotlenek potasu KOH i wodorotlenek sodu NaOH.
Nie reaguje z większością metali, szkła lub soli. Czasami reaguje z kwasem fosforowym H3PO4. Możesz oprzeć się utlenianiu w wysokich temperaturach. BN jest stabilny w powietrzu, ale woda powoli hydrolizuje.
BN jest atakowany przez fluorowy gaz2 oraz przez kwas fluorhorowy HF.
Inne właściwości fizyczne
Ma wysoką przewodność cieplną, wysoką stabilność termiczną i wysoką rezystywność elektryczną, to znaczy jest dobrym izolatorem energii elektrycznej. Ma wysoką powierzchnię.
H-BN (sześciokątna BN) jest solidnym do dotykania, podobnie jak grafit.
Podczas podgrzewania H-BN w wysokiej temperaturze i ciśnienie staje się kształtem sześciennym C-BN, który jest niezwykle trudny. Według niektórych źródeł jest w stanie zarysować diament.
Materiały oparte na BN mają pojemność sorpcyjną zanieczyszczeń nieorganicznych (takich jak jony metali ciężkich) i zanieczyszczenia organiczne (takie jak barwniki i cząsteczki leków).
Sorción oznacza, że wchodzi z nimi wchodzi w interakcje i może je adsorbować lub wchłaniać.
Uzyskanie
Pył H-BN jest wytwarzany przez reakcję między biOtlekiem boru B2ALBO3 lub kwas borowy h3Bo3 Z amoniakiem NH3 lub z mocznikiem NH2(Co) NH2 w atmosferze azotu n2.
Może ci służyć: Mount Olympus (Mars)BN można również uzyskać przez reakcję boru z amoniakiem w bardzo wysokiej temperaturze.
Innym sposobem na jego przygotowanie jest Diborano B2H6 i amoniak NH3 przy użyciu obojętnego gazu i wysokich temperatur (600-1080 ° C):
B2H6 + 2 NH3 → 2 Bn + 6 H2
Aplikacje
H-BN (sześciokątny bor nituro) ma wiele ważnych zastosowań opartych na jego właściwościach:
-Jako stały smar
-Jako addytywne dla kosmetyków
-W wysokiej temperaturze izolatorów elektrycznych
-W krzyżach i naczyniach reakcyjnych
-W formach i pojemnikach parowania
-Do przechowywania wodoru
-O katalizie
-Do adsorbowania zanieczyszczeń ścieków
Zastosowano sześcienne notruro boru (C-BN) ze względu na jego twardość prawie równą twardości Diamentu:
-W narzędzia tnące do obróbki twardych materiałów żelaznych, takich jak stalowe stopy stalowe, żeliwa i narzędzia
-Aby poprawić twardość i odporność na zużycie innych twardych materiałów, takich jak niektóre ceramiki na narzędzia tnące.
 Niektóre narzędzia tnące mogą zawierać nitruro boru, aby wykazać większą twardość. Autor: Michael Schwarzenberger. Źródło: Pixabay.
Niektóre narzędzia tnące mogą zawierać nitruro boru, aby wykazać większą twardość. Autor: Michael Schwarzenberger. Źródło: Pixabay. - Zastosowania cienkich warstw BN
Są bardzo przydatne w technologii urządzeń półprzewodnikowych, które są elementami sprzętu elektronicznego. Służą na przykład:
-Do produkcji płaskich diod; Diody to urządzenia, które w jednym sensie umożliwiają krążenie energii elektrycznej
-W diodach pamięci z metalowo-semiconductor, takich jak Al-Bn-Sio2-Tak
-W zintegrowanych obwodach jako ograniczenie napięcia
-Zwiększyć twardość niektórych materiałów
-Aby chronić niektóre materiały utleniania
-Zwiększyć stabilność chemiczną i izolacja elektryczna wielu rodzajów urządzeń
-W cienkowarstwowym skraplaczu
 Niektóre diody i kondensatory mogą zawierać azotek boru. Autor: Sinisa Maric. Źródło: Pixabay.
Niektóre diody i kondensatory mogą zawierać azotek boru. Autor: Sinisa Maric. Źródło: Pixabay. - Zastosowania nanorurek BN
Nanorurki to struktury, które na poziomie molekularnym kształtują się jak rurki. Są to rurki, które są tak małe, że można je zobaczyć tylko za pomocą specjalnych mikroskopów.
Poniżej znajdują się niektóre cechy nanorurek BN:
-Mają wysoką hydrofobowość, to znaczy odpychają wodę
-Mają wysoką odporność na utlenianie i ciepło (utlenianie może odporność do 1000 ° C)
-Wykazują wysoką pojemność wodoru
-Absorbują promieniowanie
-Są bardzo dobrymi izolatorami energii elektrycznej
Może ci służyć: termometr oporności: charakterystyka, operacja, użycia-Mają wysoką przewodność cieplną
-Jego doskonała odporność na wysokie utlenianie temperatur oznacza, że można je wykorzystać do zwiększenia stabilności do utleniania powierzchni.
-Ze względu na ich hydrofobowość można je wykorzystać do przygotowania super hydrofobowych powierzchni, to znaczy nie mają powinowactwa do wody, a woda ich nie przenika.
-Na przykład nanorurki BN poprawiają właściwości niektórych materiałów, zastosowano go do zwiększenia twardości i odporności na złamanie szklane.
 Nitubos nitruro boru zaobserwowany za pomocą mikroskopu. Keun jego Kim i in. [CC przez 4.0 (https: // creativeCommons.Org/licencje/według/4.0)]. Źródło: Wikimedia Commons.
Nitubos nitruro boru zaobserwowany za pomocą mikroskopu. Keun jego Kim i in. [CC przez 4.0 (https: // creativeCommons.Org/licencje/według/4.0)]. Źródło: Wikimedia Commons. W zastosowaniach medycznych
Nanorurki BN zostały przetestowane jako nosiciele leków przeciwnowotworowych, takich jak doksorubicyna. Niektóre kompozycje z tymi materiałami zwiększyły wydajność chemioterapii za pomocą wspomnianego leku.
W kilku doświadczeniach wykazano, że nanorurki BN mogą potencjalnie przetransportować nowe leki i poprawnie je uwolnić.
Zastosowanie nanorurek BN w biomateriałach polimerowych zostało zbadane w celu zwiększenia ich twardości, degradacji i prędkości trwałości. Są to materiały używane na przykład w implantach ortopedycznych.
Jako czujniki
Nanorurki BN zostały wykorzystane do budowy nowych urządzeń do wykrywania wilgoci, dwutlenku węgla2 i do diagnoz klinicznych. Czujniki te wykazały szybką reakcję i krótki czas regeneracji.
Możliwa toksyczność materiałów BN
Istnieje pewne obawy dotyczące możliwych toksycznych skutków nanorurek BN. Nie ma wyraźnego konsensusu co do jego cytotoksyczności, ponieważ niektóre badania wskazują, że są toksyczne dla komórek, podczas gdy inne wskazują na odwrotność.
Wynika to z jego hydrofobowości lub nierozpuszczalności w wodzie, ponieważ utrudnia przeprowadzanie badań w materiałach biologicznych.
Niektórzy badacze pokryli powierzchnię nanorurek BN innymi związkami, które sprzyjają ich rozpuszczalności w wodzie, ale zwiększyło to większą niepewność w doświadczeniach.
Chociaż większość badań wskazuje, że ich poziom toksyczności jest niski, szacuje się, że należy przeprowadzić bardziej precyzyjne badania.
Bibliografia
- Xiong, J. i in. (2020). Heksagonalny azotek boru Adsorbent: synteza, dostosowanie wydajności i zastosowania. Journal of Energy Chemistry 40 (2020) 99-111. Odzyskane od czytelnika.Elsevier.com.
- Mukasyan, a.S. (2017). Azotek boru. W zwięzłej encyklopedii samowystarczalnej syntezy w wysokiej temperaturze. Odzyskane z naukowym.com.
- Kalay, s. i in. (2015). Synteza nanorurek azotków boru i ich zastosowań. Beilstein J. Nanotechnol. 2015, 6, 84-102. NCBI odzyskało.NLM.Nih.Gov.
- Arya, s.P.S. (1988). Przygotowanie, właściwości i zastosowania cienkich warstw azotku boru. Cienkie folie solidne, 157 (1988) 267-282. Odzyskane z naukowym.com.
- Zhang, J. i in. (2014). Ceramiczne kompozyty matrycy zawierające azotek boru. W postępach w kompozytach macierzy ceramicznych. Odzyskane z naukowym.com.
- Bawełna, f. Albert i Wilkinson, Geoffrey. (1980). Zaawansowana chemia nieorganiczna. Czwarta edycja. John Wiley & Sons.
- Suanarsan, v. (2017). Materiały do wrogiego środowiska chemicznego. W materiałach w ekstremalnych warunkach. Odzyskane z naukowym.com
- Dean, J.DO. (redaktor) (1973). Podręcznik chemii Lange. McGraw-Hill Company.
- Mahan, ur.H. (1968). Chemia uniwersytecka. Inter -American Educational Fund, S.DO.

