Struktura metoksyetanu, właściwości, uzyskiwanie, zastosowania, ryzyko
- 3716
- 1115
- Pani Waleria Marek
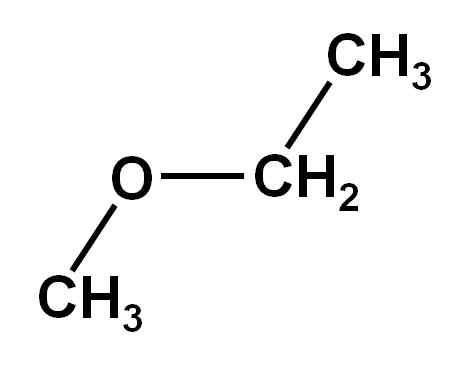
On Metoksyetan Jest to organiczny związek rodziny eterów lub alcoxides. Jego formuła chemiczna to Cho3Och2Ch3. Nazywa się to również eterem metylowym lub eterem etylowym. Jest to związany gaz gazowy w temperaturze pokojowej, a jego cząsteczka przedstawia dwie grupy metylowe3, jeden przymocowany bezpośrednio do tlenu, a drugi należący do etyl -ch2Ch3.
Metoxietano to bezbarwny gaz, rozpuszczalny w wodzie i mieszany z alkoholem eterycznym i alkoholem. Bycie eterem jest małym reaktywnym związkiem, jednak może reagować w wysokich temperaturach z niektórymi skoncentrowanymi kwasami.
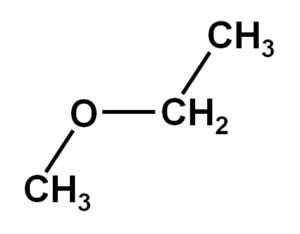 Metoksietano lub eter metylowy. Autor: Marilú Stea
Metoksietano lub eter metylowy. Autor: Marilú Stea Zasadniczo jest uzyskiwany przez SO -Called Synthese Williamson, która obejmuje stosowanie alkohotlenku sodu i jodku alkilowego. Z kolei jego rozkład był badany w kilku warunkach.
Metoxietano jest stosowany w laboratoriach badawczych o różnych celach, na przykład w badaniu nanomateriałów półprzewodników lub w obserwacji materii międzygwiezdnej w konstelacjach i dużych chmur cząsteczkowych wszechświata.
W rzeczywistości dzięki bardzo wrażliwym teleskopom (interferometrach) został wykryty w niektórych miejscach przestrzeni międzygwiezdnej.
[TOC]
Struktura
Związek metoksyetanu ma grupę metylową -ch3 i grupa etylowa -ch2Ch3 oba przymocowane do tlenu.
Jak widać, w tej cząsteczce istnieją dwie grupy metylowe, jedna przyłączona do tlenu Cho3-O i drugi należący do etyl2-Ch3.
W podstawowym lub niższym stanie energetycznym grupa metylowa -Ch2-Ch3 jest w pozycji trans W odniesieniu do metylu przywiązanego do2-ALBO. Dlatego czasami nazywa się to trans-Eter etylu metylowy.
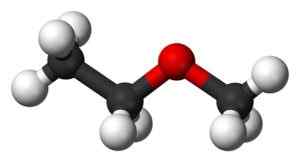 Struktura eteru transetylogrytylowego w 3D. Czarny karbon. Biały: wodór. Czerwony: tlen. Związek między tlenem a -ch2- może się obrócić, w takim przypadku dwa -chacie3 byliby bliżej siebie. Ben Mills i Jynto [domena publiczna]. Źródło: Wikipedia Commons.
Struktura eteru transetylogrytylowego w 3D. Czarny karbon. Biały: wodór. Czerwony: tlen. Związek między tlenem a -ch2- może się obrócić, w takim przypadku dwa -chacie3 byliby bliżej siebie. Ben Mills i Jynto [domena publiczna]. Źródło: Wikipedia Commons. Ta cząsteczka może doświadczyć skręcania w linku CHO2-Lub, który umieszcza metyl w innej pozycji przestrzennej od trans , Grupy metylowe3 Są bardzo blisko siebie, a skręt generuje przejście energii wykrywalne przez wrażliwe instrumenty.
Może ci służyć: kulisetria: podstawy, typy, aplikacjeNomenklatura
- Metoksyetan.
- Eter etylu metylu.
- trans-Eter ethil metylowy (głównie w literaturze anglojęzycznej, tłumaczenie na angielski trans-Eter etylu metylowy).
Właściwości fizyczne
Stan fizyczny
Bezbarwny gaz
Waga molekularna
60 096 g/mol
Temperatura topnienia
-113,0 ° C
Punkt wrzenia
7,4 ° C
Temperatura zapłonu
1,7 ° C (metoda zamkniętej kubka).
Temperatura samokierowania
190 ° C
Dokładna waga
0,7251 do 0 ° C/0 ºC (jest mniej gęste niż woda, ale cięższa niż powietrze).
Współczynnik załamania światła
1 3420 do 4 ° C
Rozpuszczalność
Rozpuszczalna w wodzie: 0,83 mole/l
Rozpuszczalne w acetonie. Mamiczne z alkoholem etylowym i eterem etylowym.
Właściwości chemiczne
Metoxietano jest eterem, więc jest stosunkowo mało reaktywny. Związek węgla-tlenek-węgiel C-O-C jest bardzo stabilny przed bazami, środkami utleniającymi i redukcjami. Wytwarza tylko degradację kwasu, ale przebiega tylko w energicznych warunkach, to znaczy ze skoncentrowanymi kwasami i wysokimi temperaturami.
Jednak ma tendencję do utleniania się w obecności powietrza tworzących niestabilne nadtlenki. Jeśli pojemniki zawierające go do ciepła lub pożaru są odsłonięte, pojemniki wykorzystują gwałtownie.
Rozkład ciepła
Gdy metoksyetan jest poddany ogrzewaniu między 450 a 550 ° C, jest podzielony na acetaldehyd, etan i metan. Ta reakcja jest katalizowana przez obecność jodku etylu, który jest na ogół obecny w próbkach laboratoryjnego metoksyetanu, ponieważ jest stosowany w jego uzyskiwaniu.
Rozkłada się na fotoczury
Metoksyetan napromieniowany lampą parową rtęci (długość fali 2537 Å) rozkłada się generując szeroką gamę związków, wśród których wyróżniają się: wodór, 2,3-dimetoksybtano, 1-etoksy-2-metoksypropanu i eteru eteru eterowego eteru eteru.
Produkty końcowe zależą od czasu napromieniowania próbki, ponieważ poprzez kontynuowanie napromieniowania, które początkowo tworzą nowe związki.
Przedłużając czas napromieniania, mogą one również tworzyć: propan, metanol, etanol, aceton, 2-butanon, tlenek węgla, eter etylo-N-Pro-propyl.
Uzyskanie
Ponieważ jest to nie symetryczny eter, metoksyetan można uzyskać przez reakcję między chemtlekiem sodu CH3Ona i Yoduro de Etilo CH3Ch2Siema. Ten rodzaj reakcji nazywa się syntezą Williamsona.
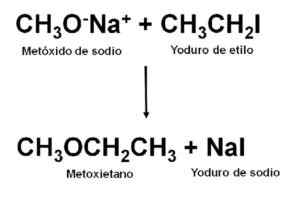 Uzyskanie metoksietano poprzez syntezę Williamsona. Autor: Marilú Stea.
Uzyskanie metoksietano poprzez syntezę Williamsona. Autor: Marilú Stea. Po wykonaniu reakcji mieszanina destyluje się w celu uzyskania eteru.
Może ci służyć: związki trójskładnikowe: cechy, szkolenie, przykładyMożna go również uzyskać przy użyciu etoksydu sodu CH3Ch2Ona i siarczan metylu (CH3)2południowy zachód4.
Lokalizacja we wszechświecie
On trans-Eter ethil metylowy został wykryty w połowie międzygwiezdnej w regionach takich jak konstelacja Orion KL i w gigantycznej chmurze molekularnej W51E2.
 Konstelacja orionów, w której obserwuje się chmury molekularne. Rogelio Bernal Andreo [CC BY-SA 3.0 (https: // creativeCommons.Org/licencje/by-sa/3.0)]. Źródło: Wikipedia Commons.
Konstelacja orionów, w której obserwuje się chmury molekularne. Rogelio Bernal Andreo [CC BY-SA 3.0 (https: // creativeCommons.Org/licencje/by-sa/3.0)]. Źródło: Wikipedia Commons. Wykrywanie tego związku w przestrzeni międzygwiezdnej wraz z analizą jego obfitości jest pomocne w budowie modeli chemii międzygwiezdnej.
Stosowanie metoksyetanu
Eter metoksietano lub eteru metyl.
Do badań nad materią międzygwiezdną
Będąc cząsteczką organiczną o obrotach wewnętrznych, Metoxietano jest chemicznym związkiem będącym przedmiotem badań materii międzygwiezdnej.
Wewnętrzne obroty ich grup metylowych wytwarzają przejścia energii w regionie mikrofalowym.
Dlatego można je wykryć za pomocą bardzo wrażliwych teleskopów, takich jak wielki milimetr/submylimetryczny zestaw Atacama lub dusza (akronim dla angielskiego Atacama Large Milmeth/Smurmeter tablica).
 Pojawienie się części wielkiego astronomicznego obserwatorium Almy. ESO/José Francisco Salgado (Josefrancisco.org) [CC przez 4.0 (https: // creativeCommons.Org/licencje/według/4.0)]. Źródło: Wikipedia Commons.
Pojawienie się części wielkiego astronomicznego obserwatorium Almy. ESO/José Francisco Salgado (Josefrancisco.org) [CC przez 4.0 (https: // creativeCommons.Org/licencje/według/4.0)]. Źródło: Wikipedia Commons. Dzięki jego wewnętrznej rotacji i wielkim obserwatoriom przestrzennym trans-Eter etylu metylowego znaleziono w konstelacji Oriona i w gigantycznej chmurze molekularnej W51E2.
Wywnioskować transformacje chemiczne w różnych dziedzinach studiów
Niektórzy badacze zaobserwowali tworzenie się metoksyetano lub eteru etylowego metylowego, gdy mieszanina etylenu CH jest promieniowana elektronami2= Ch2 I metanol ch3Oh.
Mechanizm reakcji przechodzi przez tworzenie się radykalnego CH3Lub •, który atakuje podwójne wiązanie bogate w elektrony Cho2= Ch2. Powstały addukt CH3-O-ch2-Ch2• Uchwyć wodór z Cho3Och i tworzy eter eterowy metyl3-O-ch2-Ch3.
Badanie tego rodzaju reakcji napromieniowania elektronów jest przydatne w dziedzinie biochemii, ponieważ ustalono, że uszkodzenie DNA może spowodować, lub w dziedzinie chemii organetalicznej, ponieważ sprzyja tworzeniu się nanostruktur.
Może ci służyć: wytrąćDodatkowo wiadomo, że duże ilości wtórnych elektronów powstają, gdy promieniowanie elektromagnetyczne lub cząsteczki oddziałują z materią skondensowaną w przestrzeni.
Dlatego szacuje się, że elektrony te mogą inicjować transformacje chemiczne w sprawie proszku międzygwiezdnego. Stąd znaczenie badania etylu metylowego w tych reakcjach.
Potencjalne zastosowanie w półprzewodnikach
Za pośrednictwem metod obliczeniowych niektórzy naukowcy stwierdzili, że metoksyetan lub eter metylowy może być zaadsorbowany przez grafen domowy z galu (GA) (zauważ, jaka adsorpcja różni się od wchłaniania).
Grafen jest nanomateriałem utworzonym przez atomy węgla, które są ułożone, tworząc sześciokątny wzór.
 Mikroskopowy widok grafenu. Maido Merisalu [CC BY-SA 4.0 (https: // creativeCommons.Org/licencje/nabrzeże/4.0)]. Źródło: Wikipedia Commons.
Mikroskopowy widok grafenu. Maido Merisalu [CC BY-SA 4.0 (https: // creativeCommons.Org/licencje/nabrzeże/4.0)]. Źródło: Wikipedia Commons. Adsorpcja metoksyetanu na grafenie Dopped występuje przez interakcję między tlenem eteru a atomem galu, który znajduje się na powierzchni nanomateriału. Z powodu tej adsorpcji występuje przeniesienie obciążenia netto z eteru do galu.
Po adsorpcji eteru etylowego metylowego i z powodu tego przeniesienia obciążenia grafen domowy galusem przedstawia właściwości półprzewodnika typu P.
Ryzyko
Metoxietano jest wysoce łatwopalne.
Pozostając w kontakcie z powietrzem, ma tendencję do tworzenia niestabilnych i wybuchowych nadtlenków.
Bibliografia
- LUB.S. National Library of Medicine. (2019). Eter etylu metylowy. Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov.
- Irvine w.M. (2019) eter etylu metylowy (c2H5Och3). W: Gargaoud m. i in. (Red.). Encyklopedia astrobiologii. Springer, Berlin, Heidelberg. Link odzyskał.Skoczek.com.
- Trzeci b. i in. (2015). Wyszukiwanie etylowo -metylowego etylu w Orion KL. Astronomia i astrofizyka. 582, L1 (2015). NCBI odzyskało.NLM.Nih.Gov.
- Filseth, s.V. (1969). Merkury 6 (3P1) Fotouczulezowane rozkład eteru metylowego etheru. The Journal of Physical Chemistry. Tom 73, numer 4, kwiecień 1969, 793-797. Odzyskane z pubów.ACS.org.
- Casanova, J.Jr. (1963). Przygotowanie uczniów i manipulacja eterem etheru gazowego. Journal of Chemical Education. Tom 40, numer 1, styczeń 1963. Odzyskane z pubów.ACS.org.
- Ure, w. I Young, J.T. (1933a). Na temat mechanizmu reakcji gazowych. Siema. Rozkład tematyczny eteru etylowego metylowego. The Journal of Physical Chemistry, t. Xxxvii, no.9: 1169-1182. Odzyskane z pubów.ACS.org.
- Ure, w. I Young, J.T. (1933b). Na temat mechanizmu reakcji gazowych. Ii. Homogeniczna kataliza w rozkładu metody Ethher Ethher. The Journal of Physical Chemistry, 37, 9, 1183-1190. Odzyskane z pubów.ACS.org.
- Shokuhi Rad, a. i in. (2017). Badanie DFT na temat adsorpcji eterów dietylu, ethylu i dimetylu na powierzchni grafenu domieszkowanego galem. Stosowana nauka powierzchniowa. Tom 401, 15 kwietnia 2017 r., Strony 156-161. Odzyskane z naukowym.com.
- Schmidt, f. i in. (2019). Indukowane elektronem tworzenie eteru etyltylowego w skondensowanych mieszanin metanolu i etylenu. J. Phys. Chem. A 2019, 123, 1, 37-47. Odzyskane z pubów.ACS.org.

