Masa molowa Jak jest obliczana, rozwiązane przykłady i ćwiczenia
- 1723
- 94
- Matylda Duda
Masa cząsteczkowa Jest to intensywna właściwość materii, która odnosi koncepcję mol z pomiarami masowymi. Jest bardziej zwięzły, jest to ilość masy odpowiadającej mol substancji; to znaczy, co „waży” liczbę Avogadro (6.022 · 1023) z niektórych cząstek.
Jeden kret dowolnej substancji będzie zawierał tę samą liczbę cząstek (jony, cząsteczki, atomy itp.); Jednak jego masa będzie się różnić, ponieważ jego wymiary cząsteczkowe są zdefiniowane przez liczbę atomów i izotopów, które tworzą jego strukturę. Im bardziej masa atom lub cząsteczka, tym największa jej masa trzonowa.
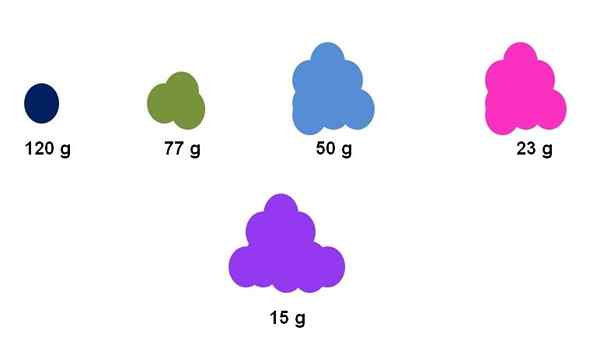
 Różnica między masami molowymi różnych substancji może być powierzchownie zauważona przez pozorną ilość ich próbki. Źródło: Gabriel Bolívar.
Różnica między masami molowymi różnych substancji może być powierzchownie zauważona przez pozorną ilość ich próbki. Źródło: Gabriel Bolívar. Załóżmy na przykład, że dokładnie jeden mol spotyka się dla pięciu różnych związków (obraz doskonały). Za pomocą równowagi ciasto zostało zmierzone dla każdego klastra, wyrażone poniżej. Ta masa odpowiada ciastowi trzonowe. Ze wszystkich fioletowych związku jest tym z jaśniejszymi cząsteczkami, podczas gdy ciemnoniebieski związek, najcięższe cząstki.
Zauważ, że pokazano uogólnioną i przesadną tendencję: im większa masa molowa, tym niższa ilość próbki, którą należy umieścić w równowadze. Jednak ta objętość materii zależy również znacznie od stanu agregacji każdego związku i jego gęstości.
[TOC]
Jak obliczane jest ciasto molowe?

Definicja
Masę molową można obliczyć na podstawie jej definicji: ilość masy na kret substancji:
M = gram substancji /mol substancji
W rzeczywistości g/mol jest jednostką, w której masa molowa jest zwykle wyrażana, obok kg/mol. Tak więc, jeśli wiemy, ile pieprzyków mamy z związku lub elementu, i ważymy go, osiągniemy jego masę molową, stosując prosty podział.
Może ci służyć: Justus von LiebigRzeczy
Masa molowa dotyczy nie tylko związków, ale także do pierwiastków. Pojęcie moli wcale nie dyskryminuje. Dlatego przy pomocy okresowej tabeli umieszczamy względne masy atomowe dla elementu zainteresowania i mnożymy jego wartość przez 1 g/mol; To jest stała Avogadro, MLUB.
Na przykład względna masa atomowa strontu wynosi 87,62. Jeśli chcemy mieć swoją masę atomową, wynosiłoby to 87,62 UMA; Ale jeśli szukamy masy molowej, będzie ona wynosi 87,62 g/mol (87,62 · 1 g/mol). I tak, masy molowe wszystkich innych elementów są uzyskiwane w ten sam sposób, nawet nie dokonując takiego mnożenia.
Związki
Masa molowa związku jest niczym więcej niż sumą względnych mas atomowych jego atomów pomnożonych przez MLUB.
Na przykład cząsteczka wody, h2Lub ma trzy atomy: dwa wodoru i jeden z tlenu. Względne masy atomowe H i O wynoszą odpowiednio 1008 i 15999. W ten sposób dodajemy jego masy mnożące się przez liczbę atomów obecną w cząsteczce złożonej:
2 H · (1,008) = 2 016
1 O · (15 999) = 15 999
M(H2O) = (2 016 + 15 999) · 1 g/mol = 18 015 g/mol
Pominięcie jest dość powszechną praktyką MLUB na końcu:
M(H2O) = (2 016 + 15 999) = 18 015 g/mol
Rozumie się, że ciasto trzonowe ma jednostki g/mol.
Przykłady
Właśnie wspomniano o jednej z najbardziej znanych mas molowych: woda, 18 g/mol. Ci, którzy zapoznają się z tymi obliczeniami, osiągają punkt, w którym są zdolni do zapamiętania niektórych mas molowych, nie szukając ich ani ich obliczania, jak to się stało. Niektóre z tych mas molowych, które służą jako przykłady, są następującymi:
Może ci służyć: zalety i wady chemii zdrowia-ALBO2: 32 g/mol
-N2: 28 g/mol
-NH3: 17 g/mol
-Ch4: 16 g/mol
-WSPÓŁ2: 44 g/mol
-HCl: 36,5 g/mol
-H2południowy zachód4: 98 g/mol
-Ch3COOH: 60 g/mol
-Wiara: 56 g/mol
Zauważ, że podane wartości są zaokrąglone. Do bardziej precyzyjnych celów masy molowe z bardziej dziesiętnym muszą być wyrażone i obliczone z należytymi i dokładnymi względnymi masami atomowymi.
Rozwiązane ćwiczenia
Ćwiczenie 1
Za pomocą metod analitycznych oszacowano, że rozwiązanie próbki zawiera 0,0267 moli analitu D. Wiadomo również, że jej masa odpowiada 14% próbki, której całkowita masa wynosi 76 gramów. Obliczyć masę molową domniemanego analitu D.
Musimy określić masę D, która jest rozpuszczona w roztworze. Postępujemy:
Masa (d) = 76 g · 0,14 = 10,64 g d
Oznacza to, że obliczamy 14% z 76 gramów próbki, które odpowiadają gramom analitu D. Następnie i na koniec stosujemy definicję masy molowej, ponieważ mamy wystarczające dane, aby ją obliczyć:
M(D) = 10,64 g d/ 0,0267 moli d
= 398,50 g/mol
Co tłumaczy: jeden mol (6.022 · 1023) Z i ma masę równą 398,50 gramów. Dzięki tej wartości możemy wiedzieć, ile i chcemy ważyć równowagę na przykład, na przykład, przygotować roztwór stężenia molowego wynoszącego 5,10-3 M; to znaczy, rozpuść 0,1993 gramów i w litrach rozpuszczalnika:
5 · 10-3 (mol/l) · (398,50 g/mol) = 0,1993 g i
Ćwiczenie 2
Oblicz masę molową kwasu cytrynowego, wiedząc, że jego wzór cząsteczkowy wynosi C6H8ALBO7.
Ta sama formuła C6H8ALBO7 Ułatwia zrozumienie obliczeń, ponieważ mówi nam, że liczba atomów C, H i lub lub że występują w kwasie cytrusowym. Dlatego powtarzamy ten sam krok wykonany dla wody:
Może ci służyć: Dodecil Siarczan sodu (SDS): Struktura, właściwości, zastosowania6 C · (12 0107) = 72 0642
8 H · (1 008) = 8 064
7 O · (15 999) = 111 993
M(kwas cytrynowy) = 72 0642 + 8,064 + 111,993
= 192 1212 g/mol
Ćwiczenie 3
Oblicz ciasto molowe siarczanu miedzi pentahydratu, cuo4· 5H2ALBO.
Wiemy, zanim masa molowa wody wynosi 18 015 g/mol. Służy to uproszczeniu obliczeń, ponieważ na razie pomijamy je i skupiamy się na bezwodnej soli4.
Mamy, że względne masy atomowe miedzi i siarki wynoszą odpowiednio 63 546 i 32 065. Dzięki tym danemu postępujemy w taki sam sposób, jak w ćwiczeniu 2:
1 cu · (63 546) = 63 546
1 s · (32 065) = 32 065
4 O · (15 999) = 63 996
M(Cuso4) = 63 546 + 32 065 + 63,996
= 159 607 g/mol
Ale jesteśmy zainteresowani ciastem trzonowym pentahydratu, a nie bezwodnym. Aby to zrobić, musimy dodać do wyniku odpowiedniej masy wody:
5 godzin2O = 5 · (18 015) = 90,075
M(Cuso4· 5H2O) = 159 607 + 90,075
= 249 682 g/mol
Bibliografia
- Whitten, Davis, Peck i Stanley. (2008). Chemia. (8 wyd.). Cengage Learning.
- Wikipedia. (2020). Masa cząsteczkowa. Źródło: w:.Wikipedia.org
- Nissa Garcia. (2020). Czym jest masa trzonowa? Definicja, formuła i egzaminy. Badanie. Odzyskane z: Study.com
- Dr. Kristy m. Bailey. (S.F.). Samouczek stechiometrii
Znalezienie masy molowej. Źródło: OCC.Edu - Helmestine, Anne Marie, pH.D. (2 grudnia 2019 r.). Przykładowy przykład masowej molowej. Odzyskane z: Thoughtco.com
- « Darmstadtio Discovery, struktura, właściwości, użycia
- Woda lub etapy cyklu hydrologicznego i znaczenie »

