Isomería
- 2349
- 497
- Pani Waleria Marek
Co to jest izomeria?
Isomería jest zjawiskiem chemicznym, w którym cząsteczki o tej samej liczbie atomów mają różne właściwości chemiczne lub fizyczne. Zatem występuje w izomerach, które z kolei są cząsteczkami, których wzory chemiczne są takie same, ale ich struktury lub przepisy przestrzenne różnią się znacznie od siebie.
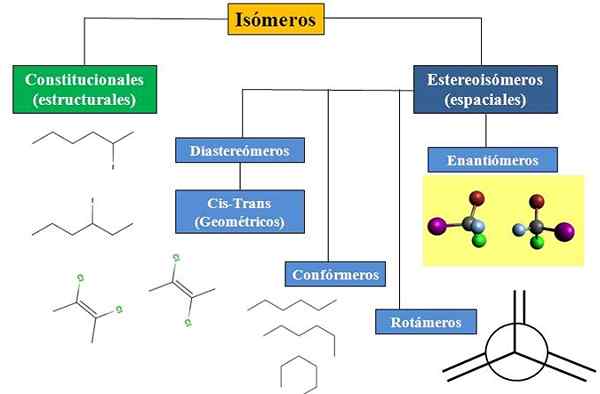
Mamy izomerię konstytucyjną lub strukturalną i izomerię kosmiczną, która koncentruje wiele uwagi w stereochemii. Niższy schemat przepływu obrazu pokazuje, że izomery są głównie podzielone na dwa typy izomerii: konstytucyjne i stereoizomery.
 Schemat przepływu dla różnych rodzajów izomerów w chemii organicznej. Źródło: Gabriel Bolívar.
Schemat przepływu dla różnych rodzajów izomerów w chemii organicznej. Źródło: Gabriel Bolívar. Wszystkie izomery dla pewnego związku mają ten sam wzór chemiczny. Ale struktury, które mogą budować te atomy i ich proporcje, są unikalne dla każdej cząsteczki lub izomeru. Ponadto, nawet jeśli sama struktura jest taka sama, atomy lub grupy mogą zajmować różne pozycje przestrzenne.
Na schemacie przepływu pokazano niektóre przykłady izomerów, które zostaną omówione w następnych sekcjach.
Rodzaje izomerów
Konstytucyjny
Izomery konstytucyjne lub strukturalne to te, które różnią się w porządkowaniu szkieletu molekularnego. Oznacza to, że ich atomy nie są powiązane w ten sam sposób, więc dane struktura lub grupy funkcjonalne mogą stać się bardzo różne.
Na przykład dla tej samej wzoru chemicznego C7H10Lub może istnieć wiele cząsteczek, które spełniają tę liczbę atomów; Wszystko będzie miało pojedynczy atom tlenu, ale strukturalne rozmieszczenie innych atomów będzie unikalne dla każdego izomeru.
A zatem właściwości chemiczne i fizyczne wszystkich izomerów konstytucyjnych dla wzoru C7H10Czy też znacznie się różnią od siebie.
Z drugiej strony izomery konstytucyjne mogą być bardzo proste, różni się tylko w względnej pozycji jednego atomu lub grupy. W poniższej sekcji będzie widoczny przykład tego i powyższego.
Stereoizomery
Stereoizomery to te, które mają ten sam porządek strukturalny, ale różnią się pozycjami przestrzennymi i orientacjami ich atomów lub grup.
Może ci służyć: modulowana amplitudaAby ich istnienie było możliwe, cząsteczki muszą zawierać centra stereogeniczne, będąc najbardziej znanym w chemii organicznej asymetryczne lub chiralne atomy węgla; to znaczy z czterem różnymi podstawnikami.
Oprócz asymetrycznych węgli, rozważana cząsteczka musi brakować elementów symetrii. W przeciwnym razie system przestrzenny nie może naliczyć stereoizomu.
Enancjomery
Enancjomery to stereoizomery, które składają się z nie narzucających lustrzanych obrazów. Na przykład prawe i lewe ręce nie są nakładające się, podobnie jak buty lub rękawiczki. W poniższej sekcji omówiono klasyczny przykład enantiomeía: Bromocloreyodometan: CBRCI.
Diastreomeres
Z drugiej strony distreomeres są również stereoizomery. To znaczy, że jedno przed drugim nie są odzwierciedleniem siebie. Z najbardziej znanych rozkurczów mamy izomerię CIS-Trans, zwaną także izomerie geometryczne, zwłaszcza gdy zastosowano do alkenów.
Conformeros
Konformatorzy, nawet jeśli znajdują się w spektrum stereoizomu, nie są tak naprawdę izomerami. Są to konfiguracje przestrzeni, które cząsteczka, w określonym czasie lub stanie energetycznym, nabywa przez obroty kilku swoich linków. Przykład konformerów N-heksan.
Rotámeros
Wreszcie mamy rotarmery, które przypominają konformery w tym sensie, które zależą od obrotu wiązań kowalencyjnych.
Jednak pojedynczy związek między dwoma atomami węgla jest przyjmowany jako odniesienie, a pozycje względne są porównywane, zaćmienie lub naprzemiennie, podstawników obu węgli. Później będzie widoczny przykład rotarmerów propylenu.
Przykłady izomerów
Jod heksanowy
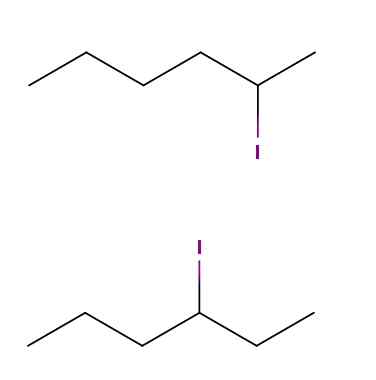 Konstytucyjne izomery jodu szesnastkowego. Źródło: Gabriel Bolívar przez Molview.
Konstytucyjne izomery jodu szesnastkowego. Źródło: Gabriel Bolívar przez Molview. Powyżej mamy dwie cząsteczki, których wzory chemiczne to C6H13Siema. W pierwszym mamy 2-jodheksan, podczas gdy w drugim 3-jodheksanie. Są to izomery konstytucyjne, ponieważ szkielet jest taki sam, z różnicą, że położenie atomu jodowego zmienia się w zależności od węgla do drugiego.
Może ci służyć: tarcie statyczne: współczynnik, przykład, ćwiczenieC3H8ALBO
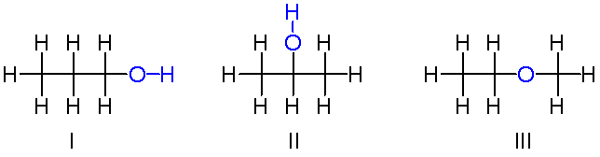 Źródło: V8RIK, CC BY-SA 3.0, Via Wikimedia Commons
Źródło: V8RIK, CC BY-SA 3.0, Via Wikimedia Commons W górę mamy inny przykład izomerów konstytucyjnych dla wzoru chemicznego C3H8ALBO. Cząsteczki I i II są odpowiednio 1-propanol i 2-propanol. Oba są alkoholami. Zamiast tego cząsteczka III to etyl-metylokoter.
Dlatego mówimy o innej grupie funkcjonalnej. Zauważ, że trzy cząsteczki mają taką samą liczbę atomów, ale ich struktury są różne.
2,3-decloro-2-buten
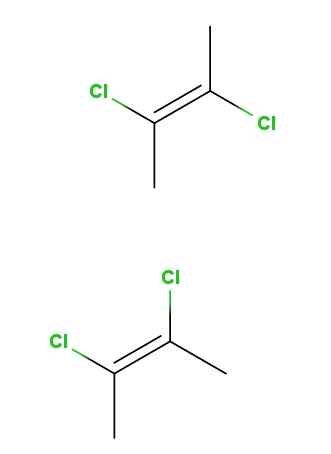 Geometryczne izomery 2,3-decloro-2-butenu. Źródło: Gabriel Bolívar przez Molview.
Geometryczne izomery 2,3-decloro-2-butenu. Źródło: Gabriel Bolívar przez Molview. W górę mamy izomer trans-22,3-decloro-2, a poniżej cis-2,3-dichloro-2-buten izomer. W pierwszym atomy chloru znajdują się w przeciwnych pozycjach w odniesieniu do podwójnego wiązania, podczas gdy w drugiej leżą po tej samej stronie podwójnego wiązania.
Szkielet dla obu cząsteczek jest taki sam, ale różni się w pozycjach przestrzennych atomów chloru; Dlatego są stereoizomerami i nie są obrazami lustrzanymi, stają się damereomerami.
3-Flúor-2-metylcykloheksan
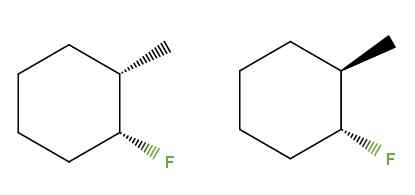 3-flúor-2-metylcycloheksano diastereomery. Źródło: Gabriel Bolívar przez Molview.
3-flúor-2-metylcycloheksano diastereomery. Źródło: Gabriel Bolívar przez Molview. Tym razem, zamiast podwójnego wiązania, mamy pierścień cykloheksanu dla związku 3-Flúor-2-metylcykloheksan. W izomerze po lewej grupy3 i F znajdują się poniżej płaszczyzny pierścienia; Po prawej stronie, Cho3 jest w górę i f poniżej.
Dlatego ten po lewej odpowiadałby izomerze cis, a tym po prawej byłby izomer trans. Są zatem diamereomerami, ponieważ nie są to znowu obrazy dne.
Conformeros del N-heksan
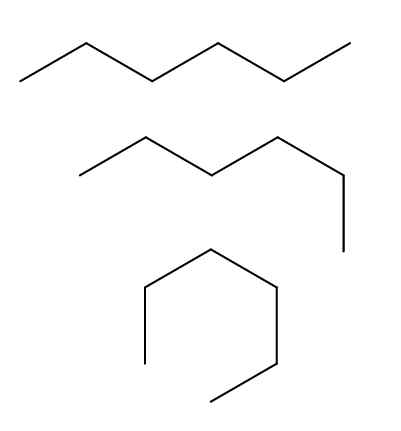 Konformery N-heksanu. Źródło: Gabriel Bolívar przez Molview.
Konformery N-heksanu. Źródło: Gabriel Bolívar przez Molview. Mamy trzech konformerów N-Heksano, które wynikają z obrotów i „fałd” węglanego łańcucha w różnych orientacjach. Wszystkie odpowiadają tej samej cząsteczce N-Heksan o różnych poziomach składania, który będzie zależeć od środowiska i energii wewnętrznej każdej cząsteczki.
3-bromo-2-penol
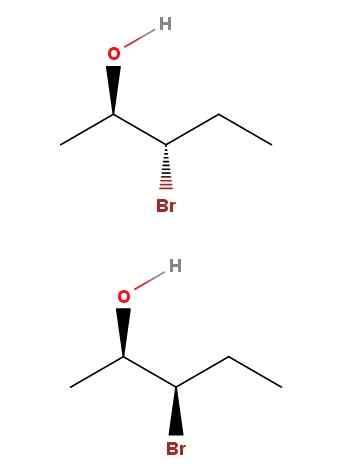 Diastroomery 3-bromo-2-pentanolu. Źródło: Gabriel Bolívar przez Molview.
Diastroomery 3-bromo-2-pentanolu. Źródło: Gabriel Bolívar przez Molview. W 3-bromo-2-pantanolu mamy inny przykład pary diastereomerów. Zauważ, że po raz kolejny w powyższym izomerze mamy OH i BR skierowane do kierunków sprzecznych z płaszczyzną szkieletu; Podczas gdy w poniższym izomerze obie grupy wskazują w kierunku czytelnika.
Może ci służyć: drugie prawo termodynamiki: wzory, równania, przykłady1-bromo-3-chloro-5-etylcykloheksan
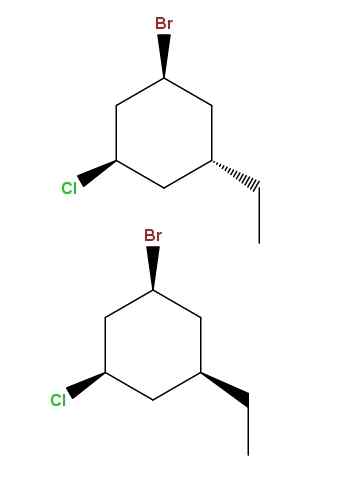 Diastreomery 1-bromo-3-clor-5-etylcykloheksanu. Źródło: Gabriel Bolívar przez Molview.
Diastreomery 1-bromo-3-clor-5-etylcykloheksanu. Źródło: Gabriel Bolívar przez Molview. I po raz kolejny mamy kolejną parę diastereomerów, z różnicą, jaką teraz różnica polega na pozycji przestrzennej jednej grupy: etyl, -ch2Ch3.
Ten typ izomerów ma bardzo specyficzną nazwę: śpiółki, które są diastheomerami, których zmienność obserwuje się tylko w konfiguracji przestrzennej pojedynczego asymetrycznego węgla; W tym przypadku ten, który jest powiązany z -ch2Ch3.
Bromokloreyodometan
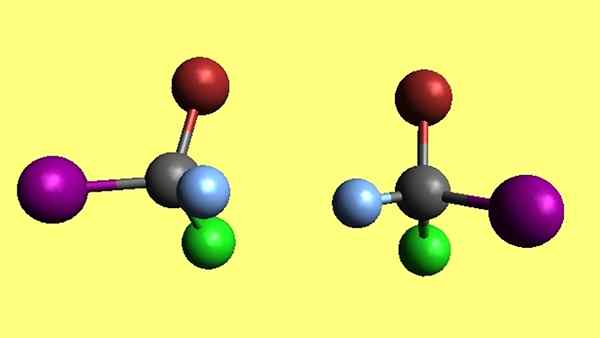 Para enantymerów bromokloreyodometanowych. Źródło: Gabriel Bolívar.
Para enantymerów bromokloreyodometanowych. Źródło: Gabriel Bolívar. Należy zauważyć, że dwie cząsteczki bromokloroyodometanu, CBRCLI, są enancjomerami, ponieważ jedno jest nie do zniesienia odbicia drugiego. Choć próbujesz, twoje cztery atomy nigdy się nie pokrywają. Mówi się, że mają przeciwne konfiguracje przestrzeni.
2-bromo-4-etylcykloheksan
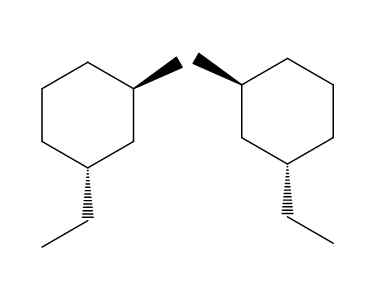 Inantimery 2-bromo-4-etylcykloheksanu. Źródło: Gabriel Bolívar przez Molview.
Inantimery 2-bromo-4-etylcykloheksanu. Źródło: Gabriel Bolívar przez Molview. W przykładzie momentu obrotowego cząsteczek 2-bromo-4-etylocykloheksanu. Jeśli spróbujemy odwrócić prawą cząsteczkę, zobaczymy, że grupa -ch2Ch3 Nie będzie znajdował się poniżej pierścienia, ale powyżej.
Podobnie Cho3 Nie wskazuje pierścienia, ale poniżej. Ustawienia przestrzeni są inwestowane, są odwrotne. To kolejna z najważniejszych cech Enatiomeía.
Rotámeros del propileno
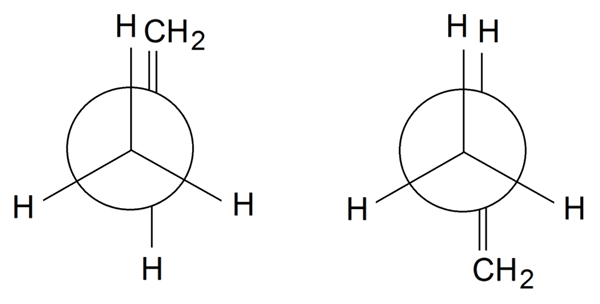 Rotámeros del propileno. Źródło: Samuele Madini, CC BY-SA 4.0, Via Wikimedia Commons
Rotámeros del propileno. Źródło: Samuele Madini, CC BY-SA 4.0, Via Wikimedia Commons W Rotámeros del propileno, aby zakończyć, obracamy prosty związek między C1 i C2: H3C-ch = ch2. Grupa = ch2 Jest w przyćminie z jednym z H3 Z przodu w Rotamerze po lewej stronie. Tymczasem = CHO2 A H są w pozycjach naprzemiennych w prawej stronie.
W zależności od zaćmienia lub nie grup, będziemy mieli przeszkodę, która destabilizuje Rotamero. Dlatego prawa rota rota jest bardziej stabilna niż ta po lewej stronie.
Bibliografia
- Graham Solomons t.W., Craig b. Fryhle. (2011). Chemia organiczna. (10th Wydanie.). Wiley Plus.
- Carey f. (2008). Chemia organiczna. (Szósta edycja). MC Graw Hill.
- Morrison i Boyd. (1987). Chemia organiczna. (Piąta edycja). Addison-Wesley Iberoamericana.
- Dr. S. Gevorg. (2020). Enancjomery, diastreomery, identyczne lub konstytucyjne izomery. Kroki chemii. Odzyskane z: chemistroodss.com
- Wikipedia. (2020). Izomer. Źródło: w:.Wikipedia.org
- Allison Soult. (13 sierpnia 2020). Izomery. Chemia librettexts. Odzyskane z: chem.Librettexts.org
- James Ashenhurst. (2020). Stereochemia i chiralność. Odzyskane z: MastorganicChemistry.com

