Wodorotlenek amonu
- 3692
- 501
- Maksymilian Kępa
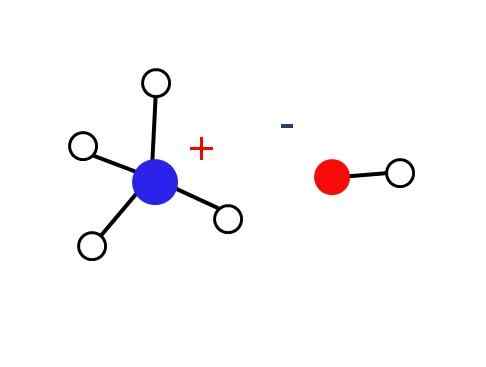
 Interakcja elektrostatyczna jonów amonu i wody. Źródło: Gabriel Bolívar
Interakcja elektrostatyczna jonów amonu i wody. Źródło: Gabriel Bolívar Co to jest wodorotlenek amonu?
On Wodorotlenek amonu Jest to związek molekularny NH4Oh5Nie jest to wytwarzane przez roztwór gazu amoniaku (NH3) W wodzie. Z tego powodu otrzymuje nazwy wody w płynnym amoniaku lub amoniaku.
Jest to bezbarwny płyn i bardzo intensywny i ostry, a nie izolowany zapach. Te cechy mają bezpośredni związek ze stężeniem NH3 Rozpuszczone w wodzie, stężenie, które może obejmować ogromne ilości amoniaku rozpuszczone w niewielkiej objętości wody, ponieważ jest to gaz.
Znacznie niewielka część tych roztworów wodnych składa się z kationów NH4+ I OH Aniony-.
Z drugiej strony, w bardzo rozcieńczonych roztworach lub w zamrożonych ciałach stałych w bardzo niskich temperaturach, amoniak można znaleźć w postaci hydratów, takich jak: NH3∙ h2Lub 2nh3∙ h2Lub NH3∙ 2H2ALBO.
Struktura chemiczna wodorotlenku amonu
Wodorotlenek amonu składa się z wodnego roztworu gazowego amoniaku. Dlatego w cieczy nie ma określonej struktury, która nie jest losowa usuwanie jonów NH4+ I och- Solwatowane przez cząsteczki wody.
Jony amonu i hydroksylowe są wynikiem równowagi hydrolizy amoniaku, więc te roztwory często mają przenikliwy zapach:
NH3(g) + h2Lub (l) NH4+(AC) + OH-(AC)
Zgodnie z równaniem chemicznym wysoki spadek stężenia wody wyparłby równowagę do największego tworzenia się amoniaku, to znaczy, ponieważ wodorotlenek amonu jest ogrzewany, zostaną uwolnione opary amoniaku.
Z tego powodu jony NH4+ I och- Nie tworzą kryształu w warunkach naziemnych, co powoduje solidną podstawę NH4Och, nie istnieje.
Wspomniane ciało stałe powinny składać się tylko z jonów oddziałujących elektrostátycznie (jak widać na obrazie).
Fizyczne i chemiczne właściwości
Formuła molekularna
NH4Oh5NIE
Waga molekularna
35 046 g/mol
Aspekt
Bezbarwny płyn.
Stężenie
Do około 30% (dla jonów NH4+ I och-).
Zapach
Bardzo mocne i ostre.
Smak
Akr.
Wartość progowa
34 ppm do niespecyficznego wykrywania.
Punkt wrzenia
38 ° C (25%).
Rozpuszczalność
Jest tylko w roztworze wodnym.
Rozpuszczalność wody
Mieszalne w nieograniczonych proporcjach.
Gęstość
0,90 g/cm3 w 25 ° C.
Gęstość pary
W stosunku do powietrza uznanego za jednostkę: 0,6. To znaczy jest mniej gęste niż powietrze. Jednak logicznie zgłaszana wartość odnosi się do amoniaku jako gazu, a nie jego roztworów wodnych lub NH4Oh.
Może ci służyć: moment dipolarny: jak jest obliczany i przykładyCiśnienie pary
2.160 mmHg w 25 ° C.
Działanie korozyjne
Jest w stanie rozpuścić cynk i miedź.
Ph
11.6 (rozwiązanie 1 N); 11.1 (roztwór 0,1 N) i 10,6 (roztwór 0,01 N).
Stała dysocjacji
PKB = 4767; KB = 1,71 x 10-5 w 20 ° C
PKB = 4751; KB = 1774 x 10-5 w 25 ° C
Wzrost temperatury prawie niezauważalnie zwiększa zasadowość wodorotlenku amonu.
Nomenklatura
NH4Och, otrzymuje wspólne i oficjalne nazwiska, zgodnie z przepisami IUPAC. Nazywa się wodorotlenek amonu do zawierania anionu hydroksylowego.
Amonium dla jego obciążenia +1 jest monowalentne, więc użycie nomenklatury zapasowej nazywane jest wodorotlenkiem amonu (I).
Ale zastosowanie „wodorotlenku amonu” jest technicznie niepoprawne, ponieważ związek nie jest izolowany (przynajmniej nie na Ziemi, jak wyjaśniono w pierwszej sekcji).
Otrzymuje również nazwy wody z płynnego amoniaku i amoniaku.
Rozpuszczalność
Jak NH4OH nie istnieje jako sól w warunkach naziemnych, nie można oszacować, jak rozpuszczalny jest w różnych rozpuszczalnikach.
Można jednak oczekiwać, że będzie bardzo rozpuszczalny w wodzie, ponieważ jego rozwiązanie wydałoby ogromne ilości NH3.
Teoretycznie byłby to niesamowity sposób przechowywania i transportu amoniaku.
W innych rozpuszczalnikach zdolnych do przyjmowania mostów wodorowych, takich jak alkohole i aminy, można się spodziewać, że będzie on również bardzo rozpuszczalny. Tutaj kation NH4+ Jest dawcą mostów wodorowych i OH- Bawić się jako oba.
Przykładami tych interakcji z metanolem wyniosłyby: H3N+-H - Ohch3 i ho- - Hoch3 (Ohch3 Wskazuje, że tlen odbiera mostek wodorowy, a nie, że grupa metylowa jest powiązana z H).
Ryzyko
- W kontakcie z oczami powoduje podrażnienie, które może prowadzić do uszkodzenia oka.
- To jest żrące. Dlatego w kontakcie ze skórą może powodować podrażnienie, a przy dużych stężeniach odczynnika powoduje oparzenia skóry. Powtarzający się kontakt wodorotlenku amonu ze skórą może powodować jego suchość, swędzenie i zaczerwienienie (zapalenie skóry).
- Wdychanie rosy wodorotlenku amonu może powodować ostre podrażnienie dróg oddechowych, charakteryzujące się uduszeniem, kaszlem lub brakiem powietrza.
- Przedłużone lub powtarzające się narażenie substancji może powodować powtarzające się infekcje oskrzela. Podobnie, inhalacja wodorotlenku amonu może powodować podrażnienie płuc.
Może ci służyć: wodorotlenek strontu (SR (OH) ₂)- Ekspozycja na wysokie stężenie wodorotlenku amonu może stanowić awarię medyczną, ponieważ akumulacja płynu może wystąpić w płucach (obrzęk płuc).
- Stężenie 25 ppm zostało przyjęte jako limit ekspozycji, w 8 -godzinnej zmianie pracy, w środowisku, w którym pracownik jest narażony na szkodliwe działanie wodorotlenku amonu.
Reaktywność
Oprócz potencjalnych szkód zdrowotnych z powodu narażenia na wodorotlenek amonu, istnieją inna opieka, którą należy wziąć pod uwagę podczas pracy z substancją.
- Wodorotlenek amonu może reagować z wieloma metali, takimi jak: srebro, miedź, ołów i cynk. Reaguje również z solami tych metali, tworząc związki wybuchowe i uwalniają gaz wodorowy, który z kolei jest łatwopalny i wybuchowy.
- Może reagować gwałtownie z silnymi kwasami, na przykład: kwas solny, kwas siarkowy i kwas azotowy. Reaguje również w ten sam sposób z dimetylistkowatym i halogenami.
- Reaguje z silnymi zasadami, takimi jak wodorotlenek sodu i wodorotlenek potasu, wytwarzający gazowy amoniak. Można to zweryfikować, czy obserwuje się równowagę w roztworze, w którym dodanie jonów OH- wypiera równowagę do tworzenia NH3.
- Nie należy stosować metali miedzi i aluminiowych, a także innych metali ocynkowanych, gdy manipulowany jest wodorotlenek amonu, ze względu na jego żrące działanie.
Aplikacje
W jedzeniu
- Jest używany jako addytywny w wielu produktach spożywczych, w którym spełnia funkcje środka opaleniającego, kontrola pH i środka wykończenia powierzchni żywności.
- Lista żywności, w której stosuje się wodorotlenek amonu, jest obszerna i zawiera pieczone produkty, sery, czekoladki, cukierki i pudiny.
- Wodorotlenek amonu jest katalogowany jako niewinna substancja przez FDA do przetwarzania żywności, pod warunkiem, że przestrzegane są normalne normy.
- W produktach mięsnych jest stosowany jako środek przeciwdrobnoustrojowy, będąc w stanie wyeliminować bakterie, takie jak I. coli, Zmniejszenie go do niewykrywalnych poziomów. Bakteria znajduje się w jelicie bydła, dostosowując się do kwaśnego środowiska. Wodorotlenek amonu, podczas regulacji pH, utrudnia wzrost bakterii.
Lecznictwo
Wśród wodorotlenku amonu ma kilka zastosowań terapeutycznych, wśród nich:
- Roztwór 10% jest stosowany jako stymulant odruchu oddechowego.
Może ci służyć: alfa-Zotoglutarate: Właściwości, funkcje i aplikacje- Zewnętrznie jest stosowany na skórze do leczenia ukąszeń owadów i ukąszeń.
- Działa w układzie trawiennym jako zobojętniby się i farmoniczne, to znaczy pomaga wyeliminować gaz.
- Jest używany jako guma miejscowa. W wyniku tego działania występuje lokalny wzrost przepływu krwi, zaczerwienienia i podrażnienia.
Przemysłowe i różne
- Działa w zmniejszeniu NOX (bardzo reaktywne gazo, takie jak tlenek azotu (NO) i dwutlenek azotu2)) W przypadku emisji baterii i redukcji NOx w emisji komina.
- Jest stosowany jako środek plastylizujący, dodatek obrazów i do obróbki powierzchni.
- Porowatość włosów wzrasta, pozwalając na większą penetrację barwników, co osiąga lepsze wykończenie.
- Wodorotlenek amonu jest stosowany jako środek przeciwdrobnoustrojowy w oczyszczaniu ścieków. Ponadto interweniuje w syntezie chloraminy. Ta substancja wypełnia funkcję chloru w oczyszczeniu wody basenowej, mając przewagę, że jest mniej toksyczna.
- Jest stosowany jako inhibitor korozji w procesie rafinacji oleju.
- Jest stosowany jako środek czyszczący w różnych produktach przemysłowych i komercyjnych, stosowany na kilku powierzchniach, w tym ze stali nierdzewnej, porcelanie, szkła i pieca.
- Jest stosowany w produkcji detergentów, mydeł, produktów farmaceutycznych i atramentów.
W rolnictwie
- Chociaż nie podawane bezpośrednio jako nawóz, wodorotlenek amonu wypełnia tę funkcję. Amoniak występuje z atmosferycznego azotu metodą posiadania-boscha i jest transportowany w lodówce poniżej jego temperatury wrzenia (-33 ºC) do miejsc jego użycia.
- Wtryskiwane jest amoniak pod ciśnieniem, w postaci pary, wewnątrz gleby, gdzie natychmiast reaguje z edyficzną wodą i przechodzi do postaci amonu (NH4+), który jest zatrzymywany w miejscach wymiany w klasie gleby. Ponadto występuje wodorotlenek amonu. Te związki są źródłem azotu.
- Wraz z fosforem i potasem azot stanowi główną triadę składników odżywczych podstawowych roślin dla ich wzrostu.
Bibliografia
- Helmestine, Anne Marie, pH.D. Fakty wodorotlenku amonu. Wyzdrowiał z Thoughco.com
- Arkusz informacyjny na temat substancji niebezpiecznych: wodorotlenek amonu [PDF]. Odzyskane z NJ.Gov
- Wodorotlenek amonu. Odzyskany z chemistrylearnera.com

