Formuła molekularna, jak to wydostać, przykłady i ćwiczenia
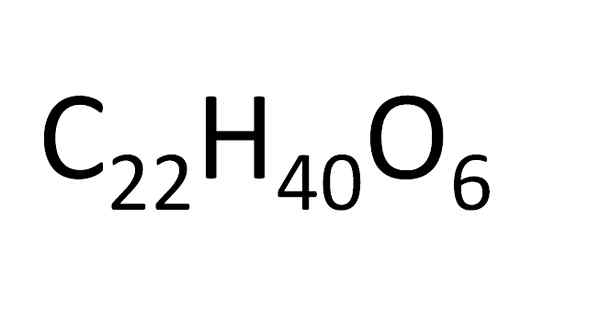
- 3898
- 936
- Maksymilian Kępa
formuła molekularna Jest to reprezentacja cząsteczki związku, w której są one wskazane, poprzez jego symbole chemiczne, atomy wszystkich elementów obecnych w związku i ich liczby. Każdemu atomowi towarzyszy indeks dolny.
Wzór molekularny ma ograniczenie, które nie wskazuje na powiązania różnych atomów cząsteczki lub ich związku przestrzennego; jak wyrażone przez formułę strukturalną. W niektórych przypadkach nie jest to konkretne, na przykład: C6H12ALBO6 Jest to wzór molekularny glukozy, galaktozy i fruktozy.
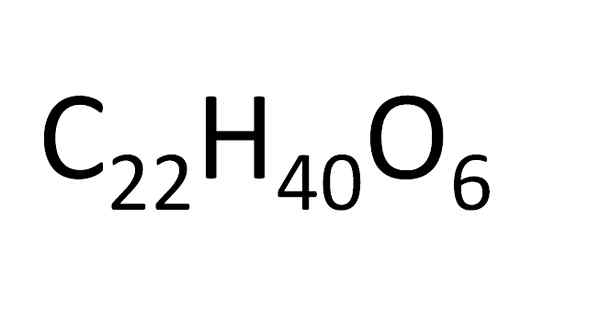 Z tego samego wzoru molekularnego można uzyskać niekończące się związki izomeryczne. Odpowiada to organicznej zmiennej masy wysokiej cząsteczkowej. Źródło: Gabriel Bolívar.
Z tego samego wzoru molekularnego można uzyskać niekończące się związki izomeryczne. Odpowiada to organicznej zmiennej masy wysokiej cząsteczkowej. Źródło: Gabriel Bolívar. Istnieje zestaw zasad dotyczących usuwania atomów w wzorze molekularnym. W przypadku soli jonowych, na przykład chlorku sodu, najpierw umieszczany jest symbol kationów (na+), a następnie symbol anionu (CL-). Właśnie dlatego wzorem molekularnym chlorku sodu jest NaCl.
Molekularny wzór związków organicznych jest zapisywany przez najpierw umieszczanie symbolu węgla (C), a następnie symbol wodoru (H), a następnie pozostałe atomy. Na przykład wzór molekularny kwasu octowego wynosi C2H4ALBO2.
[TOC]
Jak uzyskać wzór molekularny
Uzyskanie wzoru molekularnego związku opiera się na poprzednim ustaleniu minimalnego lub empirycznego wzoru tego samego. Z tego powodu początkowe kroki w uzyskiwaniu obu formuł są powszechne.
Pierwszy krok
Ekspresja masy pierwiastków związku chemicznego w postaci procentowej jest zwykle. Następnie należy przeprowadzić proste obliczenia w celu przekształcenia masowych odsetek różnych elementów w ich masy wyrażone w gramach.
Może ci służyć: stężenie procentoweDrugi krok
Znając masę w gramie każdego z elementów i jej masę atomową, możesz uzyskać względną liczbę każdego atomu lub liczbę moli każdego atomu dzielącego masę każdego z różnych elementów między jego masą atomową.
Trzeci krok
Względna liczba Wszystko atomy, między względną liczbą niższej wartości. Minimalne wartości proporcji muszą być liczbą całkowitą. W przypadku, gdy wartość proporcji zawiera dziesiętne, należy dokonać korekty, która sprawia, że tak dziesięczne zniknęły.
Korekta polega na pomnożeniu wszystkich wartości proporcji przez liczbę, która zwraca się do wszystkich wartości. Na przykład, jeśli minimalna wartość proporcji wynosi 1.25, wszystkie wartości muszą być pomnożone przez cztery (4). Od 1.25 pomnożone przez 4 jest równe 5, liczba całkowita.
Czwarty krok
Wszystkie symbole chemiczne pierwiastków związku zostaną umieszczone i wraz z odpowiadającym indeksem dolnym; to znaczy wartość minimalnego odsetka elementu.
Piąty krok
Minimalny wzór związku można przekształcić w jego wzór cząsteczkowy poprzez uzyskanie związku między masą cząsteczkową związku a masą jego minimalnego wzoru (N). Związek ten jest taki sam, jak istnieje między wzorem molekularnym a wzorem minimalnym.
n = masa cząsteczkowa związku / masy minimalnego wzoru
Aby uzyskać wzór molekularny, minimalny wzór należy pomnożyć przez n. Oznacza to, że każdy z indeksu dolnej formuły minimalnej należy pomnożyć przez n.
n = masa cząsteczkowa / minimalna masa wzoru
= Wzór molekularny / wzór minimalny
Może ci służyć: tlen: właściwości, struktura, ryzyko, użyciaWzór molekularny = n · Minimalny wzór
Przykłady wzorów molekularnych
Poniżej znajdują się niektóre typowe wzory molekularne:
-Tlenek żelaza (brzydki)
-Wodorotlenek sodu (NaOH)
-Tlenek potasu (k2ALBO)
-Tlenek nadchlorowy (CL2ALBO7)
-Wodorotlenek żelazowy [wiara (OH)3]
-Chlorek wapnia (CACL2)
-Kwas chlorowy (HCL)
-Siarczan sodu (n2południowy zachód4)
-Kwas siarkowy (h2południowy zachód4)
-Kwas okołowy (HBRO4)
-Chlorek aluminiowy (ALCL3)
-Metan (rozdz4)
-Propan (c3H8)
-Etano (c2H6)
-Alkohol etylowy (c2H6ALBO)
-Kwas octowy (c2H4ALBO2)
-Benzen (c6H6)
-Glukoza (c6H12ALBO6)
Rozwiązane ćwiczenia
- Ćwiczenie 1
Benzoesan metalu ma następujące masowe odsetki:
C: 70,57 %,
H: 5,93 %
O: 23,49 %
Oraz masę cząsteczkową 136,1 g/mol. Określić wzór molekularny.
Pierwszy krok
Pierwszym krokiem jest wyrażanie masowych odsetek pierwiastków w ich masach w gramach, wiedząc, że wartości procentowe są w stosunku do masy cząsteczkowej.
Spośród 136,1 gramów odpowiadających molowi związku 70,57% reprezentuje tylko węgiel. I tak dalej z pozostałymi elementami:
Masa węglowa = 136,1 g · (70,57/100)
= 96,05 g
Masa wodoru = 136,1 g · (5,93/100)
= 8,06 g
Masa tlenu = 136,1 · (23,49/100)
= 31,96 g
Drugi krok
W opracowaniu wzoru molekularnego należy określić względną liczbę atomów (NRA). Aby to zrobić, masy pierwiastków są podzielone między ich mas atomowe:
NRA (c) = 96 g / 12 g
= 8
NRA (H) = 8 g / 1 g
= 8 g
NRA (o) = 32 g / 16 g
= 2
Trzeci krok
Następnie musimy obliczyć minimalne proporcje elementów (PME). W tym celu wszystkie wartości NRA są podzielone między wartość mniejszej NRA:
PME (c) = 8/2
= 4
PME (H) = 8/2
= 4
Pme (o) = 2/2
= 1
Czwarty krok
Napisz minimalną formułę benzoesanu metylowego, w oparciu o fakt, że indeksy indeksyjne elementów są ich minimalnymi proporcjami obliczonymi:
Może ci służyć: dichromian sodu (Na2CR2O7): właściwości, produkcja, zastosowaniaC4H4ALBO
Piąty krok
Wreszcie należy ustalić wzór molekularny benzoesanu metylu. Obliczamy wtedy:
n = masa cząsteczkowa / minimalna masa wzoru
Minimalna masa wzoru wynosi 68 g/mol:
= 136,1 g / 68 g
n ≈ 2
Wzór molekularny = 2 · Minimalny wzór
= 2 · C4H4ALBO
Wzór molekularny benzoesanu metylu = C8H8ALBO2
- Ćwiczenie 2
Procent elementów, które tworzą benzen, są następujące:
C: 92,36 %
H: 7,64 %.
Masa cząsteczkowa benzenu wynosi 78 g/mol. Określ jego wzór molekularny.
Pierwszy krok
Przekształć masowe odsetki pierwiastków w ich masę w gram:
Masa węglowa = 78 g · (92,36/100)
= 72,04 g
Masa wodoru = 78 g · (7,64/100)
= 5,96 g
Drugi krok
Obliczenie względnej liczby atomów (NRA). Aby to zrobić, masy pierwiastków są podzielone między ich mas atomowe:
NRA (c) = 72 g / 12 g
= 6
NRA (H) = 6 g / 1 g
= 6
Trzeci krok
Obliczenie wartości minimalnego odsetka elementów (PME). Jest to obliczane przez podzielenie wartości NRA wszystkich elementów między niższą wartością NRA:
PME (c) = 6/6
= 1
PME (H) = 6/6
= 1
Czwarty krok
Czyn minimalnego wzoru benzenowego, biorąc pod uwagę, że indeksywach elementów są wartościami minimalnej obliczonej proporcji.
Minimalna formuła benzenu: Ch
Piąty krok
Ustanowienie wzoru cząsteczkowego poprzez obliczenie związku między masą cząsteczkową a masą minimalnego wzoru:
n = masa cząsteczkowa / minimalna masa wzoru
= 78 g / 13 g
n = 6
Wzór molekularny = n · Minimalny wzór
= 6 · ch
= C6H6
Bibliografia
- Whitten, Davis, Peck i Stanley. (2008). Chemia. (8 wyd.). Cengage Learning.
- Wikipedia. (2020). Wzór chemiczny. Źródło: w:.Wikipedia.org
- Bezgraniczna nauka. (S.F.). Formuły molekularne. Odzyskane z: kursów.Lumenarning.com
- Helmestine, Anne Marie, pH.D. (29 września 2019). Formuły obliczeń empirycznych i molekularnych. Odzyskane z: Thoughtco.com
- Peter J. Mikulecky, Chris Hren. (2020). Jak używać formuł empirycznych do znalezienia wzorów molekularnych. Odzyskane z: manekinów.com
- « Minimalna formuła, jak usunąć minimalną formułę, przykłady i ćwiczenia
- Historia globalizacji, cechy, przyczyny, konsekwencje »

