Struktura aluminiowa fosfuro (AIP), właściwości, zastosowania, ryzyko

- 687
- 174
- Eugenia Czapla
On Fosfor glinowy Jest to związek nieorganiczny utworzony przez atom aluminiowy (AL) i atom fosforu (P). Jego wzór chemiczny ALP. Jest ciemnoszare stałe lub, jeśli jest bardzo czysty, żółty. Jest to wyjątkowo toksyczny związek dla żywych istot.
Aluminiowy fosfuro reaguje z wilgocią, tworząc fosfinę lub fosfano pH3, który jest trującym gazem. Z tego powodu ALP nie powinien kontaktować się z wodą. Silnie reaguje z kwasami i roztworami alkalicznymi.
 Fosfor glinowy. همان [gfdl (http: // www.gnu antylopa.Org/copyleft/fdl.html)]. Źródło: Wikimedia Commons.
Fosfor glinowy. همان [gfdl (http: // www.gnu antylopa.Org/copyleft/fdl.html)]. Źródło: Wikimedia Commons. W przeszłości był używany do wyeliminowania szkodników, takich jak owady i gryzonie w miejscach, w których przechowywano ziarna zbóż i inne produkty rolne. Jednak ze względu na wysokie niebezpieczeństwo zostało zabronione w większości krajów na świecie.
Obecnie jego przydatność w obszarze elektroniki jest teoretycznie badana za pomocą komputerów, które obliczają możliwość uzyskania półprzewodnikowych nanorurek ALP, to znaczy wyjątkowo małych rur, które mogą przenosić energię elektryczną tylko w określonych warunkach.
Aluminiowy fosfuro jest bardzo niebezpiecznym związkiem, należy go manipulować za pomocą narzędzi bezpieczeństwa, takich jak rękawiczki, soczewki, sprzęt oddychający i odzież ochronna.
[TOC]
Struktura
ALP Aluminiowy fosfuro powstaje przez połączenie atomu aluminiowego w fosforowym atomie p. Związek między nimi jest kowalencyjny i potrójny, dlatego jest bardzo silny.
Aluminium w ALP ma stan utleniania +3, a fosfor ma wartościowość -3.
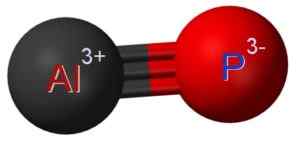 Aluminiowa struktura fosfuro, w której można zobaczyć potrójne połączenie między atomami aluminium (AL) i fosforu (P) (P). Claudio Pistilli [CC BY-SA (https: // creativeCommons.Org/licencje/nabrzeże/4.0)]. Źródło: Wikimedia Commons.
Aluminiowa struktura fosfuro, w której można zobaczyć potrójne połączenie między atomami aluminium (AL) i fosforu (P) (P). Claudio Pistilli [CC BY-SA (https: // creativeCommons.Org/licencje/nabrzeże/4.0)]. Źródło: Wikimedia Commons. Nomenklatura
- Fosfor glinowy
Nieruchomości
Stan fizyczny
Ciemnoszare krystaliczne stałe lub ciemnożółte. Kryształy sześcienne.
Waga molekularna
57 9553 g/mol
Temperatura topnienia
2550 ° C
Gęstość
2,40 g/cm3 w 25 ° C
Rozpuszczalność
Rozkłada się w wodzie.
Właściwości chemiczne
Reaguje z wilgocią, aby uzyskać fosfinę lub fosfano pH3 który jest łatwopalnym i trującym związkiem. Fosfina lub fosfaan.
Może ci służyć: gadolinio: struktura, właściwości, uzyskiwanie, użyciaAluminiowa reakcja fosfuro z wodą jest następująca:
Aluminium fosfuro + woda → wodorotlenek glinu + fosfina
ALP + 3 H2O → do (OH)3 + Ph3↑
Prezentacje komercyjne mają węglan aluminiowy do2(WSPÓŁ3)3 Aby zapobiec samowystarczalności fosfiny, która występuje, gdy ALP wchodzi w kontakt z wilgocią powietrza.
ALP jest stabilny, gdy jest suchy. Reaguje gwałtownie kwasami i roztworami alkalicznymi.
ALP Aluminiowy fosfuro nie topi się, ani podprogowy ani rozkłada się termicznie w temperaturach tak wysokich jak 1000 ° C. Nawet w tej temperaturze jego ciśnienie pary jest bardzo niskie, to znaczy nie odparowuje w tej temperaturze.
Po podgrzaniu do jego rozkładu emituje toksyczne tlenki fosforu. W kontakcie z metalami możesz emitować łatwopalne gazy wodorowe h2.
Inne właściwości
Kiedy jest czyste, pokazuje żółtawe zabarwienie, gdy jest zmieszane z resztkami reakcji przygotowawczej, przedstawia kolor od szarego do czarnego.
Jego niska zmienność wyklucza, że ma zapach, więc zapach czosnku, który czasami emituje się, wynika z fosfiny3 To powstaje w obecności wilgoci.
Uzyskanie
Aluminiowy fosfuro można uzyskać przez ogrzewanie mieszaniny proszku metalowego aluminium (AL) i czerwonego elementu fosforu (P).
Z powodu powinowactwa fosforu (p) przez tlen (lub2) i aluminium (AL) przez tlen i azot (n2), Reakcję należy przeprowadzić w wolnej atmosferze tych gazów, takich jak atmosfera wodoru (h2) lub gaz ziemny.
Reakcja zaczyna się szybko ogrzewać powierzchnię mieszaniny, aż rozpocznie się reakcja, która jest egzotermiczna (ciepło występuje w tym samym). Od tego momentu reakcja przebiega szybko.
Aluminium + fosfor → fosfuro glinu
4 do + P4 → 4 ALP
Aplikacje
W eliminacji szkodników (wycofane użycie)
Aluminiowy fosfuro stosowano w przeszłości jako środek owadobójczy i jako eksterminator gryzoni. Chociaż jest to zabronione przez jego toksyczność, jest nadal używany w niektórych częściach świata.
Może ci służyć: .Kwas stearynowy (CH3 (CH2) 16cooh): Struktura, właściwości, zastosowaniaSłuży do fumigacji w zamkniętych przestrzeniach, w których znajdują się przetworzone lub nieprzetworzone produkty żywności.
Celem jest kontrolowanie owadów i gryzoni, które atakują przechowywane artykuły, czy to jadalne, czy nie.
Umożliwia kontrolowanie gryzoni i owadów na obszarach niedomestowych, rolniczych lub pozbawionych fragmentów, fumigując na zewnątrz lub w norach i gniazdach, aby zapobiec transmisji niektórych chorób.
 Szczury i myszy to szkodniki, które atakują miejsca do przechowywania płatków zbożowych. Kilka lat temu walczyli z aluminiowym fosfuro. Autor: Andreas n. Źródło: Pixabay.
Szczury i myszy to szkodniki, które atakują miejsca do przechowywania płatków zbożowych. Kilka lat temu walczyli z aluminiowym fosfuro. Autor: Andreas n. Źródło: Pixabay.  Gryzonie kontrolowano przez umieszczenie aluminiowego fosfuro w norach. Autor: foto-rabe. Źródło: Pixabay.
Gryzonie kontrolowano przez umieszczenie aluminiowego fosfuro w norach. Autor: foto-rabe. Źródło: Pixabay. Jego forma użycia polega na ekspozycji ALP w powietrzu lub wilgoci, ponieważ pH fosfiny lub fosfaki jest uwalniane3 który generuje uszkodzenie wielu narządów zarazy, aby wyeliminować.
 Owady zostały również wyeliminowane za pomocą fosfuro ALP aluminium. Autor: Michael Power. Źródło: Unspash.
Owady zostały również wyeliminowane za pomocą fosfuro ALP aluminium. Autor: Michael Power. Źródło: Unspash. W innych aplikacjach
ALP Aluminiowy fosfuro jest stosowany jako źródło fosfiny lub fosfano pH3 i jest stosowany w badaniach półprzewodników.
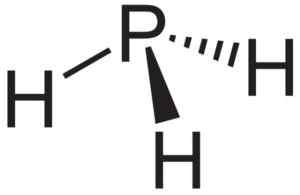 Fosfaano lub fosfina pH3, związek, który tworzy się, gdy ALP aluminiowy fosfuro wchodzi w kontakt z wodą. Neuropeker [domena publiczna]. Źródło: Wikimedia Commons.
Fosfaano lub fosfina pH3, związek, który tworzy się, gdy ALP aluminiowy fosfuro wchodzi w kontakt z wodą. Neuropeker [domena publiczna]. Źródło: Wikimedia Commons. Teoretyczne badania nanorurek ALP
Badania teoretyczne przeprowadzono w tworzeniu nanorurek fosfuro ALP. Nanorurki są bardzo małe i bardzo cienkie cylindry, które mogą być widoczne tylko za pomocą mikroskopu elektronicznego.
Nanorurki ALP z borami
Badania teoretyczne przeprowadzone poprzez obliczenia obliczeniowe pokazują, że zanieczyszczenia, które można dodać do nanorurek ALP, mogą zmienić teoretyczne właściwości tych.
Na przykład szacuje się, że dodanie atomów boru (B) do nanorurek ALP może zamienić je w półprzewodniki typu-P. Półprzewodnik to materiał, który zachowuje się jak przewodnik elektryczny lub jako izolacja w zależności od pola elektrycznego, na które jest poddawany.
Może ci służyć: stan plazmowy: cechy, typy i przykładyI półprzewodnik typu-P To wtedy, gdy materiał jest dodawany do zanieczyszczeń, w tym przypadku ALP jest materiałem początkowym, a atomy boru byłyby zanieczyszczenia. Półprzewodniki są przydatne w aplikacjach elektronicznych.
Nanorurki ALP o zmienionej strukturze
Niektórzy naukowcy przeprowadzili obliczenia w celu określenia wpływu struktury sieci krystalicznej nanorurek ALP z sześciokątnej na oktaedry.
Odkryli, że manipulacja strukturą sieci krystalicznej można zastosować do dostosowania przewodności i reaktywności nanorurek ALP i zaprojektowania ich, aby były przydatne do zastosowań elektronicznych i optycznych.
Ryzyko
Kontakt z aluminiowym fosfuro może podrażniać skórę, oczy i błony śluzowe. Jeśli jest połknięty lub wdychany, jest toksyczny. Może być wchłaniany przez skórę z toksycznymi efektami.
Jeśli ALP kontaktuje się z wodą reaguje i fosfiną lub fosfanowe pH3 co jest wyjątkowo łatwopalne, ponieważ spala się w kontakcie z powietrzem. Dlatego może wykorzystać. Ponadto fosfina powoduje śmierć ludzi i zwierząt.
Ponieważ ekonomiczny pestycyd jest fosfuro aluminium, jego stosowanie jest powszechną przyczyną zatrucia ludzi i pociąga za sobą wysoką śmiertelność.
 Aluminiowy fosfuro jest niezwykle niebezpieczny. Autor: OpencLipart-Vectors. Źródło: Pixabay.
Aluminiowy fosfuro jest niezwykle niebezpieczny. Autor: OpencLipart-Vectors. Źródło: Pixabay. Reaguje z wilgocią błon śluzowych i kwasem hydrochlorowym HCL żołądka tworzącym bardzo toksyczny pH fosfanowy3. Dlatego przez inhalację i spożycie fosfina powstaje w ciele, z śmiertelnymi efektami.
Jego spożycie powoduje krwotok przewodu pokarmowego, załamanie sercowo -naczyniowe, zaburzenia neuropsychiatryczne, niewydolność oddechowa i nerki w ciągu kilku godzin.
ALP jest bardzo toksyczny dla wszystkich zwierząt naziemnych i wodnych.
Bibliografia
- LUB.S. National Library of Medicine. (2019). Aluminium fosforowe. Odzyskane z Pubchem.NCBI.NLM.Nih.Gov.
- Sjögren, ur. i in. (2007). Aluminium. Inne związki aluminiowe. W Handbook on the Toxicology of Metals (wydanie trzecie). Odzyskane z naukowym.com.
- Gupta, r.C. i Crissman, J.W. (2013). Ocena bezpieczeństwa, w tym obecne i pojawiające się problemy w patologii toksykologicznej. Ryzyko ludzkie. W Haschek i Rousseaux's Handbook of Toxicology Pathology (wydanie trzecie). Odzyskane z naukowym.com.
- White, w.I. i Bushey, żeby.H. (1944). Aluminiowy fhosfid - przygotowanie i skład. Journal of the American Chemical Society 1944, 66, 10, 1666-1672. Odzyskane z pubów.ACS.org.
- Mirzaei, Maryam i Mirzaei, Mahmoud. (2011). Teoretyczne badanie nanorurek z glinu boru aluminium. Chemia obliczeniowa i teoretyczna 963 (2011) 294-297. Odzyskane z naukowym.com.
- Takahashi, l. I Takahashi, K. (2018). Dostrajanie elektronicznej struktury aluminiowej nanorurki fosfinowej. ACS Appl. Nano Mater. 2018, 1, 501-504. Odzyskane z pubów.ACS.org.
- Gupta, s. 1.K. (2016). Toksyczne działanie pesobójców (agrochemikalia). Aluminium fosforowe. W funduszach toksykologii. Odzyskane z naukowym.com.
- « Prostokątne współrzędne przykłady i ćwiczenia rozwiązane
- Stopień wielomianowego sposobu, w jaki jest określony, przykłady i ćwiczenia »

