Elementy, związki i mieszanki
- 3250
- 303
- Matylda Duda
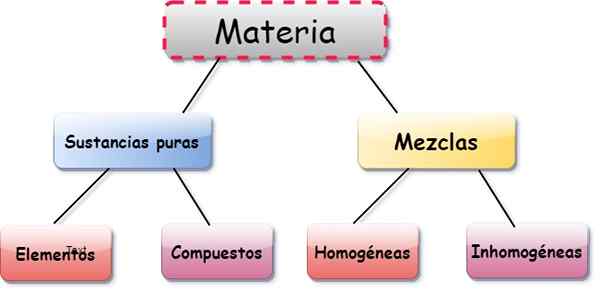
Elementy, związki i mieszanki to trzy formy prezentacji materii. rzeczy Są substancjami utworzonymi przez jedną klasę atomu, Związki Są to kombinacje między dwoma lub więcej elementami, i mieszanki Wynikają z składu kilku elementów i substancji.
Składniki mieszanin są oddzielone za pomocą środków fizycznych. Aby oddzielić pierwiastki związku, należy przeprowadzić procedury chemiczne.
Nie ma sposobu, aby podzielić je na drobne komponenty zwykłymi metodami, ale istnieją sposoby na szczelinowanie atomów. W rzeczywistości rozszczepienie jest sposobem na wydobycie z nich energii.
Atomy, które tworzą określony związek, zawsze robią to w ustalonych proporcjach. Ze swojej strony, w mieszance proporcje jego składników mogą się różnić. Dlatego elementy i związki są uważane za czyste substancje, których skład jest stały i dobrze zdefiniowany.
Na przykład sól stołowa lub chlorek sodu to związek, w którym uczestniczą atomy chloru i sodu. Tymczasem mleko jest mieszanką zmiennej składu, w której każdy składnik utrzymuje swoją tożsamość.
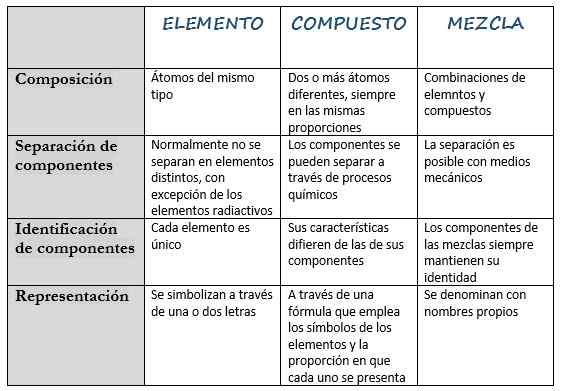
Poniższa tabela zbiera się jej głównych cech:
Element | Mieszanina | Mieszać | |
Definicja | Substancję, której nie można rozłożyć w innych prostszych substancjach. | Substancja utworzona przez dwa lub więcej różnych elementów. | Substancja wykonana podczas mieszania innych substancji. |
Kompozycja | Atomy tego samego typu. | Dwa lub więcej różnych atomów, zawsze w tych samych proporcjach. | Kombinacje pierwiastków i związków. |
Separacja komponentów | Zwykle nie oddzielają one na różne elementy, z wyjątkiem elementów radioaktywnych. | Komponenty można oddzielić poprzez procesy chemiczne. | Separacja jest możliwa ze środkami mechanicznymi. |
Identyfikacja komponentów | Każdy element jest wyjątkowy. | Jego cechy różnią się od cech jego komponentów. | Składniki mieszanin zawsze zachowują swoją tożsamość. |
Reprezentacja | Są one symbolizowane w jednej lub dwóch literach. | Poprzez formułę wykorzystującą symbole elementów i proporcji, w którym każdy jest prezentowany. | Jest wywoływany z nazwami. |
Przykłady | Wodór (H), krzem (tak), hel (HE), złoto (au), potas (k). | Chlorek sodu (NaCl), amoniak (NH3), wodorek sodu (NaH), dwutlenek azotu (NO2). | Krew, mleko, powietrze, cement. |
Rzeczy
Definicja
Elementy są czystymi, prostymi substancjami, w których składu tylko atomy tego samego typu interweniują. Zachowanie chemiczne każdego elementu jest charakterystyczne i nie ma dwóch równych, chociaż istnieją wspólne cechy między grupami pierwiastków.
Może ci służyć: jodometria: fundamenty, reakcje, procedura ogólna,Nie można rozłożyć jednego elementu w prostszym, z wyjątkiem specjalnych procedur, takich jak Bombard.
Proces rozpadu występuje spontanicznie w niektórych substancjach, takich jak radio, niektóre odmiany uranu, toru i inne elementy zwane radioaktywnymi.
Kompozycja
Elementy są tworzone przez identyczne atomy. Z kolei składają się z trzech rodzajów cząstek: elektronów, protonów i neutronów. Elektrony i protony mają odpowiednio masę elektryczną, ujemną i dodatnią. Neutrony mają masę, ale nie ładować.
Atom składa się z jądra atomowego utworzonego przez protony i neutrony, podczas gdy elektrony są rozmieszczone w otaczających ich orbitale. Jeden element odróżnia się od drugiego liczbą protonów, które ma jego jądro, zwane liczbą atomową.
Chociaż pozostaje to stałe, jest to ten sam element, nawet jeśli zmienia się liczba neutronów i elektronów, ponieważ w takim przypadku izotopy.
Identyfikacja komponentów
Na przykład stosuje się różne i złożone techniki, aby „zobaczyć” elektrony atomu.
Technika separacji
Atom pierwiastka nie jest rozdzielony metodami chemicznymi, ale jest bombardowany mniejszymi cząsteczkami, zwykle neutronami, w procesie zwanym rozszczepieniem jądrowym. Ale chociaż teoretycznie każdy atom jest fizycznie, łatwiej jest to zrobić z atomami, które mają ciężkie jądra, takie jak uran-235.
Rodzaje elementów
Istnieje 118 elementów, zlokalizowanych w tabeli okresowej, zamówione według liczby atomowej. Spośród nich 92 występuje w naturze, a pozostałe są uzyskiwane w laboratorium.
Może ci służyć: amorficzny węgiel: co to jest, typy, właściwości, użyciaSą dystrybuowane w trzech grupach:
- Metale, z wolnymi elektronami, które czynią je dobrymi przewodami ciepła i energii elektrycznej, prawie zawsze solidne (z wyjątkiem rtęci) i wysoką gęstością.
- Żadne metale, brak właściwości postępowania, nie są prezentowane w stanie stałych lub gazowych, z wyjątkiem bromu, a ich gęstość jest niższa.
- Metaloidy, elementy o cechach pośrednie.
Reprezentacja graficzna
Każdy element tabeli okresowej jest symbolizowany literami. Na przykład H, O, C i Fe odpowiadają odpowiednio wodorze, tlenu, węgla i żelaza.
Przykłady elementów
Oprócz wspomnianych istnieją następujące elementy, z ich symbolem w nawiasach:
- Chlor (CL)
- Merkury (HG)
- Fosfor (P)
- Jod (i)
- Magnez (mg)
Związki
Definicja
Związki to czyste substancje, których skład dwa lub więcej rodzajów różnych atomów jest zaangażowanych, w pewnych proporcjach, tworząc cząsteczki. Związki między atomami są przeprowadzane przez łącza, które są czynnikiem decydującym w właściwościach złożonych.
Główne linki to:
- joński
- Metal
- Kowalencyjny
Kompozycja
Związki składają się z dwóch lub więcej rodzajów atomów, zawsze w ustalonym proporcji.
Identyfikacja komponentów
Każdy związek ma właściwości, które czynią go wyjątkowym, które różnią się od właściwości elementów składowych, ponieważ tracą swoją tożsamość, tworząc związek. Na przykład w temperaturze w temperaturze pokojowej i tlenu są gazy, które po połączeniu powodują powstanie wody.
Technika separacji
Zwykle związki są oddzielone reakcjami chemicznymi, chociaż promieniowanie elektromagnetyczne, w tym światło, jest również w stanie dysocjować cząsteczki.
Rodzaje związków
Związki są podzielone na dwie główne kategorie:
- Nieorganiczny
- Organiczny
Różnica polega na tym, że związki organiczne opierają się na elemencie węglowym, gdy tworzy on powiązania typu kowalencyjnego z wodorem. Węgiel uczestniczy w ten sam sposób w wielu związkach nieorganicznych, tworząc inne linki.
Reprezentacja graficzna
Odbywa się to poprzez formułę chemiczną, w której określane są jego składniki, z ich odpowiednim symbolem i proporcją, w której uczestniczą. Związki mają również różne nazwy.
Przykłady związków
- Chlorek sodu lub sól stołowa (NaCl)
- Wodorowęglan sodu (Nahco₃)
- Amoniak (NH3)
- Węglan wapnia (caco3)
- Glukoza (c₆h₁₂o₆)
Mieszanki
Definicja
Połączenie dwóch lub więcej elementów i/lub związków, bez określonych proporcji, z których każdy utrzymuje swoją tożsamość, to znaczy bez zmiany ich właściwości, gdy są częścią mieszanki.
Kompozycja
Jest zmienna.
Identyfikacja komponentów
Jest prostsze do przeprowadzania, ponieważ komponenty utrzymują swoją tożsamość.
Technika separacji
Składniki mieszaniny można oddzielić jakąś metodą fizyczną lub mechaniczną, taką jak filtrowanie lub wirowanie, na przykład.
Rodzaje mieszanin
Mieszanki są klasyfikowane jako:
- Homogeniczne: cząstki składowe są nie do odróżnienia, mimo że mają różne substancje. Na przykład bardzo rozpuszczony cukier w wodzie.
- Heterogeniczne: mieszanki, w których cząsteczki są wyróżniające się, nawet gołym okiem, takim jak piasek i sól lub sól zmieszana z metalowymi plikami.
Reprezentacja graficzna
Mieszaninom brakuje określonej formuły, ale wiele ma własne nazwiska.
Przykłady mieszanin
- Cement
- Keczup
- Drewno
- Powietrze
- mleko
- Beton
- Krew

