Podzielność chemiczna
- 1448
- 256
- Paweł Malinowski
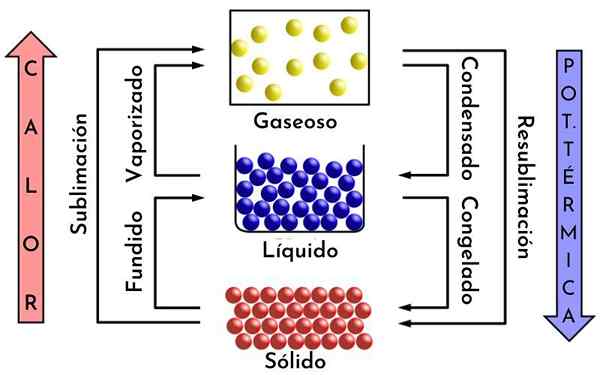
 Transformacja materii, przykład podzielności w chemię. Źródło: Mikerun, CC BY-SA 4.0, Wikimedia Commons
Transformacja materii, przykład podzielności w chemię. Źródło: Mikerun, CC BY-SA 4.0, Wikimedia Commons Jaka jest podzielność chemiczna?
Możemy zdefiniować Podzielność chemiczna jako właściwość materii, która pozwala oddzielić się w mniejszych porcjach. Aby zrozumieć koncepcję, możemy podać przykład.
Jeśli kostka lodu zostanie stopiona, staje się woda, a gdy jest poddawany ciepło, jest przekształcana w parę. Ta para można z kolei podzielić w cząsteczki, a te, w atomy.
Podzielność chemiczna jest zatem możliwością podziału na coraz małe części.
Pochodzenie i koncepcja podziału chemicznego
Przez długi czas omawiano, czy sprawa składała się z cząstek (co wiemy dzisiaj jako atomy), ogólną ideą było to, że materia była kontinuum, którą można było podzielić.
Ta uogólniona koncepcja uczyniła ofiarą kpiny genialnym naukowcom, takim jak James Clerk Maxwell (z równań Maxwella) i Ludwiga Boltzmana (z dystrybucji Boltzmana) coś, co wciągnęło pierwszego do szaleństwa, a drugi do samobójstwa.
W V wieku.C., Grecki filozof Leucipo i jego Demokryt uczeń użyli słowa Atom, aby wyznaczyć najmniejszy indywidualny kawałek materii.
Ta wczesna teoria atomowa różniła się od późniejszych wersji, ponieważ zawierała ideę ludzkiej duszy złożonej z bardziej wyrafinowanego rodzaju atomu rozmieszczonego przez ciało.
Teoria atomowa spadła w średniowieczu, ale ożywiła się na początku rewolucji naukowej w XVII wieku.
Na przykład Isaac Newton uważał, że materia składała się z „stałych, masywnych, twardych, nieprzeniknionych i mobilnych cząstek”.
Może ci służyć: wzór molekularny: jak to wyciągnąć, przykłady i ćwiczeniaPodzielność można podać różnymi metodami: najczęstszą dzielnością metodami fizycznymi, takimi jak siekanie jabłka nożem.
Jednak podzielność można również podać metodami chemicznymi, w których materia byłaby podzielona na cząsteczki lub atomy.
Przykłady podziału chemicznego
1. Rozpuść sól
Gdy sól jest rozpuszczona, na przykład chlorek sodu w wodzie występuje zjawisko solwatacyjne, w którym pękają jonowe powiązania soli:
NaCl → na+ + Cl-
Rozpuszczając tylko ziarno soli w wodzie, zostanie ono podzielone na miliardy jonów sodu i chlorku w roztworze.
2. Utlenianie metali w pożywce kwaśnej
Wszystkie metale, na przykład magnez lub cynk, reagują z kwasami, takimi jak rozcieńczony kwas chlorowodorowy, aby dać pęcherzyki wodoru i bezbarwny roztwór chlorku metalicznego.
Mg + HCl → Mg2+ +Cl- + H2
Oksyda na kwas metalowy przez oddzielenie wiązań metali w celu uzyskania jonów w roztworze.
3. Hydroliza estrów
Hydroliza jest pęknięciem wiązania chemicznego za pomocą wody. Przykładem hydrolizy jest hydroliza estrów, w której są one podzielone na dwie cząsteczki, alkohol i kwas karboksylowy.
4. Reakcje eliminacyjne
Reakcja eliminacyjna robi dokładnie to, co mówi: eliminuje atomy cząsteczki. Odbywa się to w celu stworzenia podwójnego wiązania węglowego. Można to zrobić za pomocą podstawy lub kwasu.
Może wystąpić w jednym skoordynowanym etapie (abstrakcja protonu w Cα, która występuje w tym samym czasie, co podział łącza Cβ-X) lub w dwóch etapach (podział łącza Cβ-X występuje najpierw do utworzenia, aby utworzyć Pośrednie karbokacja, która następnie „wyłącza się” przez abstrakcję protonu w alfa-węgiel).
Może ci służyć: Darmstadtio: odkrycie, struktura, właściwości, użycia5. Reakcja enzymatyczna aldolazy
W fazie preparatywnej glikolizy cząsteczka glukozy jest podzielona na dwie cząsteczki gliceraldehydu 3-fosforanowe (G3P) przy użyciu 2 ATP.
Enzym odpowiedzialny za to nacięcie jest aldolaza, która poprzez odwrotną kondensację dzieli cząsteczkę fruktozy 1,6-bifosforanu na cząsteczkę G3P i cząsteczkę fosforanu dihydroksyacetonu, która jest następnie izomeryzowana, tworząc kolejną cząsteczkę G3P.
6. Degradacja biomolekuł
Nie tylko glikoliza, ale cała degradacja biomolekuł w reakcjach katabolizmu, są przykładami chemicznej dzielności.
Wynika to z faktu, że duże cząsteczki, takie jak węglowodany, kwasy tłuszczowe i białka do wytwarzania mniejszych cząsteczek, takich jak acetyl COA, który wchodzi do cyklu Krebsa w celu uzyskania energii w postaci ATP.
7. Reakcje spalania
To kolejny przykład podziałalności chemicznej, ponieważ złożone cząsteczki, takie jak propan lub butan, reagują z tlenem, aby wytwarzać co₂ i wodę:
C3H8 + 52 → 3co2 + 4h2ALBO
Degradację biomolekuł można powiedzieć, że jest to reakcja spalania, ponieważ produkty końcowe to Co₂ i Woda, jednak występują w wielu krokach z różnymi pośrednikami.
8. Odwirowanie krwi
Oddzielenie różnych składników krwi jest przykładem podzielności. Pomimo tego, że jest procesem fizycznym, przykład jest interesujący, ponieważ elementy według różnicy gęstości są oddzielone przez wirowanie.
Najbardziej gęste składniki, surowica z czerwonymi krwinkami, pozostaną na dnie rurki wirówki, podczas gdy mniej gęste, plazma pozostanie w górnej części.
Może ci służyć: neutralny atom9. Bufor wodorowęglanowy
Wodorowęglan sodu, HCO3-, Jest to główny sposób transportu Co₂ w ciele produktu reakcji degradacji metabolicznej.
Związek ten reaguje z średniego protonem, wytwarzając kwas węglowy, który jest następnie podzielony na co₂ i wodę:
HCO3- + H+ D H2WSPÓŁ3 D Co₂ + H₂o
Ponieważ reakcje są odwracalne, jest to sposób, w jaki organizm, poprzez oddychanie, w celu kontrolowania fizjologicznego pH, aby uniknąć procesów alkalozy lub kwasicy.
10. Atom jądrowy lub podział rozszczepienia
W przypadku, gdy masywne jądro (takie jak uran-235) zostanie zepsute (fissions), doprowadzi do wydajności energii netto. Wynika to z faktu, że suma mas fragmentów będzie mniejsza niż masa rdzenia uranu.
W przypadku, gdy masa fragmentów jest równa lub większa niż żelazo w piku krzywej energii łącza, cząstki jądrowe będą ściślej połączone niż w jądrze uranu, a spadek masy występuje w postaci energii według postaci energii do równania Einsteina.
W przypadku elementów lżejszych niż żelazo fuzja wytwarza energię. Ta koncepcja doprowadziła do stworzenia bomby atomowej i energii jądrowej.
Bibliografia
- Reailion kwasów. BBC odzyskało.współ.Wielka Brytania.
- Foist, l. (S.F.). Reakcje eliminacyjne w chemii organicznej. Badanie odzyskało.com.
- Fisja nuklearna (s.F.). Odzyskane z hiperfizyki.

