Kwas winowy
- 1748
- 444
- Bertrand Zawadzki
Wyjaśniamy, co to jest kwas tartarowy, jego właściwości fizyczne i chemiczne, jego struktura i jego zastosowania
Co to jest kwas tartarowy?
On kwas winowy Jest to związek organiczny, którego wzorem molekularnym jest COOH (CHOH)2Cooh. Ma dwie grupy karboksylowe; To znaczy możesz wydać dwa protony (h+). Innymi słowy, jest to kwas dioprotyczny. Można go również zaklasyfikować jako kwas aldaryczny (cukier kwas.
Jego sól jest znana od niepamiętnych czasów i stanowi jeden z wtórnych produktów opracowywania wina. Jest krystalizowany jako biały osad ochrzczony jako „diamenty wina”, które gromadzą się w korku lub na dnie beczek i butelek. Ta sól jest bitarratem potasu (lub kwas potasu tartrato).
Sole kwasu tartarowego mają wspólną obecność jednego lub dwóch kationów (na+, K+. NH4+, AC2+, itp.) Ponieważ uwalniając dwa protony, pozostaje ujemnie naładowany obciążeniem -1 (jak w przypadku soli biterrato) lub -2.
Z kolei ten związek był przedmiotem studiów i nauczania teorii organicznych związanych z aktywnością optyczną, dokładniej z stereochemią.
Gdzie jest kwas tartarowy?
Kwas tartarowy jest składnikiem wielu roślin i żywności, takich jak morel, awokado, jabłka, tamaryndo, nasiona słonecznika i winogrona.
W trakcie starzenia win ten kwas - do niskich temperatur - łączy się z potasem, aby krystalizować jako tartrato. W czerwonych win koncentracja tych tartratów jest mniejsza, podczas gdy w białych winach są bardziej obfite.
Trwraty są solą białych kryształów, ale kiedy zatrzymują zanieczyszczenia środowiska alkoholowego, nabywają czerwonawe lub fioletowe tony.
Może ci służyć: reakcja przemieszczeniaStruktura kwasu tatarowego
 Struktura molekularna kwasu tatarowego
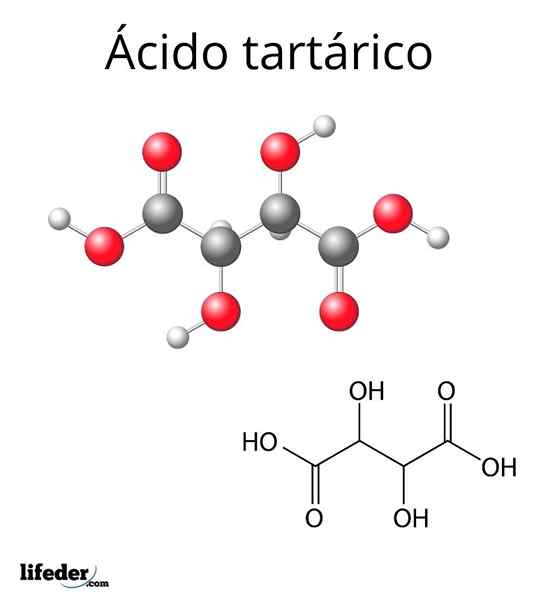
Struktura molekularna kwasu tatarowego Struktura cząsteczkowa kwasu tartarowego jest reprezentowana na górnym obrazie. Grupy karboksylowe (-COOH) znajdują się na bocznych końcach i są oddzielone krótkim dwoma łańcuchami węglowymi (c2 i C3).
Z kolei każdy z tych węgli jest powiązany z H (białą kulę) i grupą OH. Ta struktura może obrócić łącze C2-C3, generując w ten sposób kilka konformacji, które stabilizują cząsteczkę.
Oznacza to, że centralny ogniwo złamanej cząsteczki jako obracającego się cylindra, kolejno naprzemiennie przestrzennego rozmieszczenia grup -COOH, H i OH (projekcje Newmana).
Na przykład na obrazie dwie grupy OH wskazują w przeciwnych kierunkach, co oznacza, że są ze sobą w pozycjach przeciw. To samo dotyczy grup -cooh.
Kolejną możliwą konformacją jest kilka zaćmionych grup, w których obie grupy są zorientowane w tym samym kierunku. Te konformacje nie odegrałyby ważnej roli w strukturze związku, jeśli wszystkie grupy węgla C2 i C3 Były takie same.
Jak w tym związku cztery grupy są różne (-COOH, OH, H, a druga strona cząsteczki), węglowodory są asymetryczne (lub chirały) i wykazują słynną aktywność optyczną.
Sposób, w jaki grupy są ułożone w węglowodory2 i C3 kwasu tartarowego określa różne struktury i właściwości dla tego samego związku; Oznacza to, że pozwala na istnienie stereoizomerów.
Zastosowania kwasu tartarowego
W branży spożywczej
Jest używany jako stabilizator eulsiona w piekarniach. Jest również używany jako składnik drożdży, dżemu, żelatyny i napojów bezalkoholowych. Wypełnia również funkcje jako zakwaszenie, biblioteka i oferent jon.
Może ci służyć: bromek sodu (NABR)Kwas tartarowy znajduje się w tych produktach: słodkie ciasteczka, cukierki, czekoladki, płyny gazowe, produkty piekarnicze i wina.
W opracowaniu wina jest używane do tego, aby były bardziej zrównoważone, z podmuchowego punktu widzenia, zmniejszając pH tych.
W branży farmaceutycznej
Jest stosowany w tworzeniu tabletek, antybiotyków i musujących pigułek, a także w lekach stosowanych w leczeniu chorób serca.
W przemyśle chemicznym
Jest stosowany w fotografii, a także w galwanotechnika i jest idealnym przeciwutleniaczem dla tłuszczów przemysłowych.
Jest również stosowany jako porywacz z metalowego jonu. Jak? Obracając swoje linki w taki sposób, aby można było zlokalizować atomy tlenu w grupie karbonylowej, bogate w elektrony, wokół tych pozytywnie obciążonych gatunków.
W branży budowlanej
Opóźnij proces utwardzania gipsu, cementu i tynku, dzięki czemu manipulacja tymi materiałami jest bardziej wydajna.
Właściwości kwasu tartarowego

Najczęstsze zastosowania kwasu tartarowego to:
- Kwas tartarowy jest sprzedawany w postaci krystalicznego proszku lub lekko nieprzezroczystych białych kryształów. Ma przyjemny smak, a ta nieruchomość wskazuje na wino dobrej jakości.
- Topi się przy 206 ° C i płonie w 210 ° C. Jest bardzo rozpuszczalny w wodzie, alkohole, podstawowych roztworach i boraksie.
- Jego gęstość wynosi 1,79 g/ml w 18 ° C i przedstawia dwa stałe kwasowości: PKA1 i PKA2. Oznacza to, że każdy z dwóch kwasowych protonów ma swoją własną tendencję do uwolnienia się w środowisku wodnym.
- Podobnie jak grupy -coh i OH, można go analizować za pomocą spektroskopii w podczerwieni (IR) pod kątem ich jakościowych i ilościowych.
- Inne techniki, takie jak spektroskopia masowa i jądrowy rezonans magnetyczny, umożliwiają poprzednią analizę tego związku.
Stereochemia

Kwas tartarowy był pierwszym związkiem organicznym, do którego opracowano rozdzielczość enancjomeryczną. Co to znaczy? Oznacza to, że jego stereoizomery można ręcznie oddzielić dzięki pracom badawczym biochemiku Louisa Pasteura w 1848 r.
I jakie są stereoizomery kwasu tartarowego? Są to: (r, r), (s, s) i (r, s). R i S to konfiguracje przestrzenne węgli C2 i C3.
Kwas tartarowy (R, R), najbardziej „naturalny”, obraca spolaryzowane światło po prawej; Kwas tartarowy (S, S) jest złamany w lewo, w przeciwieństwie do igieł zegara. I wreszcie kwas tartarowy (R, S) nie łamie spolaryzowanego światła, będąc optycznie nieaktywnym.
Louis Pasteur, za pomocą mikroskopu i pincetów, znaleziony i oddzielone kryształy kwasu tatarowego, które wykazały wzorce „prawe” i „lewe”, takie jak na obrazie wyższym.
W ten sposób kryształy „prawe” to kryształy utworzone przez enancjomer (R, R), podczas gdy kryształy „lewe” to kryształy enancjomeru (S, S).
Jednak kryształy kwasu tatarowego (R, S) nie różnią się od innych, ponieważ wykazują jednocześnie wykwalifikowane i lewe cechy; Dlatego nie można ich „rozwiązać”.
Bibliografia
- Wikipedia. (2018). Kwas winowy. Odzyskane z.Wikipedia.org
- Pubchem. (2018). Kwas winowy. Odzyskane z Pubchem.NCBI.NLM.Nih.Gov.
- Zrozumienie wina tartatów. Odzyskany z Jordanwinery.com
- Aktywny. Kwas winowy. Wyzdrowiał z Actipedia.org
- Pochteca. Kwas winowy. Pochteca wyzdrowiał.com.MX
- Dhanesshwar Singh i in. (2012). O pochodzeniu optycznej bezczynności kwasu mezo-tartarowego. Department of Chemistry, Manipur University, Canchipur, Imphal, Indie. J. Chem. Pharm. Wołowina., 4 (2): 1123-1129.

