Struktura kwasu perracetowego, właściwości, uzyskiwanie, zastosowania
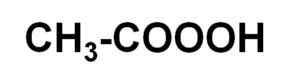
- 5086
- 1196
- Prokul Woliński
On kwas nadoctowy Jest to ciekłego związku organicznego, którego wzorem chemicznym wynosi c2H4ALBO3. Jest to nadtlenek kwasu octowego, więc jest również znany jako kwas perksetyczny. Jego cząsteczka jest podobna do cząsteczki kwasu octowego CH3COOH, ale z dodatkowym tlenem w karboksylu.
Należy do klasy nadtlenków organicznych, które są cząsteczkami stworzonymi przez człowieka. Od 1902 r. To działanie może w niektórych przypadkach ćwiczyć w stężeniach tak niskich jak 0,001%.
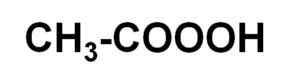 Kwas nadoctowy. Autor: Marilú Stea.
Kwas nadoctowy. Autor: Marilú Stea. Ta właściwość sprawia, że jest szeroko stosowana w klinikach i szpitalach do sterylizacji sprzętu medycznego, z dodatkową zaletą, że ich produkty rozkładowe nie są toksyczne dla ludzi.
Rozwiązania PAA silnie utleniają, cecha, która została użyta do wybielania pulpy papierowej lub pralni. Dotyczy również wykonywania reakcji chemicznych, w których wymagana jest ta właściwość, takie jak epoksydacja i hydroksylacja.
Jego utlenianie i działania dezynfekujące wykorzystano w czyszczeniu sprzętu, w którym przetwarzane są żywność i napoje. Ponadto jest żrący w niektórych metalach, a po przechowywaniu musi być trzymane z dala od związków organicznych lub łatwo utlewalnych.
Powiedź, że twoje skoncentrowane roztwory mogą być wybuchowe, dlatego musi najlepiej przygotowywać i przechowywać w zimnych miejscach. Jego potajemna siła dotyczy również skóry, błon śluzowych i tkanek człowieka, więc należy ją manipulować ostrożnością i sprzętem ochronnym.
[TOC]
Struktura
Kwas perxyoctowy ma cząsteczkę bardzo podobną do cząsteczki kwasu octowego, ale z dodatkowym tlenem w strukturze grupy -COOH, ponieważ ma 3 atomy tlenu zamiast dwóch.
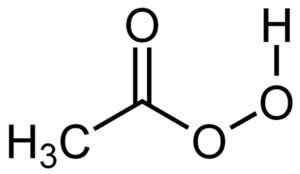 Struktura kwasu otworowego. Autor: Su-no-g. Źródło: Selfmade. Źródło: Wikipedia Commons.
Struktura kwasu otworowego. Autor: Su-no-g. Źródło: Selfmade. Źródło: Wikipedia Commons. Nomenklatura
- Kwas nadoctowy
- Kwas perxyoctowy
- Kwas etanooperoksoinowy
- PAA (angielski akronim Kwas peroksoctowy).
Nieruchomości
Stan fizyczny
Przezroczysty bezbarwny płyn z ostrym zapachem octu.
Waga molekularna
76,05 g/mol
Punkt wrzenia
110 ° C (z eksplozją)
Temperatura zapłonu
40,5 ° C (metoda otwartego kubka)
Temperatura samokierowania
200 ° C (jest to temperatura spontanicznie)
Gęstość
1 226 g/cm3 w 15 ° C
Breja
3280 CP przy 25,6 ° C
Współczynnik załamania światła
1 3974 do 20 ° C
Rozpuszczalność
Jest mieszany z wodą w dowolnym proporcji. Jest rozpuszczalny w polarnych rozpuszczalnikach organicznych, takich jak etanol. Lekko rozpuszczalne w aromatycznych rozpuszczalnikach. Bardzo rozpuszczalne w eterze i kwasie siarkowym.
Ph
Mniej niż 2.
Stała dysocjacji
PkDo = 8,20 do 25 ° C (jest słabszy niż kwas octowy, który ma PKDo = 4,8)
Właściwości chemiczne
Jako kwas, PAA jest znacznie słabsza niż kwas, z którego przychodzi kwas octowy.
Przedstawia wysoki potencjał jako utleniacz. Jest wysoce reaktywny, więc jest trudny do przechowywania, a to ograniczyło jego użycie.
Jego produkty degradacji to kwas octowy CH3COOH, tlen lub2, Nadtlenek wodoru h2ALBO2 i woda h2ALBO. H2ALBO2 z kolei degraduje się do wody i tlenu. Wszystkie te związki są bezpieczne dla środowiska.
Jest to środek epoksydacyjny i hydroaksilatu dla wiązań olefinowych (podwójne łącza C = C). Oznacza to, że aktywnie uczestniczy w tworzeniu epoksydów w podwójnych wiązaniach cząsteczek organicznych i w dodaniu w tych grupach -OH.
PAA jest żrący w stosunku do niektórych metali, takich jak gładka stal, ocynkowana żelazo, miedź, mosiądz i brąz. Inne metale są odporne, takie jak stal nierdzewna, czyste aluminium i żelazo tkankowe.
Może ci służyć: związek chemicznyAtakują syntetyczne i naturalne dziąsła i wydobywa plastyfikator niektórych polimerów winylowych.
Ma ostry i akrowy zapach przypominający kwas octowy (kwas octowy jest głównym składnikiem octu).
Uzyskanie
Poprzez reakcję lodowcowego kwasu octowego (bezwodne, to znaczy bez wody) z nadtlenkiem wodoru H2ALBO2 W obecności kwasu mineralnego (takiego jak kwas siarkowy H2południowy zachód4), część roztworów utlenionych kwasu octowego i wodnych roztworów na kwasu, kwasu octowego i H2ALBO2.
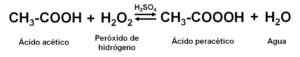 Uzyskanie wodnych roztworów kwasowych. Autor: Marilú Stea
Uzyskanie wodnych roztworów kwasowych. Autor: Marilú Stea H2południowy zachód4 działa jak katalizator lub akcelerator reakcji. Stosowane są środki stabilizatora, takie jak pirydyna-2,6-dikarboksylowy kwas.
Jeśli roztwory te są destylowane, można uzyskać wyższe stężenie o zastosowaniu.
Można go również uzyskać przez utlenianie acetaldehydu CH3Cho z ozonem lub3, lub przez reakcję bezwodnika octowego (CH3WSPÓŁ)2Lub z h2ALBO2.
Innym sposobem na uzyskanie go w miejscu, w którym jest to wymagane, jest dodanie tetra-acetylo-etylendiaminy (TAED) do alkalicznego roztworu H H2ALBO2.
Aplikacje
W medycynie jako sterylizator sprzętu
PAA działa jako środki dezynfektywne sprzętu medycznego w klinikach, szpitalach, biurach medycznych i dentystycznych.
 Sterylizowany sprzęt dentystyczny. Autor: Daniel Frank. Źródło: Pexels.
Sterylizowany sprzęt dentystyczny. Autor: Daniel Frank. Źródło: Pexels. Niektóre źródła podają, że ich działanie przeciwko mikroorganizmom można klasyfikować, a także: Bakterie> Wirus> Bakterie zarodniki> Protozoan Cysts. Oznacza to, że jest bardziej skuteczny wobec bakterii i mniej skuteczny w stosunku do torbieli pierwotniaków.
W badaniach przeprowadzonych na temat bakteriobójczego działania PAA i innych środków dezynfekujących na wysokim poziomie Staphylococcus aureus I Pseudomonas aeruginosa W wyposażeniu endoskopii PAA okazało.
On Staphylococcus aureus Może wytwarzać infekcje w tkankach miękkich, w skórze, zapaleniu płuc i infekcji tkanek serca. Pseudomonas aeruginosa Może produkować zapalenie płuc.
Bakterie tworzą biofilmy, które chronią je przed bodźcami zewnętrznymi lub stresem, poprzez grubą warstwę białek pozakomórkowych, polisacharydów i kwasów nukleinowych.
Te biofilmy są wysoce oporne na typowe antybiotyki i środki dezynfekujące. W zespołach takich jak endoskopy są zwykle tworzone w wąskich kanałach, ze względu na niezbyt odpowiednie lub nie skuteczne procedury czyszczenia i dezynfekcji.
PAA atakuje te biofilmy prawdopodobnie przez utlenianie najbardziej wrażliwych wiązań cząsteczkowych białek, enzymów i innych metabolitów. To prowadzi do pęknięcia ścian komórkowych zarodków, ich zarodników i torbieli.
Ponadto, podczas penetracji komórki, PAA może utleniać niezbędne enzymy, szkodząc transportowi cząsteczek i istotnych procesów biochemicznych.
Czasy dezynfekcji ustalono od kilku lat, ale podczas niektórych badań zaobserwowano, że leczenie PAA spowodowało zmiany w kształcie komórek po zaledwie 5 minutach, z tworzeniem się worków lub wybrzuszeniami w ścianie komórkowej bakterii i zapadnięciem się komórkową Struktury mikroorganizmów po 30 minutach.
Chociaż PAA wyróżniała się ze względu na swoją prędkość, naukowcy zalecili ponowne ponowne ponowne czasy ustalone w protokołach czyszczenia i dezynfekcji, zwiększając je dla większości antyseptyków na wysokim poziomie, aby zapewnić całkowitą skuteczność ich.
Jednym z negatywnych aspektów PAA jest to, że istnieją pewne patogeny, do których nie jest bardzo skuteczne, takie jak torbiele Giardia Lamblia i Cryptosporidium parvum (pasożyty, które mogą wytwarzać biegunkę lub inne warunki jelitowe).
W oczyszczaniu ścieków
Dezinfekcyjny wpływ PAA na ścieki miejskie lub branże był badany od ponad 30 lat.
Może ci służyć: wodorek potasu: struktura, formacja, właściwości Resztkowy oczyszczalnia wody. Autor: Michal Jarmoluk. Źródło: Pixabay.
Resztkowy oczyszczalnia wody. Autor: Michal Jarmoluk. Źródło: Pixabay. Wśród jego zalet jest szerokie spektrum jej aktywności bakteriobójczej nawet w obecności materii organicznej, a także fakt, że dla środowiska nie generują żadne szkodliwe produkty wtórne.
Skuteczność jego działania wydaje się zależeć między innymi czynnikami ilości materii organicznej obecnej w ścieku, od rodzaju i ilości mikroorganizmów, które mają zostać wyeliminowane, od stężenia PAA w wodzie, które ma być poddane obróbce, pH i Czas trwania leczenia.
W niektórych przypadkach PAA okazało się lepsze niż podchloryn sodu w celu dezynfekcji ścieków w klimatach tropikalnych i jest skuteczny przeciwko wirusowi cholery, wśród wielu innych patogenów.
Jednak jednym z negatywnych punktów jest to, że z powodu pozostałego kwasu octowego po dezynfekcji ścieki wodne są obciążone materią organiczną, co zwiększa ryzyko nowego wzrostu mikroorganizmów.
Z drugiej strony jest to drogi produkt, więc nie jest jeszcze bardzo konkurencyjny na przykład w przypadku podchlorynu sodu z powodu tego aspektu.
W branży spożywczej
Bycie silnym środkiem utleniającym jest bardzo skuteczne przeciwko mikroorganizmom w niskich temperaturach, co spowodowało jego szerokie zastosowanie jako bakteriobójcze i grzybobójcze w przetwarzaniu żywności i napojów.
Obejmuje to rośliny przetwarzania mięsa i kurczaka, nabiał, browar, winiarzy lub winnice wina i napoje bezalkoholowe. We wszystkich tych miejscach PAA dotyczy idealnego czyszczenia In situ (w miejscu).
Enzymy występujące w niektórych pokarmach, takich jak peroksydaza i katalaza, które dezaktywują nadtlenek wodoru H2ALBO2, Nie wywierają szkodliwego wpływu na spożywanie kwasu. Odpady białkowe również go nie szkodzą.
Ze względu na fakt, że w żywności PAA rozkłada się w kwasie octowym i wodorze wodorze, jego zastosowanie jest uważane za bezpieczne w zastosowaniach, w których żywność nie jest przepłukana.
Służy jako dezynfekujący i sterylizujący dla zbiorników ze stali nierdzewnej i szklanej, rur i zbiorników, które służą do transportu i przechowywania napojów.
 Zbiorniki ze stali nierdzewnej do przechowywania piwa. Autor: Roberta Keiko Kitahara Santana. Źródło: Unspash.
Zbiorniki ze stali nierdzewnej do przechowywania piwa. Autor: Roberta Keiko Kitahara Santana. Źródło: Unspash. Jego charakterystyka do generowania produktów nietoksycznych i że w wysokim rozcieńczeniu nie wytwarzają smaków ani zapachów, stanowią oszczędności czasu i pieniędzy dla tych branż.
W branży miazgi i papieru
Kwas perracetowy jest ważnym środkiem pozbawionym chloru w technologii wybielania w branży produkcji pulpy papierowej.
Niektórzy autorzy uważają kwas okretowy za aktywowaną pochodną H2ALBO2, Gdzie jeden z hydrogenów został zastąpiony grupą ACILO CH3C (= o)-.
W rezultacie, co kwas w reaguje z substratami organicznymi w większym stopniu niż H2ALBO2 i to można zastosować w reakcjach utleniania w bardziej umiarkowanych warunkach niż w przypadku H2ALBO2.
W warunkach neutralnych lub umiarkowanie alkalicznych jonowe peracetan CH3C (= O) OO- za to, że jest silnym nukleofilem (jest go przyciągany przez atomy z niedoborem elektronów), selektywnie wymieszaj chromofory lub kolorowe związki obecne w pulpie papierowej.
To pozwala tym branżom mieć bardzo skuteczny wybielacz i których odpady nie zanieczyszczają ich wodnych ścieków.
Może ci służyć: jaki jest błąd?W produkcji innych związków chemicznych
Kwas perracytowy służy jako utleniacz do przygotowania związków epoksydowych, jako katalizator do produkcji żywic poliestrowych i uzyskiwania kaprolaktamu i glicerolu.
W odzyskiwaniu polimerów do recyklingu
Niektórym badaczom udało się odzyskać przydatne materiały podczas obróbki niektórych odpadów polimerowych za pomocą rozwiązań PAA.
Proces przeprowadza się przez utlenianie pewnych odpadów polimerów wzmocnionych włóknem węglowym z aktywności lotniczej, roztworami kwasu lodowcowego i nadtlenkiem wodoru.
W ten sposób wygenerowane jest, aby kwas generował In situ, który rozkłada żywicę epoksydową o 97%, pozostawiając nienaruszone włókno węglowe.
Następnie odzyskuje się destylację ponad 90% kwasu octowego, co powoduje dodatkowy rozkład polimeru, który generuje odzyskane związki alifatyczne i fenolowe.
Włókno węglowe jest uzyskiwane czyste i utrzymuje jego długość i odporność na trakcję porównywalną z długości włókien dziewiczych.
 Włókno węglowe. CJP24 [domena publiczna]. Źródło: Wikipedia Commons.
Włókno węglowe. CJP24 [domena publiczna]. Źródło: Wikipedia Commons. Proces przeprowadzany jest w miękkich warunkach, bez emisji gazowych, co czyni go przyjaznym dla środowiska.
W praniu
Ze względu na moc utleniającą kolorowe związki, kwas okacyjny jest wykorzystywany do bielenia prania. W takich przypadkach stosuje się mieszaninę tetra-atylo-etylendiaminy z H2ALBO2 W pożywce alkalicznej, aby uzyskać go na stronie.
Jego przedział zastosowania jest bardzo szeroki, ponieważ może być stosowany w twardych wodach lub zawiera wysoki odsetek soli wapnia i magnezu, w pH od 3,0 do 7,5 i temperatury od 0 do 40 ° C.
Ryzyko
Kwas perracytowy lub PAA może być wysoce żrący. Jest silnie irytujący dla skóry i oczu.
Jeśli ich roztwory są spożywane, spowoduj korozję błon śluzowych jamy ustnej, gardła, przełyku i przewodu pokarmowego, powodując ból i trudności z połykaniem.
Jeśli ich opary są wdychane.
Rozwiązania zawierają. Mogą rozłożyć wybuchowo. Jeśli stężenie PAA w roztworze przekracza 56% może wywołać z powodu gwałtownego parowania kwasu octowego.
Należy unikać ciepła. Jest uważany za łatwopalny ciecz. Jego rozkład jest gwałtowny z eksplozji w temperaturze 110 ° C. Musi być przechowywany w świeżych miejscach, najlepiej w chłodzeniu lub w bardzo dobrze wentylowanych miejscach.
Jest to zatem silnie utleniający w kontakcie z materiałami organicznymi. Po przechowywaniu należy go izolować z innych związków, zwłaszcza organicznych, paliwa, łatwopalnych lub utlewalnych związków. Musi być oddzielony od kwasów, alkaliów i metali ciężkich.
Po podgrzaniu do rozkładu emituje akry i irytujące opary, które podrażniają oczy, nos i gardło.
Jeśli jest rozlany, nie należy jej dopuścić do pływania do drenach, ponieważ w tych niebezpieczeństwach ognia lub wybuchu jest tworzone.
Jako zalecane są środki zapobiegawcze do obsługi, gumowe rękawiczki i odzież ochronna, ochrona twarzy lub ochrony oka (okulary lub szklanki bezpieczeństwa), ochrona oddechowa i nie jedzenie, picie lub palenie podczas pracy z roztworami.
Bibliografia
- LUB.S. National Library of Medicine. (2019). Kwas nadoctowy. Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov
- Das, m. i in. (2018). Skuteczna metoda reycling odpadów CFRP przy użyciu kwasu okretowego. ACS Zrównoważona chemia i inżynieria. Odzyskane z pubów.ACS.org.
- Chińczycy, t. i in. (2017). Morfologiczne bakteriobójcze szybko działające efekty kwasu okretowego, dezynfekującego wysokiego poziomu, przeciwko Staphylococcus aureus I Aeruginous pseudomcas Biofilmy w rurkach. Odporuj na leki przeciwmionowe kontrola infekcji. 2017: 6: 122. NCBI odzyskało.NLM.Nih.Gov.
- Chleb, g.X. i in. (1999). Reaktywność kwasu ferulowego i jego czerpią w kierunku pozycji wodorowej i kwasu otworowego. J. Rolnictwo. Żywność Chem. 1999, 47, 3325-3331. Odzyskane z pubów.ACS.org.
- Kitis, Mehmet. (2004). Rozkoszkowanie ścieków za pomocą kwasu okretowego: przegląd. Environment International 30 (2004) 47-55. Odzyskane z naukowym.com.
- « Struktura kwasu fenylooctowego, właściwości, zastosowania, efekty
- Charakterystyka myślenia pionowego, metoda i przykłady »

