Węgiel anomeryczny, co jest, charakterystyka, przykłady
- 957
- 50
- Matylda Duda
On Węgiel anomeryczny Jest to stereocentro obecny w cyklicznych strukturach węglowodanów (mono lub polisacharydy))). Będąc sterecentro, dokładnie dokładnie epimerus, czerpią z niego dwa diastereoizomery, oznaczone literami α i β; Są to anomery i są częścią obszernej nomenklatury w świecie cukrów.
Każdy anomer, α lub β, różni się w pozycji OH grupy węgla Anómerico w odniesieniu do pierścienia; Ale w obu węglem anomerycznym jest taki sam i znajduje się w tym samym miejscu cząsteczki. Anomery to cykliczne hemicetale, produkt reakcji wewnątrzcząsteczkowej w otwartym łańcuchu cukrów; być aldose (aldehydos) lub ketosy (ketony).
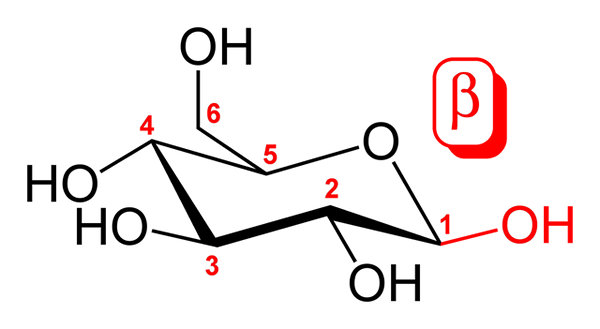
 Konformacja krzesła dla β-D-glukopiranozy. Źródło: Commons Wikimedia.
Konformacja krzesła dla β-D-glukopiranozy. Źródło: Commons Wikimedia. Górny obraz pokazuje konformację krzesła dla β-D-glukopiranozy. Jak widać, składa się z sześcioczęściowego pierścienia, w tym atomu tlenu między węglemi 5 i 1; Ten ostatni, a raczej pierwsza, to węgiel anómerico, który tworzy dwa proste wiązania z dwoma atomami tlenu.
Jeśli jest to szczegółowo obserwowane, grupa 1 OH CARBON 1 jest zorientowana nad pierścieniem sześciokątnym, a także grupa CH2Oh (Carbon 6). To jest anomer β. Z drugiej strony anomer α różniłby się tylko w tej grupie OH, która byłaby zlokalizowana na pierścieniu, tak jakby był to transtereoizomer.
Hemiacetale
Konieczne jest nieco bardziej pogłębione w koncepcji hemicetalów, aby lepiej zrozumieć i rozróżnić anomeryczny węgiel. Hemiacetale są produktem reakcji chemicznej między alkoholem a aldehydem (aldoza) lub ketonem (ketos).
Ta reakcja może być reprezentowana z następującym ogólnym równaniem chemicznym:
Może ci służyć: polik winylpirolidonu: struktura, właściwości, zastosowania, skutki uboczneRoh + r'cho => roch (oh) r '
Jak widać, alkohol reaguje z aldehydem, tworząc hemiacetal. Co by się stało, gdyby zarówno R, jak i R 'należą do tego samego łańcucha? W takim przypadku istniałby cykliczny hemiacetal, a jedynym możliwym sposobem, w jaki można go utworzyć, jest to, że zarówno grupy funkcjonalne, -OH i -cho, są obecne w strukturze molekularnej.
Ponadto struktura musi składać się z elastycznego łańcucha i z zdolnymi powiązaniami w celu ułatwienia nukleofilowego ataku OH w kierunku węgla karbonylowego grupy CHO. Kiedy tak się dzieje, struktura zamyka się w pierścieniu pięciu lub sześciu członków.
Cykliczny hemiacetal
 Cykliczne tworzenie hemiacetalu. Źródło: Alejandro Porto [CC BY-SA 3.0 (https: // creativeCommons.Org/licencje/by-sa/3.0)]
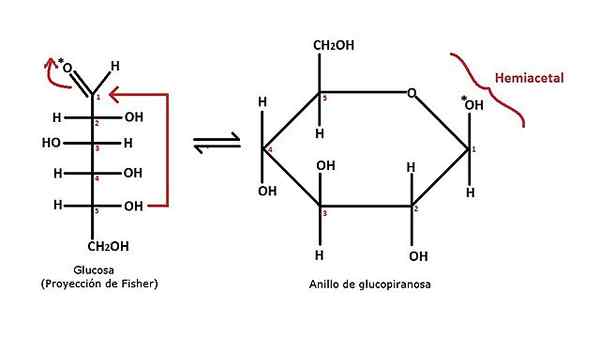
Cykliczne tworzenie hemiacetalu. Źródło: Alejandro Porto [CC BY-SA 3.0 (https: // creativeCommons.Org/licencje/by-sa/3.0)] Na górnym obrazie pokazano przykład tworzenia cyklicznego hemiacetalu dla monosacharydu glukozy. Można zauważyć, że składa się z Aldosa, z grupą cho aldehydu (węgiel 1). Jest to zaatakowane przez grupę węgla OH 5, jak wskazuje czerwona strzałka.
Struktura przechodzi od bycia otwartym łańcuchem (glukozą), do piranicznego pierścienia (glukopofareous). Początkowo nie może być żadnego związku między tą reakcją a nowo wyjaśnionym dla hemiacetal; Ale jeśli pierścień jest starannie obserwowany, szczególnie w sekcji C5-O-C1(OH) -C2, Należy docenić, że odpowiada to oczekiwanym szkielecie dla hemiacetal.
Węglowodory 5 i 2 reprezentują odpowiednio R i R 'ogólnego równania. Ponieważ są one częścią tej samej struktury, jest to następnie cykliczny hemiacetal (a pierścień wystarczy, aby być widocznym).
Charakterystyka węgla anomerycznego i jak go rozpoznać
Gdzie jest anomeryczny węgiel? W glukozie jest to grupa cho, która może ponieść atak nukleofilowy OH albo poniżej lub powyżej. W zależności od orientacji ataku powstają dwa różne anomery: α i β, jak już wspomniano.
Może ci służyć: zjawiska chemiczne: cechy i przykładyDlatego pierwszą cechą, jaką posiada ten węgiel, jest to, że w otwartym łańcuchu cukru jest tym, który cierpi na atak nukleofilowy; Oznacza to, że jest to grupa cho, dla Aldos lub grupy R2C = o, dla ketusów. Jednak po utworzeniu cyklicznego hemiacetal lub pierścienia ten węgiel może sprawić wrażenie, że zniknął.
To tutaj istnieją inne bardziej specyficzne funkcje, aby zlokalizować go w każdym piranoso lub futrzanym pierścieniu każdego węglowodanu:
-Węgiel anomeryczny jest zawsze po prawej lub lewej stronie atomu tlenu, który tworzy pierścień.
-Co ważniejsze, jest to powiązane nie tylko z tym atomem tlenu, ale także z grupą OH, od Cho lub R2C = O.
-Jest asymetryczny, to znaczy ma cztery różne podstawy.
Z tymi czterema cechami łatwo rozpoznać anomeryczny węgiel obserwujący każdą „słodką strukturę”.
Przykłady
Przykład 1
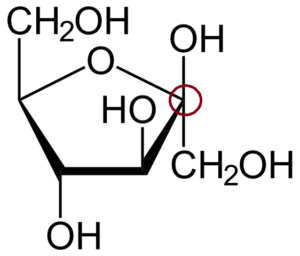 β-D-frucofuranosa. Źródło: Neurotoger (Talk • Wpisss) [domena publiczna]
β-D-frucofuranosa. Źródło: Neurotoger (Talk • Wpisss) [domena publiczna] W górę.
Aby zidentyfikować węgiel anomeryczny, musisz najpierw obserwować węgle po lewej i prawej stronie atomu tlenu, który tworzy pierścień. Następnie tym, który jest powiązany z grupą OH, jest węgiel anomeryczny; że w tym przypadku jest już zamknięte w czerwonym okręgu.
To jest anomer β, ponieważ OH z węgla anomerycznego znajduje się nad pierścieniem, podobnie jak chip2Oh.
Przykład 2
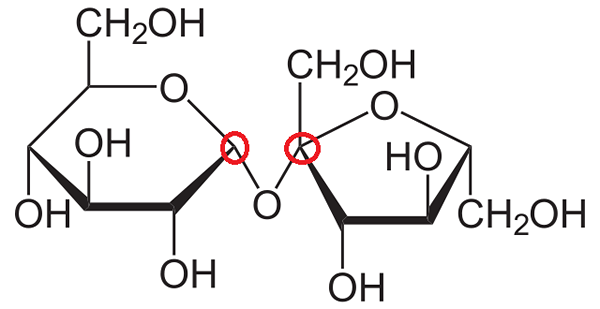 Sacharoza. Źródło: Neuropoger przez Wikipedia.
Sacharoza. Źródło: Neuropoger przez Wikipedia. Teraz stara się wyjaśnić, jakie anomeryczne węgle są w strukturze sacharozy. Jak widać, składa się z dwóch monosacharydów połączonych kowalencyjnie przez wiązanie glikozydowe, -o-.
Może ci służyć: nadanganinian sodu (namnO4): właściwości, ryzykoPrawy pierścień jest dokładnie taki sam, nowo skomentowany: β-d-frucofuranosa, tylko że jest „obrócony” w lewo. Węgiel anomeryczny pozostaje taki sam w poprzednim przypadku i spełnia wszystkie cechy, których można by się od niego oczekiwać.
Z drugiej strony pierścień po lewej to α-D-glukopiranoza.
Powtarzając tę samą procedurę rozpoznawania anomerycznego węgla, patrząc na dwa węgle po lewej i prawej stronie atomu tlenu, okazuje się, że prawy węgiel jest powiązany z grupą OH; który uczestniczy w więzi glukozydowej.
Dlatego oba anomeryczne węgle są połączone przez -o- i dlatego są zamknięte w czerwonych kółkach.
Przykład 3
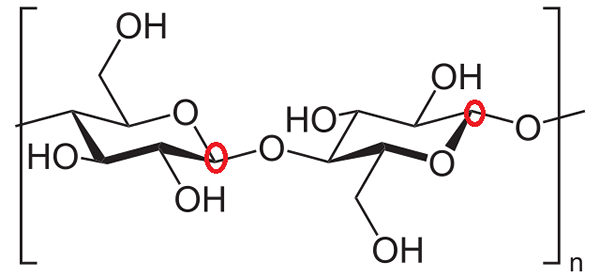 Celuloza. Źródło: Neuropoger [domena publiczna]
Celuloza. Źródło: Neuropoger [domena publiczna] Na koniec proponuje się zidentyfikowanie anomerycznych węgli dwóch jednostek glukozy w celulozie. Ponownie, węgle są obserwowane wokół tlenu wewnątrz pierścienia i stwierdzono, że w pierścieniu glukozy po lewej stronie anomeryczny węgiel uczestniczy w wiązaniu glukozydowym (zablokowane w czerwonym okręgu).
Jednak w pierścieniu glukozy po prawej, węgiel anomowy jest po prawej stronie tlenu i można go łatwo zidentyfikować, ponieważ jest powiązany z tlenem wiązania glukozydowego. Zatem oba anomeryczne węgle są w pełni zidentyfikowane.
Bibliografia
- Morrison, r. T. i Boyd, R, N. (1987). Chemia organiczna. 5ta Wydanie. Redakcja Addison-Wesley Inter-American.
- Carey f. (2008). Chemia organiczna. (Szósta edycja). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Chemia organiczna. Aminy. (10th Wydanie.). Wiley Plus.
- Rendina g. (1974). Techniki biochemii zastosowane. Inter -American, Meksyk.
- Chang s. (S.F.). Przewodnik po anomerycznym węglku: jaki jest anomeryczny węgiel? [PDF]. Odzyskane z: chem.UCLA.Edu
- Gunawardena G. (13 marca 2018 r.). Anomeria węgla. Chemia librettexts. Odzyskane z: chem.Librettexts.org
- Foist l. (2019). Węgiel anomeryczny: definicja i przegląd. Badanie. Odzyskane z: Study.com

