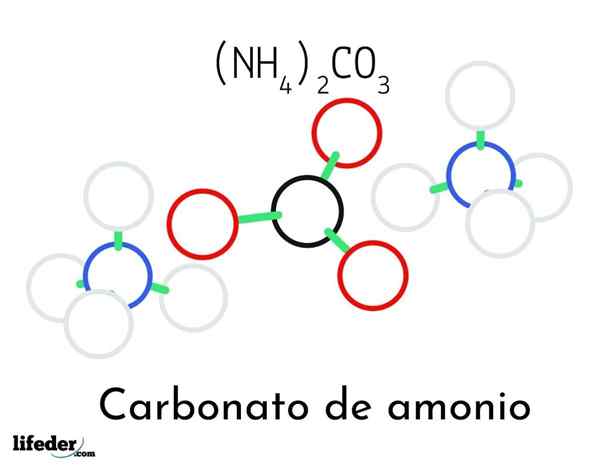
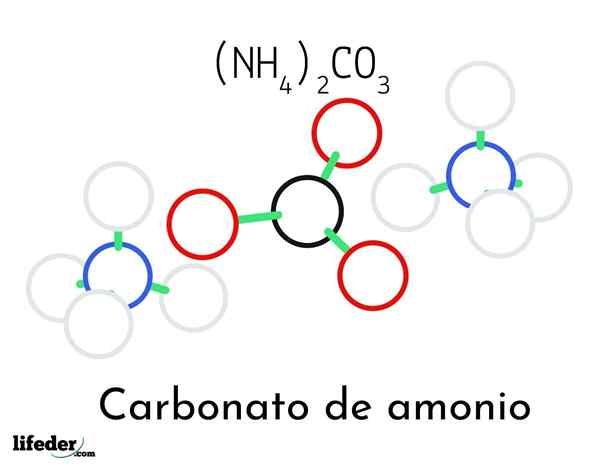
Węglan amonu ((NH4) 2CO3)
- 1044
- 124
- Marianna Czarnecki
Co to jest węglan amonu?
On Węglan amonu Jest to nieorganiczna sól azotowa, szczególnie amoniakalna, której wzór chemiczny jest (NH4)2WSPÓŁ3. Jest to opracowane metodami syntezy, wśród których warto użyć sublimacji mieszaniny siarczanu amonu i węglanu wapnia: (NH4)2południowy zachód4(s)+ caco3(s) => (NH4)2WSPÓŁ3(S)+ sprawa4(S).
Zasadniczo sole amonu i węglan wapnia są ogrzewane w pojemniku, powodując węglan amonu. Metodą przemysłową, która wytwarza tony tej soli, jest przekazanie dwutlenku węgla przez kolumnę absorpcyjną, która zawiera roztwór amonu w wodzie, a następnie wykonanie destylacji.
Opary zawierające amon, dwutlenek węgla i woda są skondensowane z tworzeniem kryształów węglanu amonu: 2nh3(g)+ h2Lub (l) + co2(g) → (NH4)2WSPÓŁ3(S). W reakcji występuje kwas węglowy, h2WSPÓŁ3, Po rozpuszczeniu dwutlenku węgla w wodzie, i to ten kwas daje swoje dwa protony, h, h+, do dwóch cząsteczek amoniaku.
Właściwości węglanu amonu
 Wygląd węglanu amonu
Wygląd węglanu amonu Jest to biała, krystaliczna i bezbarwna stała, z silnymi zapachami i smakami amoniaku. Topi się do 58 °.
Jednak ten rozkład występuje w dwóch etapach: najpierw uwolniona jest cząsteczka NH3, wytwarzanie wodorowęglanu amonu (NH4HCO3); A po drugie, jeśli ogrzewanie będzie się utrzymywało, węglan jest nieproporcja.
Jest to solidny rozpuszczalny w wodzie i mniej rozpuszczalny w alkoholu. Tworzą mosty wodorowe z wodą, a gdy 5 gramów rozpuszcza się w 100 gramach wody, wytwarza podstawowe rozwiązanie o pH około 8,6.
Może ci służyć: emulgator: proces emulsji, aspekty molekularne, zastosowaniaJego wysokie powinowactwo do wody jest wytwarzane przez higroskopowe ciało stałe (pochłania wilgoć) i dlatego trudno ją znaleźć w postaci bezwodnej. W rzeczywistości jego monohydrat (NH4)2WSPÓŁ3· H2O), jest najczęstsze ze wszystkich i wyjaśnia, w jaki sposób sól jest nośnikiem gazu amoniaku, powodując zapach.
W powietrzu rozkłada się w celu wytworzenia wodorowęglanu amonu i węglanu amonu (NH4NH2WSPÓŁ2).
Struktura chemiczna
 Model struktury węglanu amonu; Dwa kation amonu i jeden węglan
Model struktury węglanu amonu; Dwa kation amonu i jeden węglan Na górnym obrazie zilustrowano strukturę chemiczną węglanu amonu. Na środku jest anion32-, płaski trójkąt z czarnym środkiem i czerwonymi kulami; I po dwóch stronach kationów Ammonios NH4+ z geometrią czworościenną.
Geometrię jonów amonowych wyjaśniono hybrydyzacją SP3 atomu azotu, zamawianie atomów wodoru (białe kule) wokół niego w postaci czworościanu. Wśród trzech jonów ustala się przez mosty wodorowe (h3N-H-O-CO22-).
Dzięki jego geometrii, pojedynczej co -sanion32- może utworzyć do trzech mostów wodoru; podczas gdy kationów NH4+ Być może nie mogą utworzyć swoich odpowiadających czterech mostów wodorowych z powodu odpychania elektrostatycznego wśród ich dodatnich ładunków.
Rezultatem wszystkich tych interakcji jest krystalizacja układu ortorombowego. Dlaczego jest tak higroskopowy i rozpuszczalny w wodzie? Odpowiedź jest w tym samym poprzednim akapicie: mosty wodorowe.
Te interakcje są odpowiedzialne za szybkie wchłanianie wody bezwodnej soli (NH4)2WSPÓŁ3· H2ALBO). Powoduje to zmiany w rozmieszczeniu przestrzennym jonów, a zatem w strukturze krystalicznej.
Może ci służyć: chlorek niklu (NICL2): struktura, właściwości, uzyskiwanie, użyciaKurosi strukturalne
Bez względu na to, jak proste (NH wygląda4)2WSPÓŁ3, Jest tak wrażliwy na niezliczone transformacje, że jego struktura jest tajemnicą poddaną prawdziwej składu stałego. Ta struktura zmienia się również w zależności od ciśnień, które wpływają na kryształy.
Niektórzy autorzy odkryli, że jony są uporządkowane jako koplanare wyłożone mostami wodorowymi (to znaczy łańcuch z sekwencją NH4+-WSPÓŁ32--…) W których cząsteczki wody prawdopodobnie służą jako złącza do innych łańcuchów.
Co więcej, przekraczając niebo ziemskie, w jaki sposób te kryształy w warunkach przestrzennych lub międzygwiezdnych? Jakie są twoje kompozycje pod względem stabilności gatunków gazowanych? Istnieją badania, które potwierdzają dużą stabilność tych kryształów uwięzionych w masach lodowych planetarnych i kometowych.
To pozwala im służyć jako rezerwy węgla, azotu i wodoru, które, odbierające promieniowanie słoneczne, można przekształcić w materiał organiczny, taki jak aminokwasy.
To znaczy, te lody amoniakalne mogą być nośnikami „koła, które rozpoczyna maszynę życia” w kosmosie. Z tych powodów wzrasta ich zainteresowanie astrobiologią i biochemią.
Używa/aplikacje
Jest stosowany jako leuers, ponieważ podgrzewanie wytwarza dwutlenek węgla i gazy amonu. Węglan amonu jest, jeśli chcesz, prekursor nowoczesnego proszku do pieczenia i może być używany do pieczenia ciasteczek i płaskich herbatników.
Jednak jego użycie do pieczenia ciast nie jest zalecane. Ze względu na grubość ciast gazy amonu są zatrzymywane w środku i wytwarzają nieprzyjemny smak.
Może ci służyć: cyklohexen: struktura, właściwości, synteza i zastosowaniaJest używany jako wykrztuśny, to znaczy łagodzącym kaszle. Ma działanie fungicydu, wykorzystując z tego powodu w rolnictwie. Jest także regulatorem kwasowości obecnej w żywności i jest stosowany w organicznej syntezy mocznika w wysokich ciśnieniach i Hidantoinas.
Ryzyko
Węglan amonu jest wysoce toksyczny. U ludzi wytwarza ostre podrażnienie jamy ustnej podczas skontaktowania się.
Ponadto, jeśli zostanie spożyty, powoduje podrażnienie żołądka. Podobne działanie obserwuje się w oczach narażonych na węglan amonowy.
Wdychanie gazów rozkładu soli, może podrażniać nos, gardło i płuca, powodując kaszel i niewydolność oddechową.
Ostra ekspozycja na psa na ammonatu w dawce 40 mg/kg masy, powoduje wymioty i biegunkę. Najwyższe dawki węglanu amonu (200 mg/kg masy) są zwykle śmiertelne. Uszkodzenie serca jest wskazane jako przyczyna śmierci.
Jeśli jest ogrzewany w bardzo wysokich temperaturach i w powietrzu wzbogaconym tlenem, wydziela toksyczne gazy2.
Bibliografia
- Pubchem. (2018). Węglan amonu. Pobrano 25 marca 2018 r. Z Pubchem: Pubchem.NCBI.NLM.Nih.Gov
- Portal chemii organicznej. ((2009-2018)). Reakcja Bucherer-Bergsa. Pobrano 25 marca 2018 r. Z portalu chemii organicznej: WWW.Chemia organiczna.org
- Wikipedia. (2018). Węglan amonu. Pobrano 25 marca 2018 r. Z Wikipedii: w.Wikipedia.org
- Firma chemiczna. (2018). Firma chemiczna. Pobrano 25 marca 2018 r. Z firmy chemicznej: Thechemco.com