Formacja karbokacji, cechy, typy, stabilność
- 3260
- 136
- Gabriela Łuczak
A karbokacja, Jak sama nazwa wskazuje, jest to jon organiczny, który ma dodatnio obciążony atom węgla, który charakteryzuje się wysoce niestabilnym, istniejącym przez krótki czas. Zazwyczaj jest to pośrednie w reakcjach organicznych, to znaczy powstaje jako niezbędne etapy odpowiednich mechanizmów molekularnych.
Historycznie istniały punkty konfliktu w kompresji tego, czym jest karbokacja. Wynika to z faktu, że istnieją symfiny cząsteczek reaktywnych, które z jakiegoś powodu nabierają dodatniego obciążenia w jednym ze swoich węgli. Klasyczna karbokacja, że tak powiem, jest taki, który może być reprezentowany przez ogólną formułę obrazu poniżej.
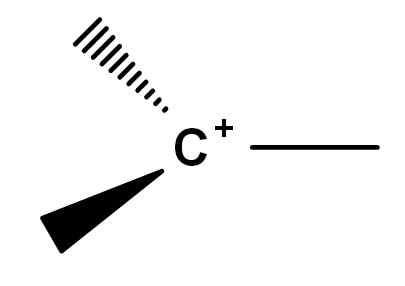 Ogólna formuła karbokacji. Źródło: Gabriel Bolívar.
Ogólna formuła karbokacji. Źródło: Gabriel Bolívar. Zwróć uwagę, w jaki sposób obciążenie dodatnie znajduje się dokładnie na atomie węgla, a także brakuje mu linku. Dlatego karbokacja jest słabymi elektronami, a to jest przyczyną jego wysokiej reaktywności.
Załóżmy, że metan, cho4. Gdyby węgiel stracił jeden z jego atomów wodoru, wyeliminowalibyśmy jedno z czterech wiązań C-H. Następnie powstało karbokacja metylowa, CH3+, które moglibyśmy reprezentować po prostu umieszczanie atomów wodoru na końcach pasków górnego wzoru. Ch3+ Jest to najprostsze ze wszystkich karbokacji.
[TOC]
Szkolenie
Jak powstają karbokacje? Odpowiedź znajduje się w mechanizmach reakcji. Jednak zdecydowana większość podział wspólnego jednego z dwóch następujących aspektów:
-Zerwanie heterolityczne
-Dodanie elektronów π do elektrofil
Zerwanie heterolityczne
W heterolitycznym pęknięciu wiązania C-G, g są dowolnym atomem lub grupą, jest one rozbite w nierówny sposób: elektrony wiązania pozostają g, podczas gdy atom węgla nabywa obciążenie dodatnie. Na przykład:
Może ci służyć: arsen: historia, struktura, właściwości, użycia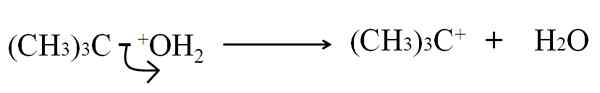 Pęknięcie heterolityczne w odwodnienie tertbutanolowym. Źródło: Gabriel Bolívar.
Pęknięcie heterolityczne w odwodnienie tertbutanolowym. Źródło: Gabriel Bolívar. Teraz ta przerwa może być podana dla kilku metod, co z kolei zmieni rozważany mechanizm i reakcję.
Dodanie elektronów π do elektrofil
Innym procesem, w którym powstaje karbokacja, jest bardzo powszechna w aromatycznych alkenach i związkach, jest atakowanie elektronów podwójnego wiązania z elektrofilem. Najczęstsze przypadki to uwodornienie alkenów poprzez działanie kwasu:
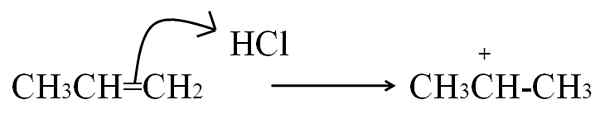 Reakcja HCl z propenem w celu utworzenia karbokacji jako pośredniej. Źródło: Gabriel Bolívar.
Reakcja HCl z propenem w celu utworzenia karbokacji jako pośredniej. Źródło: Gabriel Bolívar. Równanie to odpowiada tworzeniu się karbokacji, które to jest pośrednik, Nie jest produktem. Elektrony z podwójnym wiązaniem atakują wodór HCl, elektrofil. Wodór jest dodawany do węgla po prawej stronie podwójnego wiązania, dzięki czemu powstaje grupa3, Podczas gdy węgiel po lewej nabywa obciążenie dodatnie.
Charakterystyka
Hybrydyzacja
Ogólna formuła przedstawiona na początku ujawnia trygonalną płaską geometrię wokół atomu węgla. Wynika to z hybrydyzacji cierpiącej z powodu orbitali atomowych węgla, aby stać się hybrydowymi orbitaliami SP2, które są oddzielone pod kątem 120º. Chociaż nie jest reprezentowany, karbokacja ma orbital P Czysty i pusty, zdolny do przyjmowania elektronów.
Kwasowość
Karbokacja jest gatunkiem kwaśnym, albo zgodnie z definicją Brönsted lub Lewis. Podane są elektrony dodatniego ładunku lub atomy wodoru. Z tego powodu karbokacje nie mogą być utworzone w bardzo podstawowych mediach, ponieważ natychmiast zareagowałyby na przyczynę innych produktów.
Stabilność
Hybrydyzacja sp2 karbokacji sprawia, że podatne na ataki bogatych gatunków w elektrony. Ta funkcja jest dodatkowo podkreślona przez jej wielką kwasowość. W konsekwencji karbokacja jest gatunkiem bardzo reaktywnym, który prawie nie powstaje i wkrótce (w kwestii nanosekund) reaguje, aby powstać prawdziwy produkt reakcji chemicznej.
Może ci służyć: kwas sulfamowy: struktura, właściwości, synteza, zastosowaniaRodzaje karbokacji
Istnieje kilka rodzajów karbokacji. Można je jednak zaklasyfikować w następujący sposób:
-Podstawowy
-Wtórny
-Trzeciorzędowy
-Aromatyczne lub arillos
-Winyl i alili
Podstawowy
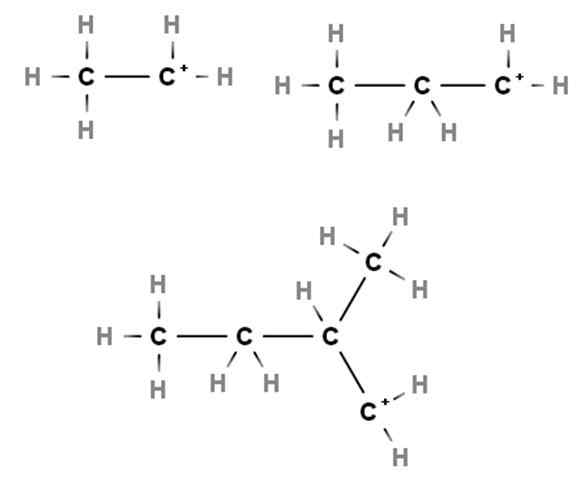 Podstawowe karbokacje. Źródło: Gabriel Bolívar przez Molview.
Podstawowe karbokacje. Źródło: Gabriel Bolívar przez Molview. Przybysze pokazują przykłady pierwotnych karbokacji. Nazywane są tym, ponieważ obciążenie dodatnie leży w węglu pierwotnym, 1st, więc jest ono powiązane tylko z atomem węgla. Etano, rozdz3Ch3, Kiedy H traci którykolwiek z końca, karbokacja Cho3Ch2+ albo +Ch2Ch3.
Wtórny
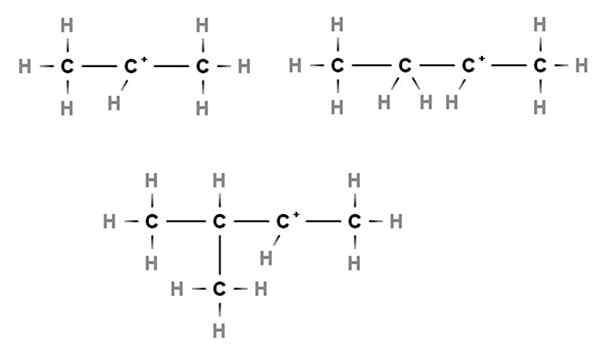 Wtórne karbokacje. Źródło: Gabriel Bolívar przez Molview.
Wtórne karbokacje. Źródło: Gabriel Bolívar przez Molview. W wtórnych karbokacjach obciążenie dodatnie znajduje się w węglu wtórnym, 2, co jest powiązane z dwoma atomami węgla. Na przykład, jeśli propan, cho3Ch2Ch3, Zabieramy H z centralnego węgla, będziemy mieli karbokacja Cho3Ch2+Ch3.
Trzeciorzędowy
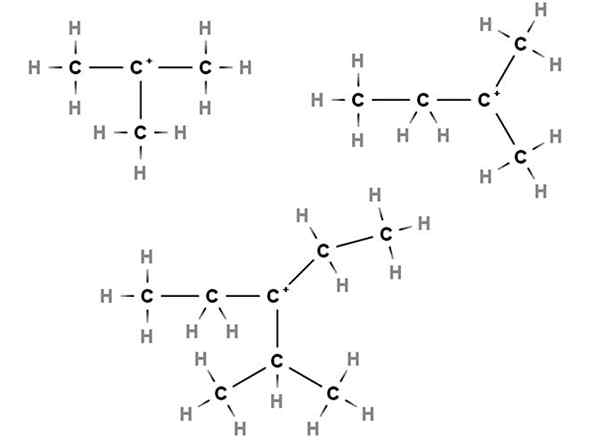 Karbokacje trzeciorzędowe. Źródło: Gabriel Bolívar przez Molview.
Karbokacje trzeciorzędowe. Źródło: Gabriel Bolívar przez Molview. W karbokacjach trzeciorzędowych obciążenie dodatnie znajduje się w węglu trzeciego. Zauważ, że w przeciwieństwie do dwóch pierwszych rodzajów karbokacji, brakuje im atomów wodoru.
W ten sposób mamy metylopropan lub izobutan, ch (CH (wybierz3)3, Co przez utratę wodoru węgiel centralny tworzy karbokokację +C (rozdz3)3.
Aromatyczny
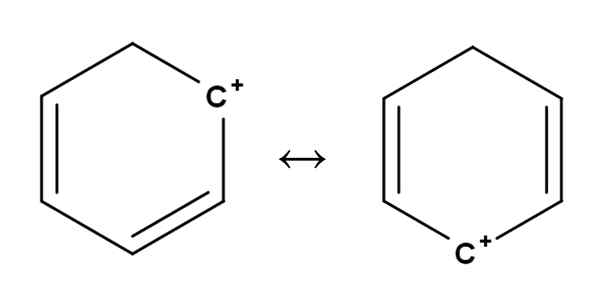 Benzen Carbocat. Źródło: Gabriel Bolívar.
Benzen Carbocat. Źródło: Gabriel Bolívar. Aromatyczne lub aromatyczne karbokacje są prawdopodobnie najbardziej wyjątkowe ze wszystkich. Twój trening jest bardzo podobny do opisanego dla alkenów w pierwszej sekcji.
W nich obciążenie dodatnie znajduje się w zasadzie w jednym z węgli aromatycznego pierścienia, takiego jak benzen. Jednak obciążenie dodatnie nie jest ustalone, ale jest rozproszone w innych pozycjach pierścienia według rezonansu.
Może ci służyć: rybulosa-1,5-bifosforan (RUBP): Charakterystyka, karboliksacjaW ten sposób obciążenie dodatnie, jak widać powyżej, przechodzi z jednego węgla do drugiego wewnątrz pierścienia benzenu. Ta cecha zapewnia tę karbokacji wielką stabilność wobec innych rodzajów karbokacji.
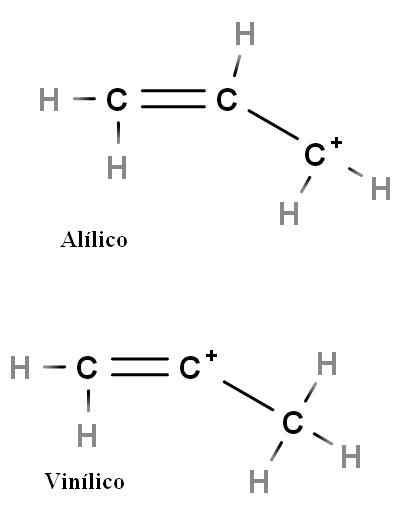
Allile i winyl
 Karbokacja alliiowa i winylowa. Źródło: Gabriel Bolívar.
Karbokacja alliiowa i winylowa. Źródło: Gabriel Bolívar. Inne specjalne typy karbokacji to alili i winyl. Różnica między nimi (powyżej) polega na pozycji ładunku dodatniego związanego z podwójnym wiązaniem.
W karbokacji winylowej obciążenie dodatnie występuje w jednym z węgli z podwójnym wiązaniem; Podczas karbokacji sojuszniczej obciążenie dodatnie znajduje się w węglu po podwójnym wiązaniu. Wystarczy zastąpić hydrogenów innymi grupami, a my będziemy mieli ogromną rodzinę karbokacji sojusznych i winylowych.
Stabilność względna
Wiedząc, które są głównymi rodzajami karbokacji, można je zamówić na podstawie ich względnej stabilności:
Płyta winylowa < Primario < Secundario < Alílico < Terciario < Aromático
Teraz mogą istnieć allowe karbokacje, które są bardziej stabilne niż określony trzeciorzędny. Wszystko będzie zależeć od ich podstawników.
Dlaczego ta stabilność? Do zdolności cząsteczki do rozproszenia lub zmniejszania dodatniego obciążenia karbokacji. Aby to zrobić, potrzebujesz bliskich atomów, które dają część jego elektronicznej gęstości karbokacji przez hiperkonjugację. Tymczasem w karbokacjach aluminiowych i aromatycznych osiąga się to przez rezonans.
W przypadku karbokacji winylowej obciążenie dodatnie znajduje się na węglu, który był już sp2, co czyni go bardzo niestabilnym.
Bibliografia
- Graham Solomons t.W., Craig b. Fryhle. (2011). Chemia organiczna. (10th Wydanie.). Wiley Plus.
- Carey f. (2008). Chemia organiczna. (Szósta edycja). MC Graw Hill.
- Morrison i Boyd. (1987). Chemia organiczna. (Piąta edycja). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Karbokacja. Źródło: w:.Wikipedia.org
- James Ashenhurst. (20 lutego 2020). 3 czynniki, które stabilizują karbokacje. Odzyskane z: MastorganicChemistry.com
- Clark Jim. (2000). Karbokacje (lub jony karbonowe). Odzyskane z: chemguide.współ.Wielka Brytania
- Dr. Kennepohl, prof. S. Farmer & T. Soderberg. (10 sierpnia 2020). Struktura i stabilność karbokacji. Chemia librettexts. Odzyskane z: chem.Librettexts.org

