Struktura, właściwości i zastosowania Butanone
- 1364
- 371
- Eliasz Dubiel
Butanone Jest to związek organiczny, w szczególności keton, którego wzorem chemicznym jest Cho3Ch2Coch3. Jego wygląd jest wyglądem bezbarwnej cieczy używanej zasadniczo jako rozpuszczalnik. Ma podobny do właściwości acetonu, ale gotuje się w wyższej temperaturze i odparowuje wolniej.
Jest wytwarzany przez katalityczne odwodornienie 2-butanolu (związek chiralny). Jest jednak w stanie naturalnym w składzie niektórych owoców. Jest częścią emanacji rur wydechowych pojazdów i jest składnikiem dymu tytoniu.
 Cząsteczka Butanone. Źródło: Pixabay.
Cząsteczka Butanone. Źródło: Pixabay. Jest po acetonie najprostszy z tej rodziny związków organicznych. Butnonone powoduje podrażnienie w oczach i nosie. W niezwykle wysokiej dawce może powodować podrażnienie błony śluzowej płucnej. Z drugiej strony płyn ten jest uważany za czynnik prekursorowy narkotyków.
Butanone ma wielką rozpuszczalność w wodzie; Ale jest również bardzo rozpuszczalny w rozpuszczalnikach organicznych, takich jak etanol, eter, aceton, benzen i chloroform. Można to wyjaśnić, ponieważ jego wartość dziennika P (0,29) dla współczynnika podziału oktanowego/wody jest niski.
[TOC]
Struktura butanonowa
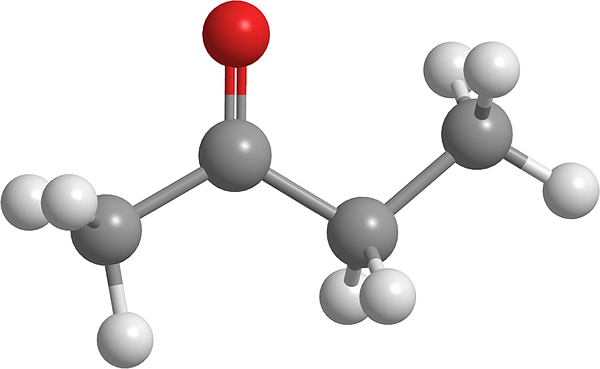
Na górnym obrazie cząsteczka butanonu jest pokazana za pomocą modelu sfery i słupków. Atom tlenu grupy karbonylowej (czerwona kula) można zobaczyć w drugim węglu. Ta grupa, C = O, jest odpowiedzialna za nadanie stałego momentu dipolowego do cząsteczki.
Butanone, widok strukturalny, jest niczym więcej niż acetonem, do którego dodano grupę metylenową, CH2. Posiadanie większej ilości węgli, moment dipolowy jest mniejszy w porównaniu z momentem acetonu; Ale jego największa masa cząsteczkowa powoduje, że gotuje się w wyższej temperaturze.
Ta cząsteczka, podobnie jak inne ketony, nie ma możliwości tworzenia mostów wodorowych; I dlatego ich interakcje dipol-dipolo nie są tak silne.
Może ci służyć: emulgator: proces emulsji, aspekty molekularne, zastosowaniaDlatego jest to lotna ciecz. Gdy temperatura spada (-86,6 ° C), jego słabe dipole to te, które prowadzą ich cząsteczki w celu utworzenia kryształu. Oprócz tego można również skomentować, że Butanone jest strukturalnie asymetryczny.
Nieruchomości
Formuła molekularna
C4H8Lub Ch3Coch2Ch3
Nazwy
- Butanone.
- 2-butanon.
- Butan -2 -ona.
- Methil Ethil Cetona.
Masa cząsteczkowa
72,107 g/mol.
Opis fizyczny
Bezbarwny płyn.
Zapach
Pachnący do mięty, umiarkowanie silny.
Punkt wrzenia
79,59 ºC przy 760 mmHg.
Temperatura topnienia
-86.6 ° C.
punkt zapłonu
-9 ° C (zamknięty kubek).
Rozpuszczalność wody
29 g /100 ml w 20 ° C. Podczas gdy jego moment dipolowy jest mniejszy niż w przypadku acetonu, nadal może oddziaływać w doskonałym stopniu z cząsteczkami wody. Od nich otrzymuje mosty wodorowe: (CH3) (Rozdz2Ch3) C = o-hah. Z tego powodu jest bardzo rozpuszczalne w wodzie.
Rozpuszczalność w rozpuszczalnikach organicznych
Rozpuszczalne w benzenie, alkoholu i eterze; Mamiczne z olejami, etanolem, eterem, acetonem, benzenem i chloroformem. Zauważ, że Butanone jest rozpuszczalny w szerokiej gamie rozpuszczalników.
Gęstość
0,7997 g/cm3 w 25 ° C.
Gęstość pary
2,41 (w stosunku do wody = 1).
Ciśnienie pary
90,6 mmHg w 25 ° C.
Współczynnik podziału oktanol/wodę
Log p = 0,29
Temperatura samowystarczalności
505 ° C.
Rozkład
Rozkłada się przez procesy fotochemiczne przez utlenianie przez wolne rodniki hydroksylowe. Po podgrzaniu do rozkładu emituje akr dym.
Breja
0,40 cpoise w 25 ° C.
Ciepło spalania
2.444,1 kJ/mol w 25 ° C.
Ciepło parowe
31,30 kJ/mol w punkcie wrzenia; i 34,79 kJ/mol w 25 ° C.
Może ci służyć: ogólne prawo gazoweNapięcie powierzchniowe
23,97 mn/m 25 ºC.
Potencjał jonizacji
0,54 eV.
Zapach próg
Niski zapach: 0,735 mg/m3.
Wysoki zapach: 147,5 mg/m3.
Współczynnik załamania światła
1788 do 20 ° C.
Stała dysocjacji
PKA = 14,70.
Stabilność
Stabilny, ale wysoce łatwopalny. Niezgodne z środkami utleniającymi, podstawami i silnymi środkami redukującymi. Należy unikać wilgoci.
Aplikacje
Rozpuszczalnik
Butanone jest używany jako rozpuszczalnik w opracowywaniu powłok powierzchniowych, produkcji pyłu bezdymnego, opracowywaniu kolorowych żywic oraz w eliminacji akumulacji tłuszczu wytwarzanej przez smary.
Ponadto jest używany w opracowaniu:
- Sztuczna skóra.
- Gomas.
- Lacas.
- Lakiery.
- Klej.
- Rozpuszczalniki.
- Painowe stawki.
- Kleje.
- Plastikowe cementy.
- Uszczelniacze.
- Taśmy magnetyczne.
- Przezroczysty papier.
- Drukuj atramenty.
- Kosmetyki i produkty farmaceutyczne.
Jest również stosowany jako rozpuszczalnik do defaracji powierzchni metalowych, urządzeń elektronicznych i ekstrakcji tłuszczu. Służy do ekstrakcji twardego drewna i oleju roślinnego.
Jest to obojętne składniki w opracowaniu pestycydów oraz w produkcji azotanu octanu i celulozowego.
Jest stosowany jako rozpuszczalnik ekstrakcyjny w przetwarzaniu żywności i składnikach żywności; Na przykład w frakcjonowaniu tłuszczów i olejków, a także w procesie bezkofeinowym kawy. Jest również używany jako rozpuszczalnik w markerach używanych na białych płytach.
Odczynnik
- Butanone jest używany jako fotoinicyator rozpuszczalny w wodzie.
- Skrapla się za pomocą formaldehydu w celu wytworzenia ketonu izopropenilu.
- Doświadczyć autokodensacji do produkcji etylowo -amylo -cetona.
- Reaguje z Cytral, aby uzyskać komponenty perfum, takie jak metylopseudoionon.
Może ci służyć: ciepło reakcyjne- Interweniuje jako katalizator w produkcji hydractyny.
- Dodatkowo jest prekursorem nadtlenku metylu etylowego, który jest katalizatorem niektórych reakcji polimeryzacji.
Cement z tworzywa sztucznego
Butanone ma zastosowanie jako plastikowy środek spawalniczy, z zastosowaniem w montażu modeli skali polistyrenu. Butnonone rozpuszcza polistyren, umożliwiając przyłączenie krawędzi, gdy nastąpi nowa polimeryzacja. To zachowanie jest cementem, a nie kleju.
Inne zastosowania
Butanone jest stosowany jako sterylizator zarodników bakterii w instrumentach chirurgicznych, igiełach, wtryskiwaczy podskórnych i instrumentach dentystycznych.
Jest stosowany jako środek aromatyzujący żywność w bardzo niskich stężeniach; Na przykład w napojach alkoholowych stężenie wynosi 20 ppm; w produktach pieczonych, 12,7 ppm; Mięso mają około 26,5 ppm; guma do żucia, 0,63 ppm; oraz w tłuszczach i olejkach, 1,0 ppm.
I wreszcie butanon jest używany w oddzieleniu apoproteiny grupy hemoproteinowej w hemoproteinach.
Bibliografia
- Morrison, r. T. i Boyd, R, N. (1987). Chemia organiczna. 5ta Wydanie. Redakcja Addison-Wesley Inter-American.
- Carey f. (2008). Chemia organiczna. (Szósta edycja). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Chemia organiczna. Aminy. (10thWydanie.). Wiley Plus.
- National Center for Biotechnology Information. (2019). Baza danych pubchem metylowego ketonu. CID = 6569. Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov
- Wikipedia. (2019). Butanone. Źródło: w:.Wikipedia.org
- Royal Society of Chemistry. (2015). Butanone. Chemspider. Odzyskany z: Chemspider.com
- Arlem Cheprasov. (2019). Co to jest Butanone? Formuła i użycie. Badanie. Odzyskane z: Study.com
- Ben Verve. (17 maja 2017 r.). Butanone. Świat chemii. Odzyskane z: ChemistryWorld.com

