Struktura pompy sodu potasu, funkcja, mechanizm, znaczenie
- 1577
- 117
- Pani Waleria Marek
Bomba sodu potasu Jest to struktura białka zawarta w szerszym zestawie cząsteczek obecnych w wielu błonach komórkowych i które są odpowiedzialne za aktywny transport jonów lub innych małych cząsteczek przeciwko jego gradientom stężenia. Wykorzystują energię uwalnianą przez hydrolizę ATP i dlatego są ogólnie nazywane Atasas.
Pompa sodowa potasu jest atpay Na+/K+, ponieważ uwalnia energię zawartą w cząsteczce ATP, aby przesunąć sód wewnątrz komórki, wprowadzając jednocześnie potas potasowy.
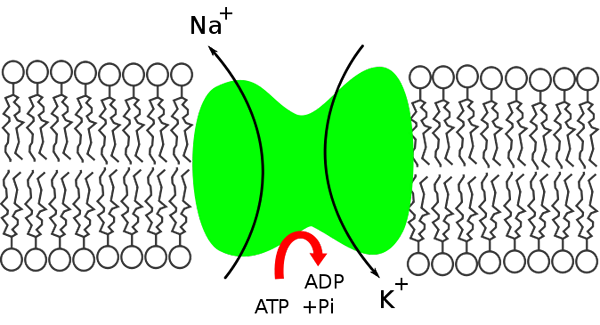
 Schemat bomby sodu potasu. Zewnętrzny i wnętrza komórki. (Źródło: Miguelferig, Via Wikimedia Commons)
Schemat bomby sodu potasu. Zewnętrzny i wnętrza komórki. (Źródło: Miguelferig, Via Wikimedia Commons) Wewnątrz komórki sód jest mniej skoncentrowany (12 meq/l) niż na zewnątrz (142 MEQ/L), podczas gdy potas jest bardziej skoncentrowany na zewnątrz (4 meq/l) niż wewnątrz (140 MEQ/L).
Bomby Atasas są podzielone na trzy duże grupy:
- Pompy jonowe typu F i V: Są dość złożonymi strukturami, mogą składać się z 3 różnych rodzajów podjednostek transmarketowych i do 5 powiązanych polipeptydów w cytosolu. Działają jako transportery protonowe.
- ABC nadrodzina (z angielskiego DOTP-BInding CAsette = Kasetę Unii ATP): Zintegrowany przez ponad 100 białek, które mogą funkcjonować jako przenośniki jonowe, monosacharydy, polisacharydy, polipeptydy i nawet inne białka.
- Pompy jonowe klasy P: utworzone przez co najmniej jedną transmembraalną podjednostkę katalityczną alfa, która ma miejsce związkowe dla ATP i niewielką podjednostkę β. Podczas procesu transportu podjednostka α to fosforyla, a zatem jego nazwa „P”.
Bomba sodowa potasu (Na+/K+ATPASA) należy do grupy pomp jonowych klasy P i została odkryta w 1957 r. Przez Jensa Skou, duńskiego badacza, kiedy badał mechanizm działania znieczulenia w nerwach kraba (Carcinus maenas); Prace, za które Nagroda Nobla w dziedzinie chemii została przyznana w 1997 roku.
 Bomba sodu potasu. Nakpompe2.JPG: Phi-gastrein w zimnie.Praca Wikipediderivative: Sonia/cc by-S (http: // creativeCommons.Org/licencje/by-sa/3.0/)
Bomba sodu potasu. Nakpompe2.JPG: Phi-gastrein w zimnie.Praca Wikipediderivative: Sonia/cc by-S (http: // creativeCommons.Org/licencje/by-sa/3.0/) [TOC]
Struktura pompy sodu potasu
Pompa sodowa potasu jest enzymem, który z punktu widzenia jej struktury czwartorzędowej powstaje przez 2 podjednostki białkowe Alfa (α) i dwa typ typu beta (β).
Jest to zatem tetramer typu α2β2, którego podjednostki są kompleksowymi białkami błonowymi, to znaczy przecinają dwuwarstwę lipidową i mają zarówno domeny wewnątrz i dodatkowej cytosolicznej.
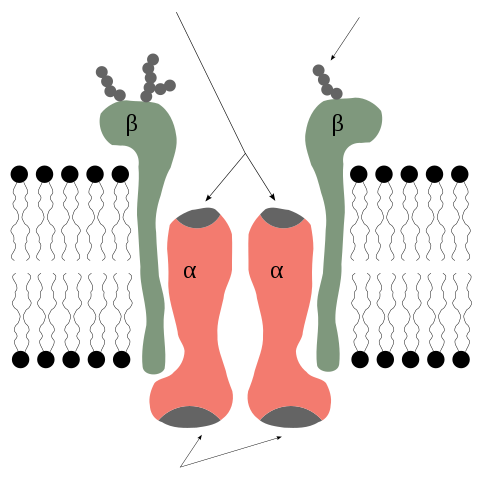 Podjednostki alfa i beta pompy potasowej. Rob Cowie/cc by-SA (http: // creativeCommons.Org/licencje/by-sa/3.0/)
Podjednostki alfa i beta pompy potasowej. Rob Cowie/cc by-SA (http: // creativeCommons.Org/licencje/by-sa/3.0/) Podpowszechności alfa
Podjednostki α to te, które zawierają miejsca związkowe dla ATP i dla jonów Na+ i K+ i reprezentują komponent katalityczny enzymu i ten, który wywiera funkcję samej bomby samej.
Podjednostki α są polipeptydami o dużych rozmiarach o masie cząsteczkowej 120 kDa, 10 segmentów transbranowych i ich końcówek N-C-końcowych położonych po stronie cytozolowej.
Mają w wewnątrzkomórkowym bocznym stanowisku związkowym dla ATP i dla Na+, a także resztę asparaginianową w pozycji 376, która reprezentuje miejsce, w którym cierpiał proces fosforylacji podczas aktywacji pompy.
Miejsce wiązania K+ jest najwyraźniej po stronie zewnątrzkomórkowej.
Podjednostki beta
Podjednostki β nie wydają się mieć bezpośredniego udziału w funkcji pompowania, ale przy ich nieobecności nie występuje funkcja.
Podjednostki β mają masę cząsteczkową około 55 kDa każda i są glikoproteinami o pojedynczej domenie transmarketowej, której odpady glucydy są wstawiane w obszarze zewnątrzkomórkowym.
Może ci służyć: arkusz podstawowy: Charakterystyka, histologia i funkcjeWydaje się, że są konieczne w retikulum endoplazmatycznym, gdzie przyczyniłyby się do właściwego fałdowania podjednostek α, a następnie, na poziomie błony, aby ustabilizować kompleks.
Oba typy podjednostek są heterogeniczne i zostały opisane do tej pory izoformy α1, α2 i α3 dla Una i β1, β2 i β3 dla drugiego. Α1 występuje w błonach większości komórek, podczas gdy α2 jest obecny w mięśniach, sercu, tkance tłuszczowej i mózgu oraz α3 w sercu i mózgu.
Izoforia β1 jest najbardziej rozproszonym rozkładem, chociaż nie ma w niektórych tkankach, takich jak komórki przedsionkowe ucha wewnętrznego i szybkie komórki mięśni glikolitycznych. Ten ostatni zawiera tylko β2.
Różne struktury podjednostek, które tworzą pompę Na+/K+ w różnych tkankach, mogą przestrzegać specjalizacji typu funkcjonalnego, a jednocześnie wyjaśnione.
Funkcja pompy potasowej
W dowolnym momencie membrana plazmatyczna stanowi granicę separacji między odpowiadającym przedzia.
Oba przedziały mają skład, który może być jakościowo różny, ponieważ wewnątrz komórek istnieją substancje, które nie są z nich poza nimi, a płyn pozakomórkowy zawiera substancje, które nie są obecne wewnątrzkomórkowo.
Substancje obecne w obu przedziałach można znaleźć w różnych stężeniach, a różnice te mogą mieć znaczenie fizjologiczne. Tak jest w przypadku wielu jonów.
Konserwacja homeostazy
Pompa Na+/K+ wypełnia fundamentalną funkcję w utrzymaniu homeostazy wewnątrzkomórkowej poprzez kontrolowanie stężeń sodu i jonów potasowych. To utrzymanie homeostazy osiąga to dzięki:
- Transport jonowy: wprowadza jony sodu i wydala jony potasowe, proces, przez który promuje również ruch innych cząsteczek przez inne transportery, które zależą od ładunku elektrycznego lub wewnętrznego stężenia tych jonów.
- Kontrola objętości komórki: Wprowadzenie lub wyjście jonów implikuje również ruchy wody zębowej komórki, więc pompa uczestniczy w kontroli objętości komórek.
- Pokolenie potencjału błony: Wyrzucenie 3 jonów sodu na każde 2 wprowadzone jony potasu powoduje błonę. Ta różnica jest znana jako potencjał odpoczynku.
Na+ ma stężenie zewnątrzkomórkowe około 142 meq/l, podczas gdy jego stężenie wewnątrzkomórkowe wynosi tylko 12 meq/l; Z drugiej strony K+jest bardziej skoncentrowane w komórce (140 MEQ/L) niż na zewnątrz (4 meq/l).
Chociaż ładunek elektryczny tych jonów nie pozwala na przejście przez membranę, istnieją kanały jonowe, które pozwalają (selektywnie), które sprzyjają ruchowi, jeśli siły, które zwykle poruszają te jony, są również obecne.
Może ci służyć: receptory membranowe: funkcje, typy, jak działająTeraz te różnice w koncentracji mają ogromne znaczenie w Ochrona homeostazy organizmu i musi być utrzymywany w rodzaju równowagi, która zostałaby utracona.
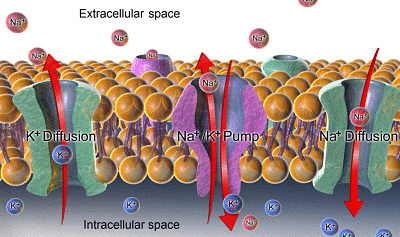 Rozpowszechnianie i sód potasu (źródło: Bruceblaus. Podczas korzystania z tego obrazu w źródłach zewnętrznych można go cytować jako: Blausen.Com Staff (2014). „Galeria medyczna Blausen Medical 2014”. Wikijournal of Medicine 1 (2). Doi: 10.15347/WJM/2014.010. ISSN 2002-4436.Pochodna autorstwa Mikael Häggström/cc autorstwa (https: // creativeCommons.Org/licencje/według/3.0) Via Wikimedia Commons)
Rozpowszechnianie i sód potasu (źródło: Bruceblaus. Podczas korzystania z tego obrazu w źródłach zewnętrznych można go cytować jako: Blausen.Com Staff (2014). „Galeria medyczna Blausen Medical 2014”. Wikijournal of Medicine 1 (2). Doi: 10.15347/WJM/2014.010. ISSN 2002-4436.Pochodna autorstwa Mikael Häggström/cc autorstwa (https: // creativeCommons.Org/licencje/według/3.0) Via Wikimedia Commons) - Różnica stężenia dla Na+ między wnętrzem i zewnętrzną komórką tworzy gradient chemiczny, który popycha sód do wewnątrz i sprawia, że jon ten nieustannie wchodzący i wyposażony w celu rozproszenia tej różnicy, to znaczy w celu dopasowania stężeń po obu stronach.
- Gradient potasu jest utrzymywany w przeciwnym kierunku, to znaczy od wewnątrz na zewnątrz, umożliwiając stałą moc wyjściową jonu i jego wewnętrzną redukcję i wzrost zewnętrzny.
Funkcja pompy Na+/K+ umożliwia ekstrakcję sodu, która wprowadziła dyfuzję przez kanały lub inne trasy transportowe oraz ponowne wprowadzenie potasu, który został rozpowszechniony na zewnątrz, umożliwiając ochronę stężeń wewnątrz i zewnątrzkomórkowych tych jonów.
Mechanizm (proces)
Mechanizm działania Na+/K+ składa się z cyklu katalitycznego, który implikuje reakcje przenoszenia grupy fosforylowej (PI) i zmiany konformacyjne enzymu, które przechodzą ze stanu E1 do stanu E2 i odwrotnie.
Operacja wymaga obecności ATP i Na+ wewnątrz komórki i K+ w płynie pozakomórkowym.
Związek jonów sodu z transporterem
Cykl rozpoczyna się w stanie konformacji E1 enzymu, w którym istnieją 3 miejsca cytozolowe unii Na+ i wysokie powinowactwo (km 0,6 mm), które są w pełni zajęte, ponieważ stężenie jonów (12 mm) pozwala na to.
Hydroliza ATP
W tym stanie (E1) i przy ustawionym Na+ w swoich miejscach związkowych, ATP jest ustalony do swojego miejsca w sektorze cytozolowym cząsteczki, grupa fosforanowa do 376 asparaganu jest przenoszona i przenoszona, tworzą Zmiana konformacyjna na stan E2.
Wydalenie 3 jonów sodu i wprowadzenie 2 jonów potasowych
Zmiana konformacyjna do stanu E2 oznacza, że miejsca Unii Na+ przechodzą do zagranicy, ich powinowactwo do jonu znacznie się zmniejsza i jest uwalniane w płynie pozakomórkowym, podczas gdy jednocześnie powinowactwo miejsc Unii do K+ wzrośnie A jony te wiążą się z pompą.
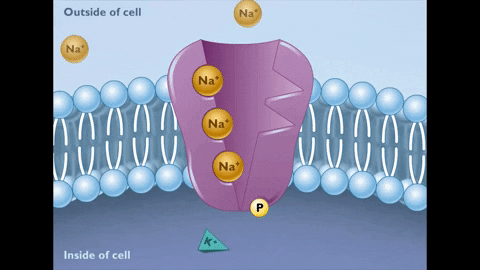 Podczas stanu E2 jony Na+ są uwalniane po drugiej stronie błony.
Podczas stanu E2 jony Na+ są uwalniane po drugiej stronie błony. 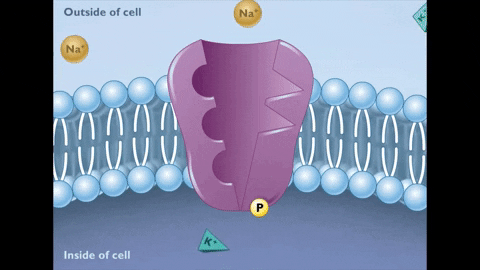 Z kolei ten nowy stan pompy generuje powinowactwo do związku Kotów K+
Z kolei ten nowy stan pompy generuje powinowactwo do związku Kotów K+ Odwrócenie od E2 do E1
Po uwolnieniu Na+ i zjednoczeniu K+, wytwarzana jest hydroliza fosforanu aspartyle, a zmiana konformacyjna stanu E2 na stan E1 jest odwrócony, z ponownym wprowadzeniem miejsc Unii dla pustego Na+ i okupowanego K+.
Kiedy nastąpi ta zmiana, miejsca dla Na+ odzyskują ich powinowactwo i k+ tracą, z którymi K+ jest uwalniane wewnątrz komórki.
Znaczenie
W utrzymaniu osmolarności komórki
Bomba Na+/K+ była obecna w większości, jeśli nie w ogóle, komórek ssaków, w których ma ogólne znaczenie, przyczyniając się do utrzymania swojej osmolarności, a tym samym objętości.
Może ci służyć: peroksydazy: struktura, funkcje i typyCiągłe wejście jonów sodowych do komórki uwarunkowało wzrost wewnątrzkomórkowej liczby cząstek osmotycznie aktywnych, co indukuje wejście wody i wzrost objętości, który ostatecznie spowodowałby pęknięcie membrany i zapadnięcia się komórki.
W tworzeniu potencjału błony
Ponieważ pompy te wprowadzają tylko 2 k+ na każde 3 Na+, które usuwają, zachowują się elektrogenicznie, co oznacza, że „dekompensują” wewnętrzne ładunki elektryczne, faworyzując wytwarzanie charakterystycznego potencjału błony komórek ciała.
Jego znaczenie jest również widoczne w odniesieniu do komórek tworzących pobudliwe tkanki, w których potencjały czynnościowe charakteryzują się wejściem jonu Na+, który depolaryzuje komórkę, oraz wyjście K+, które ją repolalizują.
Te ruchy jonowe są możliwe dzięki działaniu pomp Na+/K+, które przyczyniają się do wytwarzania gradientów chemicznych, które poruszają zaangażowane jony.
Bez tych pomp, które działają w przeciwnym kierunku, gradienty stężenia tych jonów rozproszyłyby się, a aktywność pobudzająca zniknęła.
W funkcji nerek
Innym aspektem, który podkreśla ekstremalne znaczenie bomb sodu-potasowych, jest funkcja nerek, co nie byłoby niemożliwe.
Funkcja nerek implikuje codzienną filtrację mniej więcej 180 litrów osocza i dużych ilości substancji, z których niektóre muszą być wydalane, ale wielu musi zostać wchłonięte, aby nie były utracone w moczu.
Resorpcja sodu, wody i wielu przefiltrowanych substancji zależy od tych pomp, które znajdują się w błonie podstawno -bocznej komórek, które tworzą nabłonek różnych segmentów rurowych nefronów nerek.
Komórki nabłonkowe, które podtrzymują kanaliki nerkowe, mają twarz, która jest w kontakcie ze światłem kanalików, która nazywa się wierzchołkową twarzą, a drugą, która jest w kontakcie z śródmiąższem wokół kanalików i nazywana bazolateralną.
Woda i substancje, które są wrzążne, muszą najpierw przejść do wnętrza komórki przez wierzchołek, a następnie do śródmiąższu przez podstawno -boczny.
Reabsorpcja Na+ jest kluczowa zarówno w stosunku do niego, jak i w stosunku do wody, jak i innych substancji, które zależą od jego. Wierzchołkowe wejście komórek Na+ wymaga, aby istniał gradient, który ją porusza i co oznacza bardzo niskie stężenie jonu wewnątrz komórki.
To niskie wewnątrzkomórkowe stężenie Na+ jest wytwarzane przez pompy sodowe z błony podstawno -bocznej, które intensywnie działają w celu usunięcia jonu z komórek do śródmiąższu.
Bibliografia
- Ganong WF: Ogólne i komórkowe podstawy fizjologii medycznej, w: Przegląd fizjologii medycznej, 25. edycja. Nowy Jork, McGraw-Hill Education, 2016.
- Guyton AC, Hall JI: Transport substancji przez błonę komórkową, w: Podręcznik fizjologii medycznej, 13th Ed, AC Guyton, Je Hall (red.). Philadelphia, Elsevier Inc., 2016.
- Lodish H, Berk A, Zipursky SL, Matsudaira P, Baltimore D, Darnell J: Transport przez błony komórkowe, w: Molecular and Cell Biology, 4th ed.
- Nelson, zm. L., Lehninger, a. L., & Cox, m. M. (2008). Zasady biochemii lehninger. Macmillan.
- Alberts, ur., Bray, d., Hopkin, k., Johnson, a. D., Lewis, J., Raff, m.,… I Walter, P. (2013). Niezbędna biologia komórki. Garland Science.
- « Charakterystyka soma części i funkcje
- Charakterystyka Mayat (Cotinis mutabilis), siedlisko, reprodukcja »

