Wodorowęglan wapnia

- 3163
- 243
- Prokul Woliński
 Wodorowęglan wapnia jest nieorganiczną solą z grupy wodorowęglanowej
Wodorowęglan wapnia jest nieorganiczną solą z grupy wodorowęglanowej Co to jest wodorowęglan wapnia?
On wodorowęglan wapnia Jest to sól nieorganiczna o wzorze chemicznym CA (HCO3)2. Pochodzi z natury z węglanu wapnia obecnego w wapie i kamieniach mineralnych, takich jak kalcyt.
Wodorowęglan wapnia jest bardziej rozpuszczalny w wodzie niż węglan wapnia. Ta funkcja pozwoliła na tworzenie systemów krasowych w skałach wapiennych i struktury jaskiń.
Wody gruntowe, które przecina pęknięcia, nasyca się przemieszczeniem dwutlenku węgla (CO2).
Wody te erodują wapienne skały uwalniające węglan wapnia (CACO3), że wodorowęglan wapnia powstanie, zgodnie z następującą reakcją:
Złodziej3(s) +co2(g) +h2Lub (l) => ca (hco3)2(aq)
Ta reakcja występuje w jaskiniach, w których pochodzą bardzo twarde wody. Wodorowęglan wapnia nie jest w stanie stałym, ale w roztworze wodnym, wraz z CA2+, Wodorowęglan (HCO3-) i jon węglanowy (co32-).
Następnie, poprzez zmniejszenie nasycenia dwutlenku węgla w wodzie, zachodzi odwrotna reakcja, to znaczy transformacja wodorowęglanu wapnia w węglan wapnia:
CA (HCO3)2(aq) => co2 (g) +h2Lub (l) +caco3 (S)
Węglan wapnia jest mało rozpuszczalny w wodzie, co powoduje, że jego wytrącanie występuje jako ciało stałe. Poprzednia reakcja jest bardzo ważna w tworzeniu stalaktytów, stalagmitów i innej grubości w jaskiniach.
Te skaliste konstrukcje powstają z kropli wody, które spadają z sufitu jaskini. Kako3 obecne w kroplach wody jest krystalizowane w celu utworzenia wyżej wymienionych struktur.
Fakt, że nie znalezienie wodorowęglanu wapnia w stanie stałym utrudnił jego zastosowanie, znalezienie kilku przykładów w tym zakresie.
Struktura wodorowęglanu wapnia
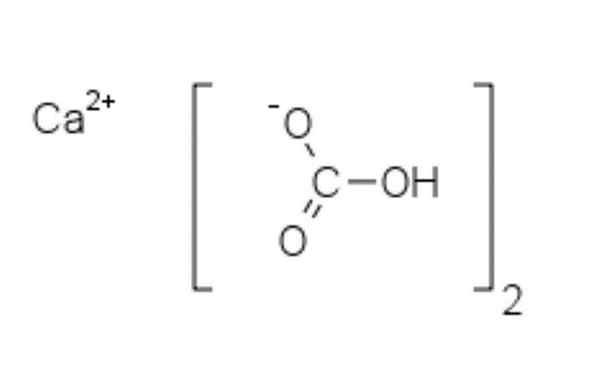 Struktura chemiczna wodorowęglanu wapnia
Struktura chemiczna wodorowęglanu wapnia Na górnym obrazie pokazano dwa aniony HCO3- i kation2+ interakcja elektrostatycznie. CA2+, Zgodnie z obrazem powinien znajdować się na środku, ponieważ tak HCO3- Nie odparły ze sobą za swoje negatywne opłaty.
Obciążenie ujemne w HCO3- Przenosi się między dwoma atomami tlenu, przez rezonans między grupą karbonylową C = O a łącznikiem C-O-; podczas gdy w CO32-, Jest to przeniesione między trzema atomami tlenu, ponieważ wiązanie C-O jest niezabezpieczone i może otrzymać ujemne obciążenie rezonansowe.
Może ci służyć: difenyloaminaGeometrie tych jonów można uznać za kulki wapnia otoczone płaskimi trójkątami węglanowymi z uwodornionym końcem. Pod względem współczynnika wielkości wapń jest niezwykle mniejszy niż jony HCO3-.
Wodne rozwiązania
Wodorowęglan wapnia Nie można tworzyć krystalicznych ciał stałych i naprawdę składa się z wodnych roztworów tej soli. W nich jony nie są same, jak na obrazie, ale otoczone cząsteczkami H2ALBO.
Każdy jon jest otoczony sfery nawodnienie, która będzie zależeć od metalu, polaryzacji i struktury rozpuszczonych gatunków.
CA2+ Koordynuje się z atomami tlenu wody, tworząc akwokompleks, CA (OH2)N2+, gdzie n zwykle uważa się za sześć; to znaczy „wodny oktaedron” wokół wapnia.
Podczas gdy aniony HCO3- Dobrze oddziałują, albo z mostami wodorowymi (lub2Co-H-OH2) lub z atomami wodoru wody w kierunku obciążenia ujemnego (hoco2- H-OH, interakcja dipolowa).
Te interakcje między CA2+, HCO3- A woda jest tak wydajna, że wodorowęglan wapnia jest bardzo rozpuszczalny w tym rozpuszczalniku; W przeciwieństwie do węglanu wapnia (CACO3), w którym atrakcje elektrostatyczne między CA2+ i co32- Są bardzo silne, wytrącając wodny roztwór.
Oprócz wody istnieją ko -molekuły2 wokół, które powoli reagują, aby wnieść więcej HCO3- (W zależności od wartości pH).
Hipotetyczne stałe
Jak dotąd rozmiary jonów i obciążenia wodorowęglanu wapnia, ani obecność wody, nie wyjaśniają, dlaczego nie ma związku stałego; to znaczy czyste kryształy, które można scharakteryzować za pomocą krystalografii X -Ray. Wodorowęglan wapnia jest niczym więcej niż jonami obecnymi w wodzie, z której formacje przepastne nadal rosną.
Tak Ca2+ i HCO3- Mogą odizolować się od wody, unikając następującej reakcji chemicznej:
CA (HCO3)2(aq) → caco3(s) + co2(g) + h2Lub (l)
Następnie można je pogrupować w białą krystaliczną substancję stałą z proporcjami stechiometrycznymi 2: 1 (2HCO3/1ca).
Może ci służyć: 30 przykładów zawiesin chemicznychNie ma badań dotyczących jego struktury, ale można go porównać z strukturą wodorowęglanu sodu (jako wodorowęglan magnezu, Mg (HCO3)2, nie istnieje również jako solidne), ani w przypadku węglanu wapnia.
Stabilność: wodorowęglan sodu (Nahco3) vs. wodorowęglan wapnia (CA (HCO3)2)
Dwodarowęglan sodu krystalizuje w układzie monoklinicznym i wodorowęglan wapnia w systemach trygonalnych (kalcytu) i ortorrombiec (aragonit).
Jeśli NA zostanie zastąpione+ dla CA2+, Sieć krystaliczna byłaby zdestabilizowana przez większą różnicę w rozmiarach; to znaczy na+ Dla bycia mniejszym, tworzy bardziej stabilne szkło z HCO3- w porównaniu do CA2+.
W rzeczywistości CA (HCO3)2(aq) potrzebuje wody do odparowania, aby jej jony mogły być pogrupowane w szklankę; Ale krystaliczna sieć tego nie jest wystarczająco silna, aby to zrobić w temperaturze pokojowej. Podczas ogrzewania wody występuje reakcja rozkładu (równanie z góry).
Bycie jonem na+ W roztworze tworzyłoby to szkło z HCO3- Przed rozkładem termicznym.
Powód, dla którego wodorowęglan wapnia nie krystalizuje (teoretycznie), wynika z różnicy radia jonowych lub rozmiarów ich jonów, które nie mogą utworzyć stabilnego kryształu przed ich rozkładem.
Wodorowęglan wapnia (CA (HCO3)2) vs. węglan wapnia (caco3)
Jeśli z drugiej strony, h jest dodawane+ Do krystalicznych struktur węglanu wapnia, drastycznie zmieniliby swoje właściwości fizyczne. Być może ich punkty topnienia znacznie spadają, a nawet morfologie kryształów kończą się.
Fizyczne i chemiczne właściwości
Wzór chemiczny
CA (HCO3)2
Waga molekularna
162,11 g/mol
Stan fizyczny
Nie pojawia się w stanie stałym. Znajduje się w roztworze wodnym, a gdy ciepło jest stosowane do odparowania, staje się węglanem wapnia.
Rozpuszczalność wody
16,1 g/100 ml w 0º C; 16,6 g/100 ml w 20º C i 18,4 g/100 ml w 100º C.
Wartości te wskazują na duże powinowactwo cząsteczek wody przez jony wodorowęglanu wapnia, jak wyjaśniono w poprzednim rozdziale. Tymczasem zaledwie 15 mg węglanu wapnia rozpuszcza się w litrach wody, co odzwierciedla jego silne interakcje elektrostatyczne.
Ponieważ wodorowęglan wapnia nie może tworzyć substancji stałej, jego rozpuszczalności nie można określić eksperymentalnie.
Jednak biorąc pod uwagę warunki stworzone przez CO2 Rozpuszczone w wodzie otaczającej wapień można obliczyć masę wapnia rozpuszczoną w temperaturze t; masa, która byłaby równa stężeniu wodorowęglanu wapnia.
Może ci służyć: kwas benzyny: synteza, transpozycja i zastosowaniaW różnych temperaturach rozpuszczona masa wzrasta, jak pokazano w wartościach w 0, 20 i 100º C. Następnie, zgodnie z tymi eksperymentami, określa się, ile wodorowęglanu wapnia Rozpuszcza się w pobliżu węglanu wapnia, w wodnym podłożu zgazowanym2.
Gdy CO ucieknie2 Gasowy węglan wapnia wytrąci się, ale nie wodorowęglanem wapnia.
Punkty fuzji i wrzenia
Sieć kryształów CA (HCO3)2 Jest znacznie słabszy niż kako3. Gdyby można go było uzyskać w stanie stałym i zmierzyć temperaturę, w której topi się w źródle, z pewnością uzyskanoby wartość znacznie poniżej 899º C. Podobnie, należy oczekiwać tego samego przy określaniu temperatury wrzenia.
Punkt spalania
To nie jest paliwo.
Ryzyko
Ponieważ ten związek nie istnieje solidnie, jest mało prawdopodobne, aby stanowiło ryzyko manipulowania jego wodnymi roztworami, ponieważ oba jony Ca2+ Jak HCO3- Nie są one szkodliwe dla niskich stężeń; I dlatego największe ryzyko, które byłoby spożywaniem takich rozwiązań, może wynikać tylko z niebezpiecznej dawki połknięcia wapnia.
Jeśli związek utworzył stałą, nawet być może fizycznie różną od kako3, Jego toksyczne działanie nie mogły wykraczać poza prosty dyskomfort i resekcja po kontakcie fizycznym lub inhalacji.
Aplikacje
- Od dawna stosowano roztwory wodorowęglanowe wapnia do mycia starożytnych dokumentów, zwłaszcza dzieł sztuki lub historycznie ważne dokumenty.
- Roztwory wodorowęglanowe zastosowano w zapobieganiu osteoporozie. Jednak w jednym przypadku zaobserwowano działania niepożądane, takie jak hiperkalcemia, alkaloza metaboliczna i niewydolność nerek.
- Od czasu do czasu podaje się wodorowęglan wapnia do skorygowania depresyjnego wpływu hipokaliemii na funkcjonowanie serca.
- Służy do uspokojenia kwasowości żołądka.
Bibliografia
- Wikipedia (2018). Wodorowęglan wapnia. Zaczerpnięte z: w.Wikipedia.org
- Sirah Dubois (3 października 2017 r.). Co to jest wodorowęglan wapnia? Odzyskane z: Livestrong.com
- Science Learning Hub (2018). Chemia węglanu. Odzyskane z: Scientelarn.org.NZ
- Pubchem (2018). Wodorowęglan wapnia. Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov

