Alkeny
- 4583
- 63
- Herbert Wróblewski
 Alkeny lub olefiny są nienasyconymi węglowodorami, które mają co najmniej podwójne wiązanie węglowe w ich strukturze
Alkeny lub olefiny są nienasyconymi węglowodorami, które mają co najmniej podwójne wiązanie węglowe w ich strukturze Co to są alkeny?
Alkeny lub olefiny Są to nienasycone węglowodory, które mają co najmniej podwójne wiązanie w swojej strukturze. Nazywa się je olefinami ze względu na zdolność eteenu lub etylenu do reakcji z halogenami w celu wytworzenia oleju lub oleju. Obecnie termin olefinas został nieużywany, a związki te są teraz nazywane alkenami.
Na właściwości fizyczne alkenów wpływa ich masa cząsteczkowa, a także szkielet gazowany. Na przykład alkeny z 2 do 4 węgli (buteno etene) to gazy. Z 5 do 18 atomami węgla w długim łańcuchu są ciekłe. Podczas gdy alkeny z ponad 18 atomami węgla są stałe.
Obecność podwójnego wiązania zapewnia dużą reaktywność, doświadczając w ten sposób wielu reakcji chemicznych, takich jak dodanie, eliminacja, uwodornienie, nawodnienie i polimeryzacja, które pozwalają mu generować wiele zastosowań i zastosowań.
Alkeny są wytwarzane przemysłowo przez pękanie termiczne o wysokiej masie cząsteczkowej (woski parafinowe); Odwodornienie katalityczne i dehydrokloklowanie chlorowania.
Struktura chemiczna alkenów
 Źródło: Self Made
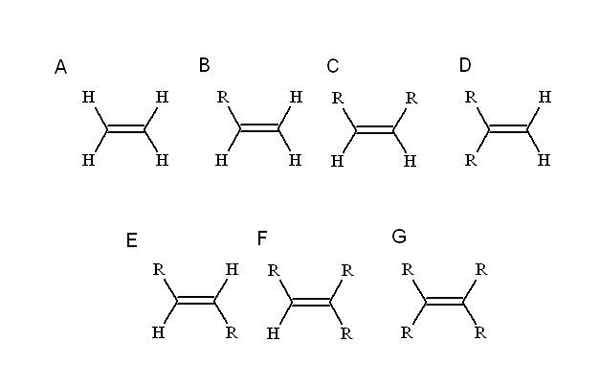
Źródło: Self Made Alkeny charakteryzują się posiadaniem jednego lub więcej podwójnych linków w ich strukturze. Jest to reprezentowane jako c = c, mając oba atomy węgla hybrydyzacja SP2.
Dlatego region łańcucha, w którym podwójne wiązanie jest lub nienasycenie, jest płaski. Zasługuje na to, że dwa węgle można powiązać z dwoma innymi podstawnikami (lub grupami).
Które podstawniki? Każdy, kto zastępuje jeden z najprostszych hydrogenów alkene: etylen (lub Eteno). Począwszy od niego (A, Superior Image) R, który jest alquilowym podstawnikiem, zajmuje miejsce jednego z czterech hydrogenów, które powodują alken.
Jak dotąd, niezależnie od tego, który wodór jest zastąpiony, tożsamość B nie jest zmieniana. Oznacza to, że brakuje mu stereoizomerów, złożonych z równych wzorów chemicznych, ale z innym przestrzennym rozmieszczeniem jego atomów.
Może ci służyć: punkt równoważnościStereoizomery
Gdy drugi wodór jest zastąpiony innym r, jak w C, teraz stereoizomery C, D i E. Wynika to z faktu, że orientacje przestrzenne w odniesieniu do zarówno R mogą się różnić, a w celu wzajemnego rozpoznania, użyte są CIS-Trans lub E-Z.
W C, alken. Jeden jest w pozycji czołowej w stosunku do drugiego. Jeśli dwa R składają się z tego samego podstawnika, na przykład F, to C jest stereoizomerowymi-ciami.
W D obie grupy R są jeszcze bliżej, ponieważ są powiązane z tym samym atomem węgla. Jest to szlachetny stereoizomer, chociaż więcej niż stereoizomer, w rzeczywistości jest to końcowe podwójne wiązanie, to znaczy, że jest on na końcu lub zasadą łańcucha (z tego powodu ma dwa hydrogeny drugi węgiel).
Aw E, najbardziej stabilne z stereoizomerów (lub izomerów geometrycznych), dwie grupy R są oddzielone większą odległością, która przecina przekątną podwójnego wiązania. Dlaczego jest najbardziej stabilny? Dzieje się tak, ponieważ ponieważ przestrzenna separacja między nimi jest większa, więc nie ma napięcia siostrzanego między nimi.
Z drugiej strony, F i G są odpowiednio alkenami w zakresie tri- i tetra. Ponownie nie są w stanie wygenerować żadnego stereoizomeru.
Właściwości fizyczne i chemiczne alkenów
Rozpuszczalność
Są niemiecone z wodą ze względu na ich niską polaryzację. Ale rozpuszczają się w rozpuszczalnikach organicznych.
Punkty fuzji w ºC
Etano -169, Propeno -185, 1 -pentine -165, 1 -Hepteno -119, 3 -Ctein
-101,9, 3 -none -81.4 i 5 -Dechenum -66,3.
Punkt wrzenia w º C
Etano -104, Propeno -47, trans2buteno 0,9, cis2buteno 3,7, 1-penten 30, 1-hepteno 115, 3-ok 122, 3-noneno 147 i 5-gruntowne.
Może Ci służyć: filtr laboratoryjny): Charakterystyka, funkcje, typyTemperatura wrzenia wzrasta w bezpośrednim związku z liczbą węgli alkene. Z drugiej strony, im bardziej rozgałęziona struktura, najsłabsi to interakcje międzycząsteczkowe, co znajduje odzwierciedlenie w spadku punktu wrzenia lub fuzji.
Gęstość
Etano 0,6128 mg/ml, Propeno 0,6142 mg/ml i 1-buten 0,6356 mg/ml, 1-pente 0,64 mg/ml i 1-heksen 0,673.
W alkenach maksymalna gęstość wynosi 0,80 mg/ml. To znaczy są mniej gęste niż woda.
Biegunowość
Zależy to od struktury chemicznej, podstawień i obecności innych grup funkcjonalnych. Alkeny mają wkładki, a zatem 2-butenowy izomer cis.
Reaktywność alkenów
Alkeny mają doskonałą zdolność do reagowania ze względu na podwójne linki, które mają. Wśród zaangażowanych reakcji są: dodanie, eliminacja, wymiana, uwodornienie, nawodnienie i polimeryzacja.
Reakcja dodania
H2C = CH2 + Cl2 => Clch2-Cclh2 (Dichlorek etylenu)
Reakcja uwodornienia
Występuje w wysokich temperaturach i w obecności odpowiednich katalizatorów (PT, PD lub drobno podzielone)
Ch2= Ch2 + H2 => Ch3-Ch3 (Etano)
Reakcja nawodnienia
Reakcja, która jest źródłem wytwarzania alkoholu z pochodnych oleju:
H2C = CH2 + H2O => h3C-ch2Och (alkohol etylowy)
Reakcje polimeryzacji
Etylen w obecności katalizatorów, takich jak próby glinu i polimeryza tetrachlorku tytanu w polietylenu, która zawiera około 800 atomów węgla. Ten typ polimeru nazywa się polimerem dodatkowym.
Zastosowania i zastosowania alkenów
Polimery
- Polietylen o niskiej gęstości jest stosowany w produkcji toreb, tworzyw sztucznych szklarni, opakowań, naczyń, naczyń itp. Podczas gdy wysoka gęstość jest bardziej sztywna i mechanicznie odporna, stosowanie w produkcji pudeł, mebli, obrońców, takich jak hełmy i kolana, zabawki i palety.
- Polipropylen, polimer propylenowy, jest stosowany w opracowywaniu pojemników, arkuszy, sprzętu laboratoryjnego, zabawek, filmów opakowaniowych, włókien sogas, tapicerki i dywanów.
- Chlorek poliwinylu (PVC) to polimer chlorku winylu, który jest stosowany w produkcji rur, płytek do podłóg, kanałów, drzwi i ramek okien, itp.
- PolyButadiena, polimer 1,3-butadiena, jest przeznaczony do produkcji pasm łożyskowych, węży i pasów pojazdów, a także do powlekania metalicznych puszek.
- Kopolimery etylenu i propylenu są stosowane w produkcji węży, ciała i części podwozia do tekstyliów itp.
Alkeny
- Są one stosowane do uzyskiwania rozpuszczalników, takich jak glikol etylenowy i dioksan. Glikol etylenowy jest stosowany jako środek przeciw zamarzaniu w grzejnikach samochodowych.
- Etylen jest hormonem roślin, który kontroluje jego wzrost, kiełkowanie nasion i rozwój owoców. Dlatego służy do wywołania dojrzewania bananów, gdy dotrą do miejsca docelowego.
- Są one stosowane jako surowiec do produkcji wielu związków, takich jak halogendy alkilowe, tlenek etylenu, a zwłaszcza etanol. Mieli również zastosowanie w branży, opiece osobistej i medycynie.
- Są one używane do uzyskiwania i produkcji lakierów, detergentów, aldehydów i paliw. 1.3-butadieno jest używany jako surowiec w produkcji gumów syntetycznych.
Bibliografia
- Przypisanie chemii. Właściwości fizyczne alkenów. Zaczerpnięte z: Chemia-Assignment.com
- Wikipedia. (2018). Alkene. Zaczerpnięte z: w.Wikipedia.org
- Chemia librettexts. Właściwości fizyczne alkenów. Zaczerpnięte z: chem.Librettexts.org
- Whitten, Davis, Peck i Stanley. Chemia. (8 wyd.). Cengage Learning.
- Francis a. Szylkret. Chemia organiczna. (Szósta edycja., Strona 194). MC Graw Hill.
- Houchton Mifflin Harcourt. (2016). Alkeny: wzory molekularne i strukturalne. Zaczerpnięte z: cliffsnotes.com
- Chipera, Angie. (25 kwietnia 2017 r.). Co to jest olefin w chemii? Naukowe. Zaczerpnięte z: naukowca.com

