Struktura alkoholowa, właściwości, zastosowania i ryzyko izoamilico
- 3142
- 528
- Pani Gilbert Stolarczyk
On Alkohol izoamylowy Jest to związek organiczny, którego wzór jest (ch3)2Chch2Ch2Oh. Mówienie chemiczne jest rozgałęzionym alkoholem pierwotnym i stanowi jeden z izomerów pentanolowych, zwany alkoholem amylowym (c5H12ALBO).
Podobnie jak wiele alkoholi o niskiej masie cząsteczkowej, jest to bezbarwna ciecz w temperaturze pokojowej. Umożliwia to i ułatwia, że jest on używany jako rozpuszczalnik do różnych zastosowań; Ponadto, gdy nie wywiera zbyt wielu negatywnych skutków na ekosystem po odrzuceniu.
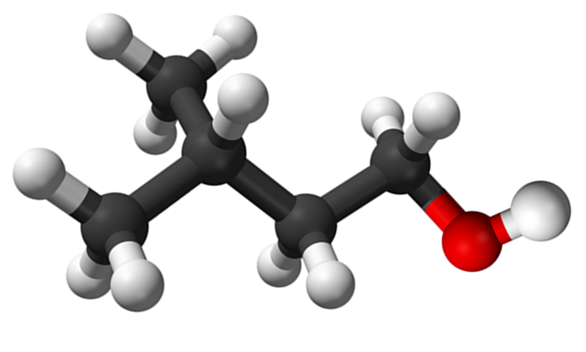
 Izoamiliczna cząsteczka alkoholu. Źródło: Claudio Pistilli de Wikipedia.
Izoamiliczna cząsteczka alkoholu. Źródło: Claudio Pistilli de Wikipedia. Chociaż jest to materiał pośredni w syntezie octanu amilo w celu opracowania zapachów bananów, jego własny zapach jest nieprzyjemny i podobny do gears.
Oprócz służenia jako rozpuszczalnik wielu substancji biologicznych i jako pośrednik w syntezie innych octanów, zmniejsza napięcie powierzchniowe niektórych preparatów przemysłowych, zapobiegając tworzeniu się pianki. Dlatego jest stosowany w systemach mikro -emulsyjnych.
Jeśli chodzi o jego naturalne pochodzenie, alkohol izoamiliczny znaleziono w Horomonach Hornets, a także w czarnych truflach, rodzajem grzybów położonych na Europie na południowy wschód.
[TOC]
Struktura izoamilico
Na górnym obrazie pokazano cząsteczkę alkoholu izoamylowego reprezentowaną za pomocą kulek i modelu słupków. Po prawej stronie, czerwona kula odpowiada atomowi tlenu grupy OH, charakterystycznej dla wszystkich alkoholi; Po lewej stronie znajduje się szkielet gazowany z grupą metylową, Cho3, Własanie struktury.
Z molekularnego punktu widzenia związek ten jest dynamiczny w przypadku atomów z hybrydycjami SP3, ułatwianie rotacji ich linków; tak długo, jak nie powoduje zaćmienia OH i3.
Warto również wspomnieć o swojej cechach amfifilowych: ma on apolowy lub hydrofobowy koniec, utworzony przez łańcuch (ch3)2Chch2Ch2-, oraz polarna lub hydrofilowa głowa, grupa OH. Ta definicja dwóch konkretnych obszarów różnych polaryzacji sprawia, że ten alkohol jest zawrotnym; I stąd ma zastosowanie mikroemulsji.
Może ci służyć: zasada dźwigniInterakcje międzycząsteczkowe
Biorąc pod uwagę obecność grupy OH, izoamiliczna cząsteczka alkoholu przedstawia stały moment dipolowy. W konsekwencji dipol-dipol.
Podczas gdy gałąź głównych łańcuchów zmniejsza skuteczne interakcje między cząsteczkami, mosty wodoru w tym alkoholu kompensują to zejście, powodując gotowanie cieczy w 131 ° C, temperaturę wyższą niż temperatura wrzenia wody.
Nie zdarza się to z jego stałym lub „lodem”, który topi się do -117 ° C, co wskazuje, że jego interakcje międzycząsteczkowe nie są wystarczająco silne, aby utrzymać ich cząsteczki uporządkowane; Zwłaszcza jeśli grupa cho3 który gałęzie łańcuch główny zapobiega lepszemu kontaktowi między cząsteczkami.
Nieruchomości
Wygląd fizyczny
Bezbarwny płyn.
Zapach i smak
Odrzuca nieprzyjemny zapach podobny do gruszki i ma ostry smak.
Masa cząsteczkowa
88 148 g/mol.
Gęstość
0,8104 g/ml w 20 ° C. Jest zatem mniej gęsty niż woda.
Gęstość pary
Jest 3,04 razy gęstszy niż powietrze.
Ciśnienie pary
2,37 mmHg w 25 ° C.
Punkt wrzenia
131,1 ° C.
Temperatura topnienia
-117,2 ° C.
punkt zapłonu
43 ° C (zamknięty kubek).
Temperatura samo -kierunkowego
340 ° C.
Rozpuszczalność
Jest stosunkowo rozpuszczalny w wodzie: 28 g/l. Wynika to z faktu, że wysoce polarne cząsteczki wody nie odczuwają szczególnego powinowactwa do gazowanego łańcucha alkoholu izoamylowego. Gdyby mieszane, zaobserwowanoby dwie fazy: dolna, odpowiadająca wody i lepszy, alkohol izoamylowy.
W przeciwieństwie do tego, jest znacznie bardziej rozpuszczalny w mniej polarnych rozpuszczalnikach, takich jak: aceton, eter, chloroform, etanol lub kwas octowy lodowcowy; i nawet w eterze olejowym.
Może ci służyć: termometr laboratoryjny: Charakterystyka, do czego służy, przykładyBreja
3738 CP w 25 ° C.
Napięcie powierzchniowe
24,77 din/cm A 15 ° C.
Współczynnik załamania światła
1 4075 do 20 ° C.
Pojemność cieplna
2382 kJ/g · k.
Aplikacje
Surowiec
Od izoamilowego alkoholu innych estrów, tiofenu i leków, takich jak azotyn amilo -azotu, VAVOL (ISAVALERATE PERSILE), bromisoval (Bromobalerilurea), Corvalol (kallerski tranquanar) i Barbamil (amobarbital) (amobarbital) (amobarbital) (amobarbital) (amobarbital) (amobarbital) (amobarbital) (amobarbital) (amobarbital).
Zapachy
Oprócz zastosowania do syntezy octanu amilo, który ma aromat bananowy, uzyskane są również inne zapachy owocowe, takie jak morela, pomarańcze, śliwki, wiśni i słód. Dlatego jest to niezbędny alkohol w opracowaniu wielu produktów jadalnych lub kosmetyków.
Antypumant
Zmniejszając napięcie powierzchniowe, promuje jego zastosowanie w systemach mikro -emulsyjnych. Praktycznie unikaj przyspieszonej tworzenia się bańki, zmniejszając ich rozmiar, aby je złamać.
Pomaga także lepiej zdefiniować interfejs między fazami wodnymi i organicznymi podczas ekstrakcji; Na przykład jest dodawany do mieszanki ekstraktora fenol-chloroformu w proporcji 25: 1. Ta technika jest przeznaczona do ekstrakcji DNA.
Ekstrakcje
Alkohol izoamylowy pozwala również wydobywać tłuszcze lub oleje z różnych próbek, na przykład mleko. Również rozpuszczenie wosku parafinowego, atramentów, gumy, lakierów i estrów celulozowych.
Kontynuując ekstrakcje, dzięki nim można uzyskać kwas fosforowy z fosforowych roztworów mineralnych żelaza.
Ryzyko
Przechowywanie i reaktywność
Jak każdy ciecz, który wydziela zapachy, może reprezentować nieuchronne ryzyko pożaru, jeśli miejsce, w którym jego temperatura jest zbyt przechowywana, tym bardziej, jeśli jest już źródło ciepła.
W tych warunkach po prostu działa jak paliwo, karmiąc płomienie, a nawet wykorzystując jego pojemnik. Po oparzeniu, uwalnianie oparów, które mogą wpływać na zdrowie i powodować uduszenie.
Może ci służyć: analiza ilościowa w chemii: pomiary, przygotowanieInne przyczyny, które są podpalające alkohol izoamiliczny, jest mieszanie go lub reagowanie z substancjami takimi jak: nadtlenki, brome.
Zdrowie
W kontakcie ze skórą możesz podrażniać i wysuszyć. Objawy są jednak poważniejsze, jeśli są wdychane zbyt długo (kaszel, oparzenia nosa, gardło i płuca) lub jeśli są spożyte (ból głowy, nudności, biegunka, wymioty, zawroty głowy i utrata wiedzy).
I wreszcie, kiedy rozlewa się w oczach, irytuje je, a nawet może ich wyrządzić szkodę. Na szczęście zapach „alkoholowych gruszek” pozwala wykryć go w przypadku ucieczki lub rozlania; Oprócz tego jest to związek, który musi być manipulowany z szacunkiem.
Bibliografia
- Morrison, r. T. i Boyd, R, N. (1987). Chemia organiczna. 5. edycja. Redakcja Addison-Wesley Inter-American.
- Carey f. (2008). Chemia organiczna. (Szósta edycja). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Chemia organiczna. Aminy. (10. edycja.). Wiley Plus.
- Wikipedia. (2019). Alkohol izoamylowy. Źródło: w:.Wikipedia.org
- National Center for Biotechnology Information. (2019). Alkohol izoamylowy. Baza danych Pubchem. CID = 31260. Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov
- Zhang Yu i Muhammed Mamoun. (17 września 2008 r.). Ekstrakcja kwasu fosforowego z roztworów azotanowych z alkoholem izoamylowym. Ekstrakcja rozpuszczalnika i wymiana jonowa Tom 6, 1988 - Wydanie 6. doi.Org/10.1080/07366298808917973
- Departament Zdrowia w New Jersey. (2008). Alkohol izoamylowy. [PDF]. Odzyskane z: NJ.Gov
- Kat Chem. (2019). Alkohol izoamylowy. Odzyskany z: kat-chem.Hu
- Chemoxy International Ltd. (S.F.). Alkohol izoamylowy. Odzyskane z: chemoksy.com
- « Struktura, właściwości, zastosowania i ryzyko trietilaminy
- Liechtenstein Historia i znaczenie flagi »

